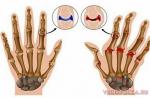
Septicemie - Aceasta este o boală infecțioasă gravă în care bacteriile patogene, toxinele lor și substanțele inflamatorii produse în organism, depășesc imunitatea de apărare și se răspândesc în tot corpul.
Fapte Sepsis:
- În Statele Unite, sunt raportate anual aproximativ 500.000 de cazuri de sepsis.
- Sepsisul se caracterizează prin mortalitate ridicată. În Statele Unite, aproximativ 100.000 de pacienți mor din cauza acestei boli în fiecare an.
- În fiecare oră în Statele Unite, sepsisul ucide 25 de persoane.
- Două treimi din pacienți apelează inițial la medici pentru alte boli și abia ulterior dezvoltă sepsis.
- Asistența medicală în țările dezvoltate cheltuiește foarte mult pe tratamentul sepsisului. De exemplu, în SUA - 17 miliarde de dolari pe an.
- Prevalența sepsisului este în creștere în majoritatea țărilor dezvoltate. Acest lucru se datorează faptului că proporția populației în vârstă este în creștere, speranța de viață la persoanele cu boli cronice și infecție cu HIV este în creștere. Aceste persoane prezintă un risc ridicat.
Cauzele sepsisului
Microorganisme care provoacă sepsis
Sepsisul este o infecție. Pentru dezvoltarea sa, este necesar ca agenții patogeni să intre în corpul uman.Principalii agenți cauzali ai sepsisului:
- Bacterii: streptococi, stafilococi, protea, Pseudomonas aeruginosa, acinetobacter, Escherichia coli, enterobacter, citrobacter, Klebsiella, enterococ, fusobacterii, peptococi, bacteroizi.
- Fungus. Practic - ciuperci asemănătoare cu drojdia din genul Candida.
- Viruși. Sepsisul se dezvoltă atunci când o infecție virală severă este complicată de o infecție bacteriană. Cu multe infecții virale, se observă o intoxicație generală, agentul patogen este transportat cu sânge în tot corpul, dar semnele unor astfel de boli diferă de sepsis.
Apărările corpului
 Pentru apariția sepsisului este necesară pătrunderea agenților patogeni în corpul uman. Dar în cea mai mare parte, ele nu provoacă tulburări grave care însoțesc boala. Mecanismele de protecție încep să funcționeze, care în această situație sunt redundante, excesive, duc la deteriorarea propriilor țesuturi.
Pentru apariția sepsisului este necesară pătrunderea agenților patogeni în corpul uman. Dar în cea mai mare parte, ele nu provoacă tulburări grave care însoțesc boala. Mecanismele de protecție încep să funcționeze, care în această situație sunt redundante, excesive, duc la deteriorarea propriilor țesuturi. Orice infecție este însoțită de un proces inflamator. Celulele speciale secretă substanțe biologic active care determină fluxul sanguin afectat, deteriorarea vaselor de sânge, funcționarea afectată a organelor interne.
Aceste substanțe biologic active sunt numite mediatori inflamatori.
Astfel, sepsisul este cel mai bine înțeles ca răspunsul inflamator patologic al organismului însuși, care se dezvoltă ca răspuns la introducerea agenților infecțioși. La diferite persoane, acesta este exprimat în grade diferite, în funcție de caracteristicile individuale ale reacțiilor de protecție.
Adesea cauza dezvoltării sepsisului este bacteriile patogene condiționate, cele care nu sunt capabile să producă rău în normă, dar în anumite condiții pot deveni agenți patogeni ai infecțiilor.
Ce boli sunt cel mai adesea complicate de sepsis?

- Rănile și procesele purulente la nivelul pielii.
- Osteomielita este un proces purulent în oase și măduva osoasă roșie.
- Dureri de gât severe.
- Otită medie purulentă (inflamație a urechii).
- Infecție în timpul nașterii, avort.
- Boli oncologice, în special în etapele ulterioare, cancerul de sânge.
- Infecția HIV în stadiul SIDA.
- Leziuni extinse, arsuri.
- Infecții diverse.
- Boli infecțioase și inflamatorii ale sistemului urinar.
- Boli infecțioase și inflamatorii ale abdomenului, peritonită (inflamația peritoneului - o peliculă subțire care se încadrează în interiorul cavității abdominale).
- Tulburări congenitale ale sistemului imunitar.
- Complicații infecțioase și inflamatorii după operație.
- Pneumonia, procese purulente în plămâni.
- Infecție nosocomială. Adesea, în spitale circulă microorganisme speciale, care în timpul evoluției au devenit mai rezistente la antibiotice și diverse influențe negative.
Uneori, boala inițială care a cauzat sepsis nu poate fi detectată. În timpul testelor de laborator, nu se găsesc agenți patogeni în corpul pacientului. Această sepsis se numește criptogenă.
De asemenea, sepsisul nu poate fi asociat cu infecția - în acest caz, apare ca urmare a pătrunderii bacteriilor din intestin (care în mod normal trăiesc în ea) în sânge.
Un pacient cu sepsis nu este contagios și nu este periculos pentru alții - aceasta este o diferență importantă față de așa-numitele forme septice în care pot apărea unele infecții (de exemplu, scarlatină, meningită, salmoneloză). Cu o formă septică de infecție, pacientul este contagios. În astfel de cazuri, medicul nu va diagnostica sepsis, deși simptomele pot fi similare.
Tipuri de sepsis
 În funcție de timpul de curgere:
În funcție de timpul de curgere:- galopant (Cea mai clara). Toate simptomele apar și cresc foarte repede. Munca organelor interne este grav perturbată. Starea pacientului se deteriorează rapid. După 1-2 zile, poate apărea moartea.
- Acut.Simptomele cresc boala mai lentă durează până la 6 săptămâni.
- subacută. De obicei, se desfășoară de la 6 săptămâni la 3-4 luni.
- Recurent. Durează până la șase luni sau mai mult. În loc să îmbunătățească starea pacientului apar noi exacerbări - boala se desfășoară în valuri.
- Criozapsie (sepsis cronic). Durează mult timp, câțiva ani. Există un focal de inflamație care nu se vindecă mult timp. Apărările corpului sunt reduse.
 În funcție de schimbările din corp:
În funcție de schimbările din corp:- Septicemie - o afecțiune în care starea generală a organismului este perturbată, în el apare o reacție inflamatorie sistemică, dar nu există focare de inflamație purulentă în organele interne. Această formă se desfășoară cel mai adesea brusc sau cu viteză fulger.
- Septicopyemia- o formă de sepsis în care abcesele se formează în diferite organe.
- Endocardită septică- Un tip de septicemie în care focalizarea inflamației este pe suprafața valvelor inimii.
- dobândit-comunitar - infecția s-a produs în afara pereților spitalului.
- nosocomiale- infecția a apărut în spital după operație, injecție, naștere, avort, diverse proceduri medicale.
Ce este sepsisul și ce nu?
 Afecțiuni legate de sepsis care nu sunt sepsis:
Afecțiuni legate de sepsis care nu sunt sepsis: - bacteriemie - Bacteriile și toxinele lor sunt în sânge, dar nu are loc o reacție inflamatorie sistemică puternică.
- Sindromul de răspuns inflamator sistemic - un concept mai general. Indică reacția organismului sub forma unui proces inflamator sistemic la orice efect dăunător. Sepsisul este una dintre soiurile acestei afecțiuni atunci când o infecție acționează ca un factor care are un efect dăunător.

Componente obligatorii ale sepsisului:
- Prezența unui focal, sursă de infecție, în organism. Din aceasta provin bacteriile și toxinele lor intră în fluxul sanguin.
- Răspândirea agenților patogeni cu sânge. Sunt transportate în tot corpul.
- Răspunsul este un sistem de apărare. Inflamația generalizată se dezvoltă în întregul corp.
Simptomele sepsisului
Simptomele septicemiei
Caracteristicile septicemiei:- De obicei are un fulger sau un curs acut. De obicei durează câteva zile.
- Se desfășoară într-o formă severă, însoțită de o deteriorare semnificativă.
- Cel mai frecvent în rândul copiilor, în special până la 3 ani.
- Cele mai frecvente agenți patogeni sunt streptococul și bacteriile stafilococice.
- Adesea boala începe ca o infecție respiratorie, simptomele pot crește literalmente în fața ochilor. Uneori, viața pacientului depinde de cât de rapid este început tratamentul.
- Focusul de la care se răspândește infecția este cel mai adesea mic, abia sesizabil. Uneori nu poate fi identificată deloc.
| Simptom | Mecanismul de apariție și descriere |
| Creșterea temperaturii până la 39-40 °C. | Toxinele bacteriene și substanțele active inflamatorii secretate în organism afectează centrul creierului, care este responsabil de reglarea temperaturii corpului. Ca urmare, începe să se genereze căldură „în exces” în organism. Acest lucru apare cu multe infecții. Simptome care însoțesc febra:
 |
| Hemoragii sub piele. | Toxinele bacteriene și propriul sistem imunitar deteriorează pereții vaselor de sânge, în urma cărora se izbesc, se formează hemoragii.
 |
| Încălcarea condiției generale. | Simptome:
|
| Gălbenimea pielii și a mucoaselor. | Apare din cauza funcției hepatice afectate. În mod normal, acest organism ar trebui să proceseze bilirubina, un produs de descompunere a hemoglobinei. În caz de afectare a funcției hepatice, bilirubina neprocesată intră în sânge, se instalează în piele și în creier.  |
| Tulburări respiratorii, circulatorii. | Simptome:
|
| Tulburări digestive | Ele apar ca urmare a afectării stomacului, intestinelor, pancreasului. Simptome: |
Septicemia este dificilă, are un prognostic grav. Pacientul trebuie dus imediat la spital. Tratamentul trebuie început cât mai devreme.
Simptomele septicopyemiei
Caracteristici ale septicopiemiei:- Focusul de la care a început să se răspândească infecția este întotdeauna clar. Acesta este adesea un abces mare.
- Există abcese în alte organe.
- Această formă de sepsis este mai puțin severă și mai lungă (câteva săptămâni) în comparație cu septicemia.
- Putem spune că septicopemia este o reacție mai „corectă” a organismului la infecție în comparație cu septicemia.
- Principalii agenți patogeni sunt stafilococul și Pseudomonas aeruginosa. Adesea, aceste două tipuri de bacterii provoacă boala împreună.
- Când bacteriile încep să se răspândească în tot corpul, primele ulcerații apar în plămâni, apoi, de regulă, în ficat, splină, măduvă osoasă, sub piele, în articulații.
| Simptom | Mecanismul de apariție, descriere |
| Creșterea temperaturii până la 40 ° C. | Temperatura corporală a unui pacient cu septicopyemia se modifică în valuri. Se ridică în timpul următoarei intrări de bacterii în sânge. Durerea de cap severă începe să deranjeze, pacientul devine letargic, iritabil sau, dimpotrivă, letargic, apetitul este deranjat. Apoi vine îmbunătățirea.  |
| Deteriorarea inimii și vaselor de sânge. | Bacteriile care circulă în sânge și toxinele lor afectează mușchiul inimii, îi perturbă activitatea. Ca urmare a inflamației peretelui vascular și a formării cheagurilor de sânge, fluxul sanguin este perturbat. Se poate dezvolta endocardita, o inflamație a mucoasei interioare a căptușelii inimii din interiorul camerei sale. Acest lucru afectează supapele inimii. Simptome:
|
| Deteriorarea rinichilor. |
|
| Afectarea ficatului. |
|
| Inflamația plămânilor (pneumonie). |
|
| Deteriorarea creierului și a membranelor sale (meningită, encefalită, meningoencefalită). |
|
| Afectare articulară (artrită purulentă). | Simptome:
|
În cazul septicopyemiei, prognosticul pentru pacient este mai favorabil decât în \u200b\u200bcazul septicemiei. Cu toate acestea, acest tip de sepsis este de asemenea pericol pentru viață și necesită un tratament imediat imediat.
Simptomele endocarditei septice
Cu endocardita septică, există simptome similare cu cele ale sepsisului.:- Creșterea temperaturii corpului, febră.
- Încălcarea sănătății generale: slăbiciune, slăbiciune, dureri de cap.
- Micii noduli dureroși pe palme, degete.
- Culoarea pielii "cafea cu lapte".
- Hemoragii pe piele.
- Durere în mușchi și articulații.
- Pierdere în greutate.
 Posibile simptome ale anomaliilor valvului cardiac:
Posibile simptome ale anomaliilor valvului cardiac:
- senzația de pulsare a vaselor de sânge în cap și gât;
- bătăi rapide ale inimii crescute;
- dureri de cap, tinitus, „zboară înaintea ochilor”;
- conștiința afectată;
- durere în spatele sternului (angina pectorală);
- dispnee;
- aritmie (tulburarea ritmului cardiac);
- scăderea tensiunii arteriale;
- tuse (poate fi cu sânge).
Simptomele croniozei
Caracteristici ale cronicilor:- curs prelungit, de obicei de câțiva ani;
- scăderea apărărilor corpului;
- încălcarea sănătății generale, epuizare;
- slăbiciune;
- disfuncția ficatului, inimii, splinei, altor organe;
- corpul are o concentrare purulentă mare, care nu se vindecă mult timp (poate fi un dinte carosit, o amigdală inflamată, supurație la locul plăgii etc.)
Complicații de sepsis
| Complicaţie | Descriere |
| Șoc septic | Cea mai severă complicație a sepsisului. Munca tuturor organelor, metabolismul, fluxul sanguin este perturbată. Cel mai mare risc de a dezvolta șoc septic la vârstnici cu pacienți imunocompromisi. Până la jumătate din toți pacienții cu această complicație mor. Simptomele șocului septic:
|
| Pierdere în greutate, epuizare | Statisticile arată că fiecare al patrulea pacient cu sepsis pierde aproximativ 20% din masă. |
| Sângerare | Ca urmare a afectării vasculare în timpul sepsisului, sângerarea internă se poate dezvolta în diferite organe, de exemplu în stomac. Starea pacientului se agravează, apare paloare, slăbiciune. |
| Tromboflebita | Tromboflebita este o inflamație a peretelui venos cu formarea de cheaguri de sânge pe ea. Simptome:
 |
| Embolie pulmonară | Cel mai adesea este o complicație a tromboflebitei. Odată cu tromboembolismul, o bucată de tromb iese, intră cu un flux de sânge în inimă, apoi în vasele pulmonare. Ajungând la un vas suficient de mic, un cheag de sânge îl blochează. Simptome:
 |
| Tromboembolism cerebral | De obicei este o complicație a tromboflebitei. Adesea apare noaptea. Simptome:
 |
Examinarea sepsisului
| Titlul studiului | Descriere | Cum se realizează? |
| Analiza generală a sângelui | Modificări ale sepsisului:
| Sângele este luat în mod obișnuit de la un deget sau de la o venă.  |
| Chimia sângelui | Aceștia evaluează conținutul diferitelor substanțe din sânge, acest lucru ajută la identificarea tulburărilor din diferite organe interne. | Sângele pentru analiză este colectat dintr-o venă stomacală goală.  |
| Cultura de sânge pentru sterilitate (sinonime: cultura de sânge pentru microflora, cultura de sânge). | Studiul ajută la detectarea agenților patogeni ai sepsisului, la determinarea sensibilității acestora la medicamentele antibacteriene. | Sângele este eliminat dintr-o venă și trimis la un laborator. Studiul oferă cele mai precise rezultate înainte de începerea tratamentului cu antibiotice .; |
| Test de coagulare a sângelui | Se efectuează în cazul în care sepsisul este însoțit de formarea de cheaguri de sânge, sângerare. | Sângele pentru analiză este prelevat dintr-o venă. |
Tratamentul cu Sepsis
Am nevoie de spitalizare pentru sepsis?
Sepsisul este o boală gravă care este însoțită de o defecțiune a tuturor organelor, este o amenințare la viața pacientului. Prin urmare, spitalizarea este obligatorie. Cel mai adesea, tratamentul se efectuează în secția de chirurgie sau în secția de terapie intensivă.Adesea, un pacient este internat într-un spital cu o altă boală, iar ulterior, ca o complicație, dezvoltă sepsis.
Tratament complet pentru sepsis
Tratamentul pentru sepsis include:- antibioterapie - utilizarea medicamentelor antibacteriene care distrug agentul patogen;
- imunoterapie - utilizarea de medicamente care cresc apărarea organismului;
- utilizarea de medicamente care elimină simptomele sepsisului, tulburări în organism, restabilesc activitatea organelor interne;
- tratament chirurgical - eliminarea focurilor purulente din organism.
Tratament cu antibiotice
 Regulile terapiei cu antibiotice pentru sepsis:
Regulile terapiei cu antibiotice pentru sepsis:- tratamentul trebuie să înceapă imediat, cât mai curând posibil;
- medicul alege medicamentele în funcție de sensibilitatea agentului patogen la anumite tipuri de antibiotice, care este stabilit în timpul culturii de sânge;
- de obicei prescrise 2-3 medicamente diferite în cele mai mari doze posibile;
- În medie, antibioterapia poate dura de la 6 la 10 săptămâni.
- peniciline;
- cefalosporine;
- aminoglicozide;
- carbapeneme;
- lincosamide;
- antibiotice din grupul cloramfenicolului etc.
Tratament imunostimulant
 Un pacient cu sepsis a redus imunitatea. Organismul nu este capabil să reziste în mod adecvat la infecții. Pentru a corecta această afecțiune, se folosesc medicamente speciale - imunostimulante.
Un pacient cu sepsis a redus imunitatea. Organismul nu este capabil să reziste în mod adecvat la infecții. Pentru a corecta această afecțiune, se folosesc medicamente speciale - imunostimulante. Imunostimulante care sunt utilizate pentru sepsis și alte boli infecțioase:
- thymalin;
- taktivin;
- thymoptin;
- thymactide;
- vilosen;
- myelopidul;
- thymogenul;
- immunofan;
- nucleinat de sodiu;
- ribomunyl;
- bronho-munal;
- biostim;
- levamisol și alții
Infuzie intravenoasă de diferite soluții în sepsis (terapie perfuzabilă)
 Scopul perfuziei intravenoase a diferitelor soluții în sepsis:
Scopul perfuziei intravenoase a diferitelor soluții în sepsis:- O creștere a volumului de sânge în organism, datorită căreia circulația normală a sângelui este restabilită.
- Restabilirea distribuției normale a fluidului în organism.
- Restaurarea proprietăților fizico-chimice normale ale plasmei (partea lichidă a sângelui).
- Îmbunătățirea fluxului de sânge în vasele mici: organele încep să primească mai mult oxigen și nutrienți cu sânge.
- Excreția de toxine bacteriene, substanțe inflamatorii.
Pentru perfuzie intravenoasă prelungită de soluții într-o venă, este instalat un cateter special.
Nutriția pacientului
Mulți pacienți cu sepsis sunt în stare gravă și nu pot mânca singuri. Mai mult, corpul lor trebuie să primească zilnic 1,5-2 g de proteine \u200b\u200bpe kilogramul de greutate corporală și 40-50 kcal pe kilogramul de greutate corporală.Metode de hrănire a pacienților cu sepsis care nu sunt capabili să mănânce singuri:
- Printr-un tub gastric, care este un tub, de obicei introdus prin nas.
- intravenosfolosind soluții speciale.
Alte medicamente utilizate în sepsis
- medicamente care restabilesc funcțiile organelor interne: inimă, ficat, rinichi, etc .;
- vitamine și antioxidanți;
- medicamente pentru creșterea tensiunii arteriale;
- medicamente care îmbunătățesc circulația sângelui în vasele mici etc..
Interventie chirurgicala
 În timp ce accentul infecției rămâne în corpul pacientului, tratamentul cu antibiotice și alte medicamente nu va aduce efectul dorit. Prin urmare, tratamentul chirurgical trebuie să fie efectuat cât mai devreme.
În timp ce accentul infecției rămâne în corpul pacientului, tratamentul cu antibiotice și alte medicamente nu va aduce efectul dorit. Prin urmare, tratamentul chirurgical trebuie să fie efectuat cât mai devreme. Chirurgul conduce:
- autopsia abcesului;
- purificarea sa de puroi;
- eliminarea tuturor țesuturilor neviabile care otrăvesc organismul cu produsele lor de descompunere;
- spălarea cu antiseptice, asigurând fluxul de conținut.
O creștere a temperaturii corpului în perioada postoperatorie nu este neapărat o manifestare a infecției. Cel mai
infecțiile după operații obstetrice și ginecologice sunt cauzate de microflora endogenă a tractului genital inferior. Prevenirea infecțiilor postoperatorii constă în respectarea tehnicilor chirurgicale de precizie și a terapiei cu antibiotice profilactice.
Febra postoperatorie este o creștere a temperaturii până la 38 ° C și mai mare în două măsurători cu un interval de cel puțin 6 ore mai mult de 24 de ore după operație.
Frecvența infecțiilor după histerectomie abdominală este cuprinsă între 3,9 și 50% din cazuri; după histerectomie vaginală - de la 1,7 la 64%. Frecvența tromboflebitei pelvine septice după operația ginecologică este de 0,1-0,5%.
Flora vaginala. Numărul de microorganisme din conținutul vaginal este de 108-109 bacterii la 1 ml, reprezentat atât de microflora aerobă, cât și de anaerobă (38.1).
Profilaxia antibiotică și tratamentul vaginal cu antiseptice înainte de operație au ca scop tocmai reducerea cantității acestei microflore vaginale. Intervenția chirurgicală încalcă compoziția cantitativă și calitativă a microflorei tractului genital. După histerectomia vaginală și abdominală, numărul de lactobacili scade și conținutul de bacili gram-negativi, B. fragilis și enterococi crește. Spitalizarea preoperatorie ajută la creșterea mai multor microorganisme virulente în conținutul vaginului.
Factorii de risc pentru infecția postoperatorie sunt:
Tulburare imunitară
Vârsta premenopauză
obezitatea
Chirurgie radicală
Vaginoza bacteriană
Spitalizare preoperatorie îndelungată
Pierderea excesivă de sânge intraoperator
Tehnica operațională imperfectă
Stare socioeconomică scăzută
subnutriție
Cantitate excesivă de țesut devitalizat
Diabet
Lipsa profilaxiei antibiotice
Intervenția chirurgicală într-un câmp chirurgical infectat
Un factor de risc semnificativ pentru infecția postoperatorie este o încălcare a stării imune a pacientului.
Etiologia. Virulența bacteriilor și volumul de inoculare depind de statutul imunitar al organismului gazdă; acești factori pot fi reduceți datorită profilaxiei antibiotice.
Pericultita (celulita ciotului vaginal) este o infecție a marginilor chirurgicale ale părții superioare a vaginului după o histerectomie. Simptomele pot apărea chiar în spital sau după externarea pacientului. Perioada postoperatorie nu este de obicei dificilă. Se remarcă garniturile, eritemul și edemul ciotului vaginal. Când este infectat, pacientul se plânge de dureri abdominale, pelvis, lateral, febră, secreție vaginală anormală. Liuvannya constă în numirea unuia sau a două antibiotice cu spectru larg.
Hematom vagin infectat. Acumularea de sânge în cavitatea abdominală duce la formarea unui hematom. Când un hematom se infectează, se dezvoltă un abces al ciotului vaginal, se manifestă prin durere, senzație de presiune în pelvis, pe rect, febră, durere a ciotului vaginal în timpul palpării și, eventual, secreție purulentă. Un hematom este adesea însoțit de o scădere a nivelului de hemoglobină. Examen cu ultrasunete și tomografie computerizată Confirmă diagnosticul.
Abcesul ovarian (tubo-ovarian) postoperator este însoțit de dureri abdominale sau pelvine în perioada postoperatorie târzie, după externarea din spital. Diagnosticul este confirmat prin ecografie. O creștere accentuată a durerii poate indica o rupere a abcesului, care necesită intervenție chirurgicală urgentă, evacuarea și drenarea focalizării. Aspirația chistului și rezecția ovariană nu trebuie efectuate în timpul histerectomiei vaginale, deoarece aceasta duce la contaminarea cu flora vaginală și inițierea infecției ovariene, în special la pacienții premenopauza, când foliculul este expulzat.
Tromboflebita pelvină septică se dezvoltă în 0,1-0,5% din cazuri după operații ginecologice. Diagnosticul este determinat prin excludere dacă febra NU este corectată cu antibiotice la pacienții fără abcese pelvine sau hematom infectat. Factorii de risc includ staza venoasă (obezitate, diabet zaharat), traume și contaminarea bacteriană a vaselor pelvine. Forma clasică de tromboflebite pelvice septice se dezvoltă la 2-4 zile de la intervenția abdominală și se manifestă prin febră, tahicardie, tulburări gastrointestinale, dureri abdominale pe de o parte. În 50 67% din cazuri se pot simți corzile venoase abdominale. În forma „misterioasă”, după nașterea vaginală sau chirurgia pelvină, febra apare în ciuda terapiei cu antibiotice, a tahicardiei și a trombozei difuze la nivelul venelor pelvine mici. Diagnosticul este confirmat prin tomografie computerizată sau imagistică prin rezonanță magnetică. Tratamentul constă în prescrierea heparinei timp de 7-10 zile, antibiotice eficiente împotriva bacteriilor producătoare de heparină. Tratamentul este continuat timp de 48 de ore după normalizarea temperaturii corpului.
Osteomielita pubiană poate fi o complicație rară a suspensiei uretrale pulmonare, a vulvectomiei radicale sau a exentării pelvine. Infecția se dezvoltă la 6-8 săptămâni după procedura chirurgicală. Pacienții se plâng de durere în simfiza pubiană, în special atunci când merg pe jos, febră. În sânge, se poate observa leucocitoza, o creștere a PIE. Prescrie antibiotice care acționează asupra stafilococului aureus și a florei gram-negative.
Infecția rănilor este observată în timpul procedurilor chirurgicale abdominale, în special în timpul contaminării rănilor peretelui abdominal anterior. Clasificarea plăgilor chirurgicale le împarte în curate, inteligent contaminate, contaminate și contaminate sau infectate (Secțiunea 1).
Celulita rănită este o infecție a pielii și a bazei de grăsime subcutanată a fascii. Se caracterizează prin eritem, edem, calmarea marginilor plăgii, o creștere a temperaturii locale. Agenții cauzali ai infecției sunt cel mai adesea Staphylococcus aureus, stafilococi coagulaza-negativi și streptococi. În absența descărcării purulente, este prescrisă antibioterapia cu cefalosporine sau Augmentin.
Seromul este format prin acumularea de lichid seros în rană și necesită tratament chirurgical - deschiderea, drenarea și curățarea plăgii.
Infecția rănilor profunde. În prezența secrețiilor purulente ale plăgii, rana este deschisă pentru drenarea și îndepărtarea țesutului necrotic. Dacă fascia este intactă, efectuează curățarea mecanică a plăgii, o tamponează cu tampoane de tifon cu peroxid de hidrogen și soluție fiziologică de clorură de sodiu (1: 1). Podidonă iodă nu este utilizată, deoarece nu contribuie la dezvoltarea granulațiilor. Prescrie antibiotice anti-anaerobe. Dacă infecția se răspândește în fascia, poate apărea eviscerarea, ceea ce necesită o intervenție chirurgicală urgentă (curățarea plăgii, drenarea și suturarea defectului).
Fasciita necrotizantă este o complicație gravă cauzată de o infecție bacteriană sinergică a fascii, țesutului subcutanat și pielii. Factorii de risc sunt diabetul, imunosupresia. Pacienții se plâng de durere severă în zona afectată, descărcarea tulbure cu un miros neplăcut. Tratamentul constă într-o rezecție largă a țesuturilor necrotice și utilizarea medicamentelor antibacteriene eficiente împotriva streptococilor și anaerobelor.
Infecțiile tractului urinar sunt o complicație destul de frecventă a chirurgiei ginecologice. Pacienții sunt preocupați de febră, disurie, urinare frecventă forțată, dar în multe cazuri infecțiile sunt asimptomatice. Criteriul de diagnostic pentru bacteriuria adevărată este mai mult de 100.000 de colonii de microorganisme în 1 ml de urină. Prevenirea infecțiilor tractului urinar constă în utilizarea rațională a cateterului urinar și înlăturarea rapidă a acestuia după operație sau, în cazul unei suspensii a vezicii urinare, în utilizarea auto-cateterismului. Prescrieți terapia antibacteriană cu spectru larg împotriva uropatogenelor.
Examinarea pacienților. Cauzele hipertermiei trebuie clarificate. Febra postoperatorie este observată la 39% dintre pacienți și doar la 8% este asociată cu infecția. Alte simptome ale infecției postoperatorii sunt eritemul, inducția, calmarea plăgii, prezența secrețiilor, durerea la membre, colțurile vertebrale, tuse, disurie. Efectuați analize generale și biochimice ale sângelui, urinei luate cu un cateter, teste bacteriologice ale sângelui, urinei și excretorilor rănilor. Metodele de cercetare suplimentare sunt ultrasonografia, radiografia plămânilor, tomografia computerizată și imagistica prin rezonanță magnetică.
Tratamentul infecției postoperatorii se bazează pe mai multe principii:
1) contabilizarea etiologiei polimicrobiene a acestora
2) cei mai frecventi agenți patogeni sunt microorganismele streptococi, stafilococi, gram-negativi (Escherichia, Klebsiella, enterobacterii) și anaerobe (bacteroizi, Prevotella sp, B. fragilis);
3) enterococii pot provoca sepsis
4) terapia cu antibiotice este prescrisă empiric până la obținerea unei culturi de microorganisme;
5) momentul infecției poate fi un indicator al unui grup de agenți patogeni;
6) microorganismele devin rezistente la atibiotice sunt adesea utilizate;
7) terapia cu antibiotice cu un singur medicament poate fi nu mai puțin eficientă decât mai mulți agenți.
Infecțiile postoperatorii polimicrobiene constau din 20% cocci gram-pozitivi aerobi, 20% din tije gram-negative și 60% din anaerobe. Infecțiile care se dezvoltă la 24 de ore de la operație sunt, desigur, cauzate de cocci gram-pozitivi sau, uneori, de bacili gram-negativi. Dacă infecția apare după 48 de ore, mai des este anaerobă. La un debut precoce al infecției, numirea de cefalosporine sau peniciline cu spectru extins este considerată optimă (38.2).
Antibioterapia parenterală este continuată timp de 24 până la 48 de ore după normalizarea temperaturii corpului. În absența efectului antibioterapiei timp de 72 de ore, pacienții trebuie reaplicate complet.
profilaxie Principalii factori de risc pentru infecțiile postoperatorii sunt obezitatea, vaginoza bacteriană, chirurgia radicală și pierderea excesivă de sânge (mai mult de 1 L). Pentru a reduce incidența infecției postoperatorii, tratamentul preoperator adecvat al mâinilor chirurgului și al câmpului chirurgical, al vaginului și al perineului, este importantă evitarea contactului cu pacienții infectați înainte de operație.
Pentru a reduce frecvența infecțiilor respiratorii după anestezia endotraheală, se recomandă oprirea fumatului și tratarea bolilor bronhopulmonare cronice înainte de operație, respirație profundă, tuse în perioada postoperatorie timpurie. Analgezia adecvată este importantă pentru respirația normală în perioada postoperatorie.
Prevenirea infecției tractului urinar constă în utilizarea rațională a unui cateter urinar, tratamentul preoperator al bolilor cronice.
Prevenirea infecției rănilor chirurgicale În timpul unei histerectomii, bacteriile vaginale și cervicale sunt inoculate la locul chirurgical, ceea ce crește riscul de infecție postoperatorie. Profilaxia antibioticului modern reduce incidența infecției postoperatorii de la 30-50% la 15% (38,3).
Fluorochinolonele pot fi o alternativă la cefalosporine. Pacienții cu defecte cardiace congenitale și risc de endocardită bacteriană sunt prescrise ampicilină (2 g) și gentamicip (1,5 mg / m2). Pentru alergii la peniciline, se utilizează vancomicină.
Reacțiile adverse ale profilaxiei antibiotice cu cefalosporine sunt de 1-10%; șocul anafilactic se dezvoltă la 0,02% dintre pacienți. Cele mai multe reacții adverse sunt erupții cutanate care regresează independent. Diareea ca complicație a colitei pseudomembranoase este asociată cu utilizarea prelungită | 3-lactam antibiotice în 15% din cazuri.
Astfel, principalii factori în reducerea morbidității infecțioase postoperatorii în stadiul preoperator sunt reducerea șederii preoperatorii în spital, evitarea bărbieritului părului pubian în noaptea precedentă a intervenției chirurgicale, pregătirea adecvată a intestinului, utilizarea iodului povidonei sub formă de gel sau supozitor în noaptea anterioară operației și tratamentul la timp al vaginozei bacteriene. În stadiul intraoperator, este important un tratament chirurgical atent al mâinilor chirurgilor, tehnica chirurgicală de precizie, minimizarea traumelor chirurgicale, pierderea de sânge și materialul de sutură, îndepărtarea țesutului necrotic și evitarea spațiilor „moarte” la suturarea plăgii. Sutura țesutului subcutanat nu este necesară și poate crește riscul de infecție din cauza creșterii cantității de material de sutură. În loc de drenuri gravitaționale trebuie utilizate sisteme de drenaj închise. La pacienții obezi, drenarea țesutului subcutanat scade incidența rănilor de domn și hematom.
Prevenirea infecției cu HIV și a hepatitei B devine din ce în ce mai relevantă în practica chirurgicală. Principalii agenți preventivi includ:
Utilizarea mănușilor în contact cu sângele și lichidele corporale, mucoasele, pielea rănită
Utilizarea măștilor și ochelarilor pentru procedurile chirurgicale
Utilizarea halatelor de baie și a șorțurilor de plastic
Spălarea minuțioasă a mâinilor atunci când este contaminată cu sânge sau lichide corporale
Manevrarea atentă a acelor și a altor instrumente ascuțite
Evitarea procedurilor chirurgicale la pacienții cu dermatită exudativă la vindecarea lor
Infecțiile postoperatorii pot fi cauzate de factori endogeni și exogeni.
Endogen: starea imună a pacientului, autoflora
Exogen: factori fizici și chimici ai mediului extern al spitalului, microflora secției, caracteristicile sale calitative și cantitative, regimul igienic al instalațiilor medicale.
O rană chirurgicală (ca oricare alta - arsuri industriale, gospodărești) încalcă integritatea pielii și mucoaselor, dăunează barierelor chimice care împiedică introducerea și colonizarea microorganismelor atipice și modifică caracteristicile cantitative ale microflorei normale. Dezvoltarea complicațiilor este observată mai des în grupurile de risc:
Pacienți cu diferite tipuri de imunodeficiențe, pacienți cu diabet zaharat, malnutriție etc.
Pacienții postoperatorii care au implantat substraturi din materiale sintetice sau țesuturi animale, care pot servi ca mediu pentru dezvoltarea microorganismelor. Mai mult decât atât, acestea sunt de obicei impermeabile la fagocite, anticorpi și medicamente antibacteriene.
Pacienții cu diferite tipuri de corpuri străine de reședință temporară (catetere, tuburi de scurgere, material de sutură), care inițial pot fi însămânțate cu microorganisme, servesc ca material suplimentar pentru aderența anumitor bacterii ( P. aeruginosa).
În orice caz, țesuturile de la locul intervenției sunt deteriorate, circulația sângelui este afectată, ceea ce, pe de o parte, favorizează invazia microbiană, iar pe de altă parte, reduce posibilitatea de a dezvolta reacții inflamatorii și imune adecvate.
Utilizarea antibioticelor și antisepticelor în scopuri profilactice, în același timp, suprimând microflora opțională, facilitează colonizarea bacteriilor patogene și multirezistente.
Infecții cu răni
Rănile curate: răni care nu penetrează la nivelul toracelui și abdomenului, aplicate în condiții aseptice sau fără semne de inflamație. Aceasta include răni cu gastroectomie, colecietectomie, apendectomie (în absența inflamației primare). Frecvența infecției este de 5-7%.
Rănile contaminate condiționat. Leziunile care implică peretele muscular al organelor goale fără o contaminare semnificativă cu microflora opțională: incizii în timpul intervenției pe căile respiratorii și tractul gastro-intestinal, cu o alunecare minimă de bacterii care contaminează țesuturile sterile, frecvența infecției nu depășește 11%.
Rănile infectate - leziuni cu inflamații acute, contaminare semnificativă de către microorganisme, în principal din organele musculare goale, dar fără secreție purulentă. Leziuni extinse în condiții aseptice sunt, de asemenea, menționate la astfel de răni contaminate. Frecvența infecției este de 15,2-21,9%.
Rănile purulente - caracterizate prin descărcare purulentă profuză. Acestea includ, de asemenea, răni care apar în timpul perforației organului, în prezența unor focare de inflamație cronică (de exemplu, manifestarea plagilor sub presiune). Frecvența infecției este de 22-40%.
Semănarea cu microorganisme nu duce întotdeauna la dezvoltarea infecției, de aceea ar trebui considerată un factor de risc. Prezența descărcării purulente indică dezvoltarea infecției.
LA. rănile detașabile înainte de semne de complicație purulentă pot fi cercetate în scop prognostic: prezența agentului patogen, tipul acestuia, caracteristica tulpinii, inclusiv sensibilitate la antibiotice. Studiul descărcării purulente are ca scop stabilirea etiologiei infecției dezvoltate.
Patogeni ai proceselor purulent-inflamatorii: Stafilococ spp., streptococ sp, Pseudomonas spp, Esherichia, Proteu, Citrobacter, Klebsiella, Enterobacter, Acinetobacter, Haemophilus, Candida, Actinomyces
Selecția, cercetarea și evaluarea NTD: Ordinul Ministerului Sănătății din URSS nr. 535 din 22.04.85, „La unificarea metodelor de cercetare microbiologice (bacteriologice) utilizate în laboratoarele de diagnostic clinic ale instituțiilor medicale”.
Departamentul de Boli Chirurgicale, Universitatea Medicală-Dentară de Stat din Moscova
URL-
Fără îndoială, o definiție clară a unui concept exclude interpretarea sa ambiguă. Acest lucru este valabil și în ceea ce privește definirea unui astfel de fenomen ca „infecții nosocomiale” (infecții nosocomiale). Cea mai reușită și destul de completă trebuie considerată definiția infecțiilor nosocomiale propuse de Oficiul Regional OMS pentru Europa în 1979: infecția nosocomială (spital, spital, spital, nosocomial) - orice boală infecțioasă recunoscută din punct de vedere clinic, care afectează pacientul ca urmare a internării sale în spital sau tratament a ei pentru ajutor medical sau o boală infecțioasă a unui angajat din spital, ca urmare a activității sale în această instituție, indiferent de apariția simptomelor bolii înainte sau în timpul șederii sale în spital.
În mod natural, cea mai semnificativă parte a infecțiilor nosocomiale este infecția pacienților din spitale. Frecvența infecțiilor nosocomiale este de cel puțin 5%. Rapoartele oficiale reflectă doar o mică parte a infecțiilor nosocomiale chirurgicale și, conform datelor citate de cercetători străini, infecțiile chirurgicale reprezintă 16,3-22%
.
Istoria a păstrat afirmațiile și observațiile medicilor celebri despre semnificația problemei infecției nosocomiale. Printre acestea se numără cuvintele lui N.I. Pirogov: „Dacă mă uit înapoi la cimitirul în care sunt îngropați cei infectați în spitale, nu știu la ce să mă surprindă mai mult: dacă există stoicismul chirurgilor sau încrederea pe care o au spitalele cu guvernul și cu societatea. până când medicii și guvernele pornesc pe o nouă cale și vor depune eforturi comune pentru a distruge sursele miasmei din spital "*.
Sau observația lui I. Semmelweis, care a stabilit o legătură între incidența ridicată a „febrei materne” în secțiile obstetrice ale Spitalului din Viena din a doua jumătate a secolului al XIX-lea și nerespectarea medicilor cu regulile de igienă, a devenit clasică.
Astfel de exemple în sensul complet al cuvântului, infecția nosocomială poate fi găsită ulterior. În 1959, am descris focarele de mastită purulentă postpartum la femeile care au născut în maternitatea unuia dintre cele mai mari spitale din Moscova. Majoritatea pacienților au fost tratați și apoi tratați în secția chirurgicală a clinicii din același spital. În toate cazurile, agentul cauzal a fost stafilococul alb, izolat de abcese mamare. Este caracteristic faptul că un stafilococ similar a fost izolat în timpul studiilor bacteriologice sistematice efectuate în maternitate. După măsurile sanitare planificate la secție, numărul pacienților cu mastită a scăzut, iar pe măsură ce contaminarea bacteriană a spațiilor maternității a crescut din nou.
Tabelul 1. Natura florei microbiene izolată de focarele de infecție la pacienții chirurgicali
| microorganismele |
Frecvența de selecție,% |
|
|
1994-1997 |
1998-1999 |
|
| Candida spp. | ||
| Citrobacter spp. | ||
| Enterobacter spp. |
13,2 |
|
| Enterococcus spp. |
12,3 |
|
| Escherichia coli |
28,3 |
23,0 |
| Klebsiella spp. |
12,1 |
|
| Proteus spp. | ||
| Pseudomonas spp. |
10,0 |
|
| Staphylococcus spp. |
12,3 |
10,0 |
| Streptococcus spp. |
12,1 |
|
| anaerobi | ||
| Notă. * - nicio informație de încredere. | ||
Tabelul 2. Flora bacteriană se excretă cel mai frecvent din cavitatea abdominală, vezica biliară și rănile postoperatorii.
|
microorganismele |
abdominal cavitate |
Bilă |
Rănile postoperatorii |
| Enterobacter spp. | |||
| Enterococcus spp. | |||
| Escherichia coli | |||
| Klebsiella spp. | |||
| Proteus spp. | |||
| Pseudomonas spp. | |||
| Staphylococcus spp. | |||
| Streptococcus spp. |
În prezent, nu există nicio îndoială că încălcarea regimului sanitar-igienic în instituțiile medicale duce la o creștere a incidenței și a focarelor de infecții nosocomiale. Acest lucru este cel mai frecvent pentru infecțiile respiratorii și intestinale.
Cu toate acestea, există o categorie specială de infecții nosocomiale care atrage atenția diverșilor specialiști, în primul rând chirurgi, și nu are o soluție lipsită de ambiguitate. Vorbim despre complicații postoperatorii în secțiile chirurgicale din spitale cu diferite profiluri și capacități ale paturilor, a căror gravitate specifică este destul de mare.
Unii autori cred că complicațiile postoperatorii variază între 0,29 și 30%, dar majoritatea furnizează date mai uniforme - 2-10%. Cel mai adesea vorbim despre supurația unei rani postoperatorii, însă, după operațiile efectuate în legătură cu bolile acute însoțite de peritonită difuză, se dezvoltă destul de des abcese ale cavității abdominale (1,8-7,6%).
Conform lui N. N. Filatov și colab. , frecvența complicațiilor purulente-septice la pacienții operați în spitale cu profil chirurgical din Moscova este de 7,1%. O frecvență mai mare a infecțiilor cu rani chirurgicale (de la 11,5% la 27,8%) este dată de M.G. Averyanov și V.T. Sokolovsky, iar monitorizarea acestora a relevat un nivel ridicat de complicații purulente (9,7% -9,8%) ) cu clase I-II de răni chirurgicale, în care practic nu ar trebui să existe complicații și cu o opțiune acceptabilă - nu mai mult de 1%. Pentru mai mult de 53 de mii de operații, frecvența complicațiilor postoperatorii purulente-septice este de numai 1,51%.
Incoerența datelor nu reduce semnificația problemei complicațiilor postoperatorii ale plăgii, a căror dezvoltare agravează în mod semnificativ dezvoltarea bolii de bază, prelungește șederea în spital a pacientului, crește costul tratamentului, cauzează adesea decese și afectează negativ timpul de recuperare al pacienților operați.
Se știe că toate operațiile trebuie mai întâi divizate în funcție de gradul de posibilă infecție. Riscul de complicații infecțioase postoperatorii crește pe măsură ce factorii care afectează infecția în timpul operației cresc.
Ar trebui să țină seama de diferența de frecvență a complicațiilor după operații de urgență și planificate, influența vârstei pacientului, gradul de pierdere de sânge, durata operației, timpul petrecut de pacienți în spital înainte de operație și mulți alți factori care afectează frecvența infecției rănilor chirurgicale și a altor complicații septice.
Printre acești factori, formele neglijate ale bolilor acute au o importanță deosebită atunci când operația este efectuată la o dată ulterioară din diferite motive. Acest lucru este ilustrat de apendicita gangrenată și perforată, în care frecvența complicațiilor purulente ajunge la 50% sau mai mult.
Este interesant de menționat că, în funcție de multe date, frecvența de supurație a rănilor chirurgicale depinde de ora de operație. Cel mai adesea, complicațiile apar atunci când se efectuează operațiuni noaptea, iar acest lucru se aplică și operațiunilor de curățare.
În această lucrare, nu am stabilit sarcina de a studia întreaga varietate de factori care afectează frecvența și natura complicațiilor postoperatorii, ci am dorit să urmărim relația lor cu infecțiile nosocomiale, deși în conformitate cu definiția OMS dată mai devreme, toate complicațiile postoperatorii ar trebui să fie atribuite infecțiilor nosocomiale.
Cu toate acestea, pentru a înțelege esența diferențelor atât în \u200b\u200bmanifestările infecțiilor nosocomiale, cât și în recomandările fundamentate pentru prevenirea lor, în opinia noastră, este necesar să luăm în considerare nu doar câteva aspecte bacteriologice ale manifestărilor infecțiilor nosocomiale, ci și natura agenților patogeni ai infecțiilor care au determinat boala de bază care necesită intervenție chirurgicală .
Dacă multe manifestări ale infecțiilor nosocomiale sunt asociate cu natura tulpinilor spitalicești care circulă în interior o instituție medicală specială, dezvoltarea complicațiilor postoperatorii depinde adesea de natura agentului cauzal al bolii care stă la baza, care a servit ca motiv al spitalizării și a fost un indiciu pentru o intervenție chirurgicală.
Natura florei microbiene izolată de focarele de infecție ale pacienților pe care le-am operat cu boli acute sau leziuni ale organelor cavității abdominale, în ciuda întregii imperfecțiuni a laboratoarelor bacteriologice din spital și a erorilor posibile în colectarea materialului, relevă o anumită imagine (tabelul 1) cu predominanțăEscherichia coli, Enterobacter spp., Klebsiella, diverse tipuri de stafilococi și streptococi. În ultimii ani, nu s-au produs modificări notabile în natura florei microbiene.
În ultimii 3 ani, în culturile luate în cursul dezvoltării complicațiilor postoperatorii din răni purulente, abcese intraabdominale și alte focare, care pot fi considerate manifestări ale infecțiilor nosocomiale, se distinge o floră microbiană apropiată de aceasta (tabelul 2).
În același timp, natura florei microbiene a spitalului este destul de diversă, care depinde de multe caracteristici ale spitalelor chirurgicale. Diferiți autori notează un nivel ridicatP.aeruginosa (18,1%) și E coli (26,9%), acordați atenție prevalenței enterobacteriilor (42,2%) și Staphylococcus aureus (18,1%); stafilococul a fost izolat în 36,6% din cazuri,E coli - la ora 13.6, P.aeruginosa - în 5,1%.
S-au remarcat diferențe în natura florei microbiene izolate în departamentul de infecție a rănilor și ranilor, unde 55% au fost gram pozitive și 38% au fost microorganisme gram-negative și stafilococi (44%), Pseudomonas aeruginosa (21%) și reprezentanți ai familiei Enterobacteriaceae (10%). secții în care pacienții au suferit operații legate de condițiile curate și contaminate condiționat, unde proporția de stafilococi a fost mai mică (33%), iar reprezentanții grupului intestinal au fost la nivelul de 18%, iar P.aeruginosa a fost de doar 6%.
Tulpinile de spital selectate sunt caracterizate prin rezistență mare la antibiotice; rezistența la cele mai utilizate antibiotice poate atinge 70-90%. S-a remarcat o rezistență ridicată la peniciline și o sensibilitate bună la fluorochinolone.
Conform datelor noastre, Staphylococcus aureus (41,5%), stafilococ epidermic (22%), E. coli (22,1%) au fost cel mai adesea izolați de răni în secția de chirurgie purulentă; în secțiile de chirurgie abdominală, unde se efectuează cu precădere operații de urgență, microbii intestinali (49,6%) au predominat în culturi din răni postoperatorii supurative, iar proporția de stafilococ a fost de 26,5%.
Dacă comparăm aceste date cu informațiile de mai sus despre natura florei microbiene secretate din focarele de infecție în timpul primei operații la pacienții internați în secția de chirurgie abdominală, unde predomina flora microbiană a grupului intestinal (E.coli, Enterobacter spp., Klebsiella spp.), iar stafilococii alcătuiau nu mai mult de 15%, devine evident că flora microbiană a rănilor postoperatorii purulente este mult mai apropiată în compoziția speciilor lor de flora microbiană izolată de focuri în timpul primei operații (a se vedea tabelul 2).
Această comparație ne permite să luăm în considerare cauza dominantă a complicațiilor purulente postoperatorii nu numai tulpinilor spitalicești, ci flora microbiană, care se afla deja în corpul pacientului înainte de internare. Această circumstanță nu are nici o importanță mică și, eventual, decisivă în interpretarea cauzelor complicațiilor postoperatorii ale plăgii, care, prin definiție, se referă la manifestările infecțiilor nosocomiale și sunt în esență o continuare a acelei boli purulent-inflamatorii (apendicită acută, colecistită acută, peritonită etc.), s prin care pacientul a fost internat în spital sau o reflectare a florei microbiene endogene a pacientului, care a arătat proprietățile sale agresive din cauza slăbirii factorilor de protecție anti-infecție din cauza bolii de bază, a traumelor chirurgicale sau a pierderii de sânge.
Cu toate acestea, nu poate fi refuzată importanța tulpinilor spitalicești în dezvoltarea complicațiilor postoperatorii ale plăgii, care, în special, este confirmată de date despre dependența predominantă a structurii agenților cauzali ai infecției rănii după un tratament chirurgical simultan și complet asupra naturii infecției nosocomiale.
Evaluând factorii care afectează frecvența complicațiilor plăgii postoperatorii, nu se poate lua în considerare importanța reactivității imune afectate.
Rolul statutului imunitar în dezvoltarea complicațiilor postoperatorii este deosebit de pronunțat în incidența ridicată a complicațiilor infecțioase nosocomiale la pacienții cu un rinichi transplantat, care se datorează în primul rând imunosupresiei. Studiile de lungă durată ale angajaților noștri cu privire la rolul imunodeficienței în dezvoltarea complicațiilor postoperatorii au făcut posibilă determinarea valorii prioritare nu numai a unui cerc destul de restrâns de indicatori studiați ai statutului imunitar, ci să ofere o înțelegere mai largă a protecției anti-infecție sub forma unui sistem de adaptare care include o gamă largă de indicatori ai sistemului nervos imun, endocrin și autonom și a acestora afectează reciproc relațiile.
Există un punct de vedere că antibioticele afectează negativ starea funcțională a sistemului imunitar. O încercare de a utiliza antibiotice pentru prevenirea complicațiilor postoperatorii duce adesea la imunosupresie și la progresia procesului infecțios. Această afirmație destul de categorică nu are dovezi convingătoare, cu toate acestea, putem fi de acord că utilizarea incorectă a antibioticelor poate fi însoțită într-adevăr de manifestări ale infecției rănilor în perioada postoperatorie.
Discutând problemele complicațiilor infecțioase nosocomiale, în primul rând, aceștia acordă atenție importanței tulpinilor spitalicești de infecție microbiană.
Controlul sanitar și bacteriologic este cel mai accesibil și indicativ test, caracterizând nivelul de contaminare microbiană a instituțiilor medicale și predominanța anumitor tulpini spitalicești.
În majoritatea datelor publicate, numărul rezultatelor nesatisfăcătoare ale controlului bacteriologic este mic și se ridică la 0,5-2%.
Starea mediului nosocomial, desigur, determină probabilitatea unei infecții spitalicești, dar joacă un rol predominant în raport cu infecțiile intestinale și respiratorii sau în dezvoltarea infecțiilor purulente ale nou-născuților și puerperasului. În ceea ce privește complicațiile postoperatorii ale plăgii, atunci legătura lor cu starea mediului nosocomial este mai puțin pronunțată.
Acest lucru este convins de o analiză retrospectivă a contaminării bacteriene dezvăluite în timpul studiilor bacteriologice sistematice efectuate în instituțiile medicale pe baza ordinului Ministerului Sănătății din Federația Rusă nr. 720. Am utilizat datele obținute în ultimii 6 ani (1994-1999) la unitățile clinice ale secției din două mari spitale din Moscova, în care numărul de paturi chirurgicale este de 210 și 180, iar compoziția pacienților este destul de omogenă. În același timp, într-unul dintre spitale, 180 de paturi includ un departament de chirurgie purulenta-septica.
Din 22.971 de studii bacteriologice, inclusiv cele din spălări din obiecte înconjurătoare, s-a observat creșterea florei microbiene în 502 de culturi. În 1996, contaminarea bacteriană a crescut de la 1 la 3,7%, dar în 1997 a scăzut la 1,6%. În secțiile chirurgicale, rata de însămânțare a florei microbiene a fost de 2,5%.
Cea mai mică contaminare bacteriană rămâne în secțiile de operare (0,8%) și cea mai mare în secțiile de terapie intensivă (3,6%). Stafilococul epidermic domină în culturi (84,6% în spital și doar 2,3% în secțiile chirurgicale). Staphylococcus aureus și Escherichia coli reprezintă 13,9% și 6,7% în secțiile chirurgicale, 3,1% - în unitatea de operare și 28,4% - în unitățile de terapie intensivă.
Atunci când comparăm aceste date cu rezultatele examinării bacteriologice a rănilor postoperatorii purulente în secțiile chirurgicale „curate” (peste 100 de culturi), stafilococul epidermic reprezintă 26,5%. Cel mai adesea în culturile din răni postoperatorii au fost izolateE coli - 49,6%. În secția chirurgie purulentă-septică, stafilococul epidermic reprezintă 22,0%, Staphylococcus aureus - 41,5%,E coli - 22,1%.
Cu diferențe regulate în natura florei microbiene izolate de rănile postoperatorii în secțiile chirurgicale „curate” și purulente, această flora microbiană este mai consistentă cu agenții cauzali dominanți ai bolii de bază prima operatie (E coli și Enterobacter spp. - 51%, stafilococi - 12,6%).
Variabilitatea agenților cauzali ai infecției postoperatorii în spitale chirurgicale a fost remarcată într-o serie de lucrări, cu toate acestea, evaluarea acesteia necesită clarificări și prudență. De exemplu, se remarcă faptul că în același compartiment chirurgical a existat o modificare a infecției rănilor după operațiile pe organele abdominale, manifestată printr-o scădere a rolului Staphylococcus aureus de la 66,8% în 1973 la 19,1-25% în 1992-1997 . și absența completă a acestuia în exudatele rănilor la pacienți în 1998-1999. . Frecvența enterobacteriilor a crescut constant, a atins un maxim (88,7%) în 1987 și a fost apropiată de aceste valori la începutul anilor 90. În 1996-1999 proporția de enterobacterii din etiologia infecției plăgii postoperatorii a scăzut la 58,3%. În anii 90 a fost remarcată o creștere a rolului stafilococilor și pseudomonadelor coagulază negative.
Cu toate acestea, nu este indicat dacă natura agenților patogeni s-a schimbat în timpul însămânțării cavității lor abdominale în timpul primei operații.
La evaluarea mecanismelor infecțiilor nosocomiale, nu se poate ignora posibila transportare bacteriană a personalului medical. Când am examinat 555 de angajați din spital (recoltele au fost prelevate din tractul respirator superior), Staphylococcus aureus a fost izolat în 22 (3,9%), în timp ce stafilococul aureus era de 1,6% în personalul medical al secțiilor chirurgicale, al unității de operare și al secțiilor de reanimare.
Informațiile prezentate sugerează că, evaluând rolul infecțiilor nosocomiale în dezvoltarea complicațiilor plagii purulente postoperatorii, starea mediului nosocomial nu ar trebui acordată o importanță primară.
Printre motivele care determină creșterea infecțiilor nosocomiale se numește în mod tradițional formarea de tulpini în spital a unui număr mare de microorganisme caracterizate prin rezistență multiplă la medicamente, rezistență ridicată la factorii de mediu adversi. Este indicat pe bună dreptate că tulpinile nosocomiale s-au format în Staphylococcus aureus auriu și epidermic, Pseudomonas aeruginosa, Proteus, Enterobacter, o serie de sermonare Salmonella etc.
Cu toate acestea, evaluând rolul acestor tulpini nosocomiale în dezvoltarea infecțiilor nosocomiale, trebuie să se țină cont și de evoluția procesului epidemic al infecțiilor purulente-septice din spital în chirurgie. Acest lucru este demonstrat de o revizuire de peste 20 de ani, în care, atunci când studiem rezultatele 38.750 de operații, au fost observate 3120 (8%) cazuri de complicații purulente-septice, iar reducerea acestor complicații a fost de 3-6 ori; precum și o schimbare periodică a agentului patogen, în special, trecerea de la S.aureus la P.aeruginosa, apoi la stafilococi coagulaz-negativi, apoi infecții enterococice, care se datorează tehnologiilor medicale aplicate și particularităților procesului de diagnostic. Reducerea formelor generalizate și predominarea infecțiilor exogene în ultimul trimestru al perioadei observate și o reducere semnificativă a complicațiilor cauzate de tulpinile spitalicești
. Acesta este un punct foarte important, în special în ceea ce privește complicațiile plăgii postoperatorii.
O diferență vizibilă în frecvența complicațiilor purulente după operațiile planificate și de urgență, remarcată în multe studii, confirmă semnificația așa-numitei infecții stradale sau rolul infecției endogene în comparație cu tulpinile spitalicești.
Nu toate complicațiile infecțioase care apar
după operație, acestea sunt asociate cu tulpini de microorganisme spitalicești și, deși aceste complicații, prin definiție, se referă la infecții nosocomiale, sunt de origine diferită, iar evaluarea lor și, prin urmare, măsurile de prevenire, ar trebui tratate în mod diferit.
Cele mai multe dintre aceste complicații postoperatorii sunt o continuare sau o consecință a bolii sau leziunilor care stau la baza lor, care au servit drept indicație pentru o operație chirurgicală, care în unele cazuri a contribuit la manifestarea unei infecții endogene a pacientului însuși, care a fost anterior într-o stare inactivă. Aceasta ar trebui să includă și translocarea infecției care a cauzat sepsis.
Statisticile oficiale privind infecțiile nosocomiale și sepsis nu iau în considerare toate caracteristicile complicațiilor septice postoperatorii și nici specialiștii din centrele de supraveghere sanitară și epidemiologică de stat nu iau în considerare originea lor, ceea ce, împreună cu caracterul adesea represiv al investigațiilor efectuate de epidemiologi, conduce la ascunderea multor cazuri de purulent-septic complicații și denaturarea statisticilor.
Acest lucru este demonstrat de experiența mai multor instituții medicale și de o comparație a florei microbiene izolate de focarele principale în timpul operației primare și a focarelor de complicații postoperatorii.
În plus, trebuie luată în considerare importanța infecției intraoperatorii, care crește odată cu durata operației, care este dovedit prin exemplul operațiilor în coloproctologie și arată corelația complicațiilor postoperatorii cu infecția intraoperatorie.
Nu este întâmplător faptul că se subliniază că majoritatea cazurilor de infecție a plăgilor chirurgicale în chirurgia abdominală sunt rezultatul unei infecții endogene (80-85%), deși decizia cu privire la originea endogenă sau exogenă a infecției este destul de dificilă.
Un risc suficient de ridicat de a dezvolta infecții postoperatorii se datorează multor circumstanțe, printre care - prezența unei plăgi chirurgicale cu țesuturi deteriorate; un număr semnificativ de pacienți spitalizați cu diverse boli purulent-inflamatorii în care riscul de infecție a rănii este foarte mare; efectuarea unei părți semnificative a operațiunilor de urgență; scăderea rezistenței la infecție din cauza bolilor de bază și concomitente (diabet zaharat, obezitate); factori operaționali defavorabili (prelucrarea inadecvată a câmpului chirurgical, tehnica nesatisfăcătoare a chirurgului operator, durata operației, calitatea materialului de sutură) etc.
Chiar și tipul de pansament care acoperă rana afectează frecvența supurației, care este aproape dublă atunci când utilizați pansamente lipicioase din plastic.
Pacienții cu cancer sunt localizați în special pentru dezvoltarea complicațiilor purulente-septice.
În multe privințe, frecvența complicațiilor postoperatorii este determinată de clasificarea operațiunilor în funcție de gradul de contaminare posibil în cele curate, condiționate curate, contaminate și murdare (infectate). Acest lucru este confirmat de cifrele care caracterizează probabilitatea infecției plăgii chirurgicale pentru intervențiile chirurgicale curate - 1-5%, pentru cele curate condiționate - 3-11%, contaminate - 10-17% și murdare - mai mult de 27%.
Sistemul de măsuri pentru prevenirea complicațiilor plăgii postoperatorii este bine cunoscut, se bazează pe eliminarea factorilor de risc enumerați pentru dezvoltarea complicațiilor chirurgicale ale plăgii.
Printre aceste măsuri, o profilaxie antibacteriană rațională semnificativă ocupă un loc semnificativ, deși utilizarea antibioticelor pentru prevenirea complicațiilor postoperatorii este într-o oarecare măsură discreditată de utilizarea lor incorectă.
În primul rând, antibioticele nu trebuie utilizate la efectuarea intervențiilor chirurgicale curate, cu excepția celor foarte lungi, însoțite de pierderi semnificative de sânge ale intervențiilor chirurgicale cardiovasculare, în special cu utilizarea de bypass cardiopulmonar și chirurgii osteoplastice cu implantarea protezelor.
A doua circumstanță foarte importantă privește momentul și modul de administrare a medicamentelor antibacteriene. Concentrația maximă de antibiotice în țesuturi este realizată numai cu administrare intraoperatorie, de preferință cu cel puțin 30 de minute înainte de începerea operației. Așa-numitele operații murdare necesită terapie cu antibiotice.
Atunci când alegeți un medicament antibacterian în scopul prevenirii, trebuie să procedați în principal din cerința de a furniza antimicrobiene necesare spectru în raport cu cei mai frecventi agenți patogeni ai infecției chirurgicale, despre care s-a discutat la începutul articolului. Aceste medicamente ar trebui să aibă capacitatea de a pătrunde treptat în țesuturile cu cel mai mare risc de infecție în timpul intervenției chirurgicale, precum și de o toxicitate minimă și nu ar afecta proprietățile farmacocinetice ale medicamentelor utilizate pentru anestezie. De mare importanță este timpul de înjumătățire, care ar trebui să asigure o concentrație bactericidă suficientă pe întreaga operație.
Cefalosporinele din generația II-III (cefuroxim, cefazolin, cefamandol, cefoperazone, ceftriaxona) îndeplinesc cel mai bine aceste cerințe de bază. Dacă este necesar, pot fi combinate cu metronidazol.
Utilizarea medicamentelor de a treia generație, care sunt de obicei utilizate pentru tratament, este justificată de caracteristicile lor specifice. Așadar, utilizarea cefoperazonei este recomandată pentru operații pe tractul biliar în colecistită acută, colangită, deoarece are cea mai mare capacitate de a pătrunde în vezica biliară și peretele vezicii biliare.
Utilizarea ceftriaxonei este indicată dacă este necesar un efect pe termen lung, deoarece are cea mai lungă perioadă de înjumătățire în comparație cu alte cefalosporine.
S-a dovedit ca un medicament pentru profilaxia intraoperatorie a amoxicilinei / acidului clavulanic, în special în timpul operațiilor pe colon și rect.
Principiile utilizării antibioticelor pentru prevenirea complicațiilor postoperatorii sunt prezentate în detaliu în lucrări cunoscute. Mulți ani de experiență confirmă eficacitatea unei astfel de prevenții, ceea ce ne permite să reducem numărul de complicații purulente la diferite grupuri de pacienți de 1,5-2 ori.
Literatură:
1. Dmitrieva N.V., Petukhova I.N., Smolyansky A.Z. Structura etiologică și sensibilitatea la antibiotice a principalilor agenți cauzali ai complicațiilor infecțioase într-o clinică oncologică // M., 1999; 65.
2. Pokrovsky V.I. Prefață la Ghidul pentru prevenirea infecțiilor nosocomiale. M., 1993; 3.
3. Semina N.A., Kovaleva E.T., Genchikov
LA. Epidemiologie și prevenirea infecțiilor nosocomiale // Nou în prevenirea infecțiilor spitalicești. - Informa. Taur. M., 1997; 3-9.
4. Briskin B.S. Efectul secundar al antibioticelor într-o clinică chirurgicală // Rezumat. insulta. ... cand. Miere. științe. M.,
1
959; 21.
5. Dontsov V.I., Popova T.A., Bashkova N.M., Yurovskaya A.I. Infecții nosocomiale în orașul Ekaterinburg în anii 90. Secolul XX // Teză. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 87-8.
6. Wellinger R.C., Mc Langhlin S. Uniq
epidemiologia infecțiilor nosocomiale în spitalul copiilor // Amer J Dis Child. 1984; 138: 131-5.
7. Wenzel R.P. Supravegherea și raportarea infecțiilor cu domiciliu spital // Manualul infecțiilor spitalizate - Boca Raton, F.L. Cre Press. 1981; 44.
8. Zhebrovsky V.V., Menshikova G.T., Medischev V.G. Complicații precoce ale plăgii chirurgicale după apendicectomie pentru forme distructive de apendicită // Fiziologia și patologia sistemului digestiv. Simferopol, 1978; 50-94.
9. Zhebrovsky V.V., Toskin K.D. Problema complicațiilor postoperatorii în chirurgia abdominală // Complicații și pericole postoperatorii în chirurgia abdominală. M .: Medicină, 1990; 5-181.
10. Kuzin M.I., Kostyuchenok T.M. Rănile și infecția rănilor. M .: Medicină, 1981; 678
11. Kuzin M.I., Kostyuchenok T.M., Kuleshova S.Ya. Infecție anaerobă non-clostridială în chirurgie purulentă // Infecții și răni. - Eu sunt All-Union. conf. - Acestea. doc. M., 1986; 201-2.
12. Oleinik S.V., Baulin N.A. Cu privire la analiza epidemiologică a patologiei purulente postoperatorii în spitale chirurgicale // Zh. microbiol., epidemiol. și imunol. 1992; 4: 26-8.
13. Savchuk T.D. Peritonita purulentă. M .: Medicină, 1979; 188 p.
14. Brachman P.S., Dan B.B., Haley R.W. și colab. Infecții chirurgicale nosocomiale
o
ns: Incidență și cost // Surg clin North Am. 1980; 60: 1.
15. Stone H.H., Haney B. B., Koeb H. D. Antibioterapie profilactică și preventivă. Timing, durată și economie // Ann Surg. 1979; 189: 691-9.
16. Bezruk I.A. Infecția nosocomială a unui spital chirurgical (premise imunologice și imunoprofilaxie: probleme de diagnostic, clinică, tratament și prevenire) // Rezumat. insulta. ... cand. Miere. științe. Alma-Ata, 1991; 23 sec
17. Milonov O.T., Toskin K.D., Zhebrovsky V.V. Complicații și pericole postoperatorii în chirurgia abdominală. M .: Medicină, 1990; 560.
18. Toskin KD, Zhebrovsky VV, Bereznitsky F.G. Abcese postperoperatorii intraperitoneale și extraperitoneale // Complicații și pericole postoperatorii în chirurgia abdominală. M .: Medicină, 1990; 84-133.
19. Filatov N.N., Khrapunova I.A., Matveev S.I. Problema infecțiilor purulente-septice în spitale cu profil chirurgical // Teze. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 254-5.
20. Averyanov M
.
G., Sokolovsky V.T. Supravegherea epidemiologică a infecțiilor nosocomiale în spitale chirurgicale folosind un program de monitorizare epidemiologic bazat pe computer // Proc. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 6
-
7.
21. Marshall K. Infecții chirurgicale și complicații infecțioase după arsuri // Infecții nosocomiale / Ed. R. P. Vencil. M .: Medicină, 1990; 259-338.
22. Smolovsky V.T. Studierea prevalenței bolilor purulente-septice din spital în instituțiile de îngrijire a sănătății urbane și rurale din diferite regiuni ale țării // Spitalul. infecții și medicamente. rezistența microorganismelor. - Sat științific proceduri, M., 1992; 7-10.
23. Cruse P.I.E., Foord R. Epidemiologia infecției rănilor:
un studiu prospectiv de zece ani de 62939 de răni // Surg clin North Am. 1980; 60: 27-40.
24. Ghukasyan G.T., Sargsyan A.S., Kuzikyan A.M., Aleksanyan Yu.T. Natura microflorei în infecțiile nosocomiale într-un spital multidisciplinar // Proc. doc. eu
eu
Rusă științific și practic. conf. cu int. participare. M., 1999; 79-80.
25. Vilenskaya I.F., Sheprinsky P.E., Osipova A.N. și alte caracteristici ale complicațiilor postoperatorii într-un spital chirurgical // Teză. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 51-2.
26. Kulaevskaya V.G. Eșecul suturilor anastomozelor esofagiene-gastrice și esofagiene-intestinale // Rezumat. insulta. ... cand. Miere. științe. M., 1980; 20 sec
27. Moroz V.Yu., Terekhova R.P., Galkin V.V. et al. Infecția spitalului într-o clinică chirurgicală // Intra-spital. infecția este o problemă epidemică. - Acestea. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 161-2.
28. Vitkova O.A., Shatashvili A.G. Controlul epidemiologic al infecțiilor nosocomiale // Teze. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 54-5.
29. Galkin R.A., Pavlov V.V., Bykov A.A. et al. Monitorizarea microbiologică în supravegherea epidemiologică a infecțiilor nosocomiale // Proc. doc. II rus științific și practic. conf. cu int
.
participare. M., 1999; 62-3.
30. Ivanov G.A., Lebedev V.F., Sidelnikova O.P., Suborova T.N. Frecvența alocării agenților patogeni ai complicațiilor infecțioase din răni de diverse origini // Probleme reale ale infecției în chirurgie. M., 1999; 155-7.
31. Volynchik EP, Belorusov OS, Sorokina V.I. et al. Problema infecției nosocomiale la pacienții cu un rinichi transplantat // Proc. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 58-9.
32. Briskin B.S., Savchenko Z.I., Khachatryan N.N. Mecanisme adaptative de protecție pentru peritonită și posibilitatea corectării farmacologice a afecțiunilor acestora // Mat. Eu Mosk. Int. Congr. chirurgi. M., 1995; 80-1.
33. Evstifeeva O.V. Reglarea glucocorticoidă a imunității și rolul acesteia în tratamentul peritonitei // Rezumat. insulta. ... cand. Miere. științe. M., 1996; 25.
34. Khachatryan N.N. Formarea mecanismelor de protecție și adaptare și corectarea lor în peritonită // Rezumat. ... insulta. DOCT. Miere. științe. M., 1995; 25.
35. Grinsand Yu.M., Melnikova V.I., Vasilenko A.Yu. Imunomodularea prin factori fizici în prevenirea infecțiilor postoperatorii // Proc. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 75-6.
36. Aidinov G.T., Schwager M.M., Mitrofanova T.V. et al. Monitorizare microbiologică în spitale cu profil chirurgical și maternități din Regiunea Rostov // Proc. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 8-9.
37. Akhmedova R.R., Martova O.V., Burkin V.S. et al. Monitorizarea microbiologică a obiectelor de mediu în asigurarea supravegherii epidemiologice a infecțiilor nosocomiale // Proc. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 28-9.
38. Gudkova E.I., Adarchenko A.A., Sobeshchuk O.P. et al. Dinamica structurii etiologice a infecției rănilor spitalicești în spitalele cu arsuri chirurgicale din Republica Belarus // Teză. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 78-9.
39. Prevenirea infecțiilor nosocomiale. Un ghid pentru medici. M., 1993; 220.
40. Brusina E.G. Evoluția procesului epidemic de infecții purulente-septice din spital în chirurgie. Revizuire timp de 20 de ani // Teză. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 47-8.
41. Vladimirov N.I., Oparin P.S. Infecții purulente-septice într-un spital cu profil chirurgical // Teze. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 55-6.
42. Gladkova L.S., Turnikov Yu.I., Skorobulatov A.V. Problema înregistrării sepsisului nosocomial // Teză. doc. II rus științific și practic. conf. cu int. participare. M
.
, 1999; 65-6.
43. Korneva TK, Shelygin Yu.A., Konovich E.A., Nezhikova S.V., Lyagina I.A. Etiologia infecțiilor nosocomiale într-o clinică de proctologie // Rezumat. doc. II rus științific și practic. conf. cu int. participare. M., 1999; 122-3.
44. Cartea de referință a epidemiologului spitalului. M., 1999; 335.
45. Gubina G.N. Complicații nosocomiale purulent-inflamatorii după intervenția chirurgicală radicală pentru cancerul gastric // Rezumat. insulta. ... cand. Miere. științe. M., 1979; 20 sec
46. \u200b\u200bKnysh V.I., Ananyev V.S. Complicații postoperatorii la pacienții cu cancer de colon // Vopr. oncologie. 1985; 5: 42-7.
47. Gostișev V.K. Modalități și oportunități pentru prevenirea complicațiilor infecțioase în chirurgie // Metoda. recom .: Abordări raționale și prevenirea complicațiilor infecțioase în chirurgie
.
M., 1997; 2-11.
48. Stepanov V.N. Profilaxia infecției perioperatorii Posibilitatea unei singure administrări de agenți antibacterieni // Miere nouă. revistă. 1998; 2: 23-4.
49. Shevola D., Dmitrieva N.V. Profilaxia antibiotică în practica medicală. M., 1998; 128 sec
50. Yakovlev V.P., Yakovlev S.V. Terapie antibacteriană modernă în tabele // Consilium. 1999; 1 (1): 18-36.
Ce este? Intoxicația sanguină este o afecțiune în care microorganismele patogene intră în fluxul sanguin, înmulțindu-se rapid și răspândindu-se în tot corpul. Agenții cauzali pot include bacterii, virusuri și flora fungică.
Cu toate acestea, nu orice lovitură a unui microorganism din sânge duce la infecția sa - o combinație de mai mulți factori este necesară:
- intrarea simultană a unui număr mare de agenți patogeni în sânge;
- insuficiența resurselor imune din organism care sunt capabile să oprească creșterea și reproducerea microorganismelor.
Prin urmare, probabilitatea de intoxicații cu sânge este cea mai mare în următoarele cazuri:
1. Dacă există un focal de infecție în organismavând o relație strânsă cu un vas de sânge sau limfă. Această situație este observată atunci când:
- pielonefrită;
- infecții dentare;
- patologia organelor ORL etc.
2. În suprimarea sistemului imunitar:
- Infecție cu HIV
- tratamentul cu citostatice sau steroizi (aceste medicamente neutralizează anticorpii, reduc producția lor și inhibă activitatea celulelor citotoxice, adică inhibă imunitatea celulară și umorală)
- splenectomie
- limfogranulomatoza si alte leucemii (tumori ale sistemului hematopoietic)
- leziune tumorală a oricărui organ (bolile oncologice sunt întotdeauna combinate cu o stare de imunitate depresivă, care este considerată cauza principală a tumorii)
- insolare excesivă prelungită (razele soarelui pot avea un efect dăunător asupra organelor imune - timus, măduvă osoasă, ganglioni).
3. Când sunt combinate infecție cronică și o stare de imunitate depresivă (acesta este cel mai sever caz).
Natura cursului intoxicațiilor cu sânge poate fi de la acut (fulminant) la cronic. În ultimul caz, cu diferite boli concomitente însoțite de imunodeficiență, se observă o exacerbare. Începutul timpuriu de a lua antibiotice duce la o cură completă.
Aceasta se reflectă în natura cursului infecției, care acum s-a schimbat semnificativ (numărul formelor fulminante a scăzut). Fără tratament, otrăvirea sângelui este întotdeauna fatală.
Principalele cauze ale otrăvirii sângelui

Modurile de intoxicație sanguină în toate cazurile sunt asociate cu orice (chiar și cea mai mică) posibilitate de contact direct al agentului patogen cu sângele, unde intră imediat. Poate fi:
- rani festive extinse;
- fierbe;
- răni postoperatorii.
În unele cazuri, cauza intoxicației cu sânge poate deveni o infecție a unui cheag de sânge care a căzut în filtrul vena cava inferioară sau este localizat în.
În mod similar, infecția apare în prezența cateterelor intravasculare. Acestea devin deosebit de periculoase dacă sunt instalate mult timp. Prin urmare, timpul optim între schimbarea cateterelor este de 72 de ore. Riscurile cateterelor venoase au un mecanism dublu:
- Posibilitatea directă de contact cu sângele și microorganismele care trăiesc în mediu;
- Posibilitatea formării și infecției unui cheag de sânge.
Există, de asemenea, posibilitatea unei infecții prin transfuzie de sânge. Prin urmare, materialul donat pregătit este testat timp de 6 luni. Acesta este stadiul ferestrei pentru majoritatea infecțiilor atunci când studiile serologice nu pot detecta anticorpi împotriva acestora.
Riscul există în timpul operațiunilor. Este deosebit de important pentru intervențiile ginecologice efectuate conform indicațiilor de urgență. Traseul nosocomial poate fi realizat prin pansamente, mâinile personalului și instrumente.
Adesea, sursa invaziei bacteriene nu poate fi detectată. Această afecțiune se numește sepsis criptogenă.
Diverse microorganisme pot deveni o cauză a otrăvirii sângelui:
- stafilococii;
- meningococi;
- pneumococ;
- pseudomonas aeruginosa;
- proteus;
- e coli;
- virus herpes;
- ciuperci (Candida, Aspergilus și altele).
De regulă, acesta este rezultatul otrăvirii sângelui cu un singur tip de microorganism, care începe să se împartă incontrolabil, „rupând” toate barierele de protecție. Combinația mai multor agenți patogeni sau modificarea lor în cursul bolii este o excepție, nu o regulă.
Primele semne și simptome ale intoxicației cu sânge
Când sângele este infectat, simptomele și manifestările bolii depind de tipul de microb cauzal și de starea sistemului imunitar. Simptomele clinice constau în manifestări generale și specifice. Semnele comune sunt:
- O creștere semnificativă a temperaturii până la 39-40 ° C;
- Frisoane;
- Transpirație crescută, în special noaptea, înlocuind frisoanele;
- Slăbiciune;
- Hepato- și splenomegalie (o creștere a ficatului și a splinei, respectiv);
- O erupție cutanată care apare pe piele și are diverse caracteristici (erupții cutanate, pete cu contur neuniform etc.);
- Lipsa poftei de mâncare, ceea ce duce la o reducere semnificativă a greutății până la cachexia;
- Durere în mușchi și articulații (în absența modificărilor morfologice în aceștia);
- Scăderea presiunii la valorile critice, care poate fi însoțită de dezvoltarea șocului septic cu pierderea cunoștinței.
Apariția primelor simptome ale otrăvirii sângelui nu este întotdeauna acută. Uneori se poate observa o creștere treptată a temperaturii și intoxicației. Cu toate acestea, într-o perioadă scurtă de timp, starea unei persoane devine vizibil mai grea - devine dificil pentru el să se deplaseze, să facă ceva de lucru, el refuză complet mâncarea etc.
Manifestările specifice sunt determinate de tipul de microorganism cauzal. În funcție de acest fapt, otrăvirea sângelui are următoarele caracteristici.
Sepsis stafilococic manifestată prin durere musculară severă și febră. Pe piele apar erupții unice sub formă de vezicule. Inițial, starea pacientului este extrem de dificilă, dar conștiința rămâne la același nivel. În același timp, poate fi prezentă o tuse uscată, care este însoțită apoi de eliberarea sputei galbene în cantități mari.
Sepsis meningococic Începe foarte repede. Starea pacientului este foarte gravă. Șocul se poate dezvolta în câteva ore. Caracteristicile distinctive ale acestei infecții sunt creșterea rapidă a congestiei cu pierderea cunoștinței, apar mai multe hemoragii de diferite forme pe piele.
Dezvoltarea șocului septic este facilitată de hemoragia suprarenală, care complică adesea infecția meningococică.
pneumococică otrăvirea sângelui se caracterizează prin astfel de semne: febră până la valori foarte mari, apariția frisoanelor și slăbiciunii severe, adynamia (atât fizică cât și psihică), intoxicația organismului.
Pentru generalizat infecția pneumococică, pierderea cunoștinței și șocul nu sunt caracteristice. În ciuda stării extrem de grave a pacientului, pentru acest tip de intoxicații din sânge, durerea musculară, erupțiile și tulburările severe în funcționarea organelor nu sunt caracteristice.
Comparativ cu infecția meningococică, pneumococul nu este caracterizat printr-un curs rapid. În același timp, îmbunătățirea clinică pe fundalul terapiei apare mult mai târziu.
Acest fapt se explică prin caracteristicile meningococilor, care sunt imune la multe medicamente antibacteriene. În cele mai multe cazuri, alegerea lor finală devine posibilă numai după obținerea rezultatelor unui studiu bacteriologic.

Sepsis gram-negativ cel mai adesea însoțește imunodeficiența și este cauzată de o infecție care se dezvoltă ca urmare a complicațiilor postoperatorii (supurație în cavitatea abdominală sau pelvis în timpul operațiilor ginecologice). Intoxicațiile de sânge postpartum sunt, de asemenea, foarte des asociate cu microorganisme gram-negative.
Diferențele clinice între acești microbi sunt o tendință crescută la hemoragii necrotice la nivelul pielii. Sunt erupții dureroase de roșu închis, înconjurate de un puț dens, care cresc treptat în dimensiune.
Infecția gram-negativă se caracterizează printr-o temperatură corporală scăzută (până la 38 ° C). Prin urmare, deseori pacienții solicită asistență medicală cu întârziere.
O excepție de la cursul clinic tipic este pseudomonas aeruginosadezvoltându-se pe fondul inhibării sistemului imunitar. Procesează cu viteza fulgerului, cu probabilitatea unei dezvoltări rapide a șocului (2-3 ore după debutul febrei).
Dezvoltarea infecției cu sânge herpetic apare întotdeauna din cauza imunodeficienței severe, care se observă cu leucemie și limfogranulomatoză (datorită scăderii activității antivirale a organismului), infecției HIV în stadiul SIDA și după transplant.
Infecțioase generalizate procesul începe cu apariția erupțiilor veziculelor herpetice pe piele de-a lungul coastelor. Apoi, există o răspândire masivă de erupții pe părțile rămase ale pielii, pe membrana mucoasă a traheei și bronhiilor, a cavității bucale și a esofagului.
După deschiderea veziculelor, o infecție stafilică se poate reaprinde din nou, ceea ce duce la supurație.

O caracteristică a unei boli infecțioase este masivitatea însămânțării microbiene de sânge în combinație cu tulburări severe de coagulare (DIC). Prin urmare, tratamentul intoxicațiilor cu sânge are ca scop eliminarea acestor doi factori patogeni.
Pacienții cu un diagnostic stabilit (sau numai dacă este suspectat) sunt întotdeauna spitalizați în secția de terapie intensivă sau în terapia intensivă.
Principala direcție a tratamentului este antibacteriană. Pentru aceasta, este selectat un medicament care corespunde sensibilității agentului patogen.
Dacă este imposibil să se stabilească cel mai probabil microorganism cauzativ în funcție de semnele clinice, terapia este prescrisă empiric. Medicamentele la alegere în acest caz sunt gentamicina + cefaloridină sau cefazolina.
Tratamentul este considerat adecvat dacă se observă îmbunătățiri clinice:
- Reducerea slăbiciunii.
- Dispariția frisoanelor.
- Lipsa apariției de noi erupții cutanate pe piele.
- Temperatura scade (dar poate rămâne ridicată câteva zile)
- În cadrul testului de sânge, există o scădere a procentului de neutrofile înțepate (forme tinere imature, care indică o sarcină crescută asupra sistemului imunitar, pe care nu le pot face față).
În cazurile în care nu există îmbunătățiri într-o zi după începerea tratamentului, grupul de antibiotice trebuie înlocuit. Se preferă fonduri mai puternice pentru o clasă mai mare în activitate.
Prezența imunodeficienței complică tratamentul intoxicațiilor cu sânge, deoarece nu toate antibioticele sunt eficiente. Astfel de pacienți li se recomandă terapia cu gamma globulină (endobulină). Aceste substanțe distrug direct agenții patogeni.
Pentru tratamentul sindromului DIC, sunt prescrise heparină, plasmafereză și transfuzia plasmei proaspăt înghețate. Cu toate acestea, alegerea unui medicament specific depinde de stadiul sindromului. Deci, în faza hipercoagulării este prezentată heparina și analogii acesteia, iar în faza hipocoagulării sunt contraindicate categoric. Plasmafereza ca metodă de purificare a sângelui de toxinele bacteriene este indicată în orice stadiu al tulburărilor de coagulare.
Efecte
Lipsa tratamentului în timp util pentru intoxicații sanguine duce întotdeauna la dezvoltarea mai multor leziuni în întregul corp care sunt incompatibile cu viața.
Cu o sensibilitate ridicată a microorganismelor cauzatoare la tratament și îmbunătățire clinică satisfăcătoare, antibioterapia durează 2-3 săptămâni. Dacă procesul se produce și se dezvoltă complicații, atunci tratamentul este efectuat timp de câteva luni.
Terapia cu început tardiv amenință dezvoltarea gangrenei extremităților (necroza țesuturilor), modificări ireversibile ale organelor interne și hemoragii la nivelul glandelor suprarenale. Aceste complicații sunt mortale.
După 2-4 săptămâni de la debutul bolii, pot apărea următoarele:
- dureri articulare
- semne de laborator de glomerulonefrită;
- murmur cardiac;
- tulburări ale ritmului cardiac;
- modificările ECG
Răspunsuri la întrebări frecvente despre otrăvirea sângelui
Cum se manifestă sângele HIV după infecție?
În formele severe de imunodeficiență, care includ stadiul SIDA în infecția cu HIV, microorganismele patogene condiționate pot provoca intoxicații cu sânge. În mod normal, trăiesc constant pe piele și mucoase, dar nu dăunează unui corp sănătos.
Odată cu imunodeficiențele, acestea devin cauza proceselor infecțioase severe. O altă caracteristică a infecției cu HIV este infecția polimicrobiană, a cărei apariție este asociată cu mai multe tipuri de agenți infecțioși simultan - această afecțiune se caracterizează printr-un curs extrem de sever.
Cât timp apare otrăvirea sângelui?
Reproducerea microorganismelor patogene (corespunzătoare perioadei de incubație, în care nu există manifestări clinice) poate dura de la câteva ore la câteva zile.
După apariția primelor simptome, otrăvirea sângelui poate continua cu viteze diferite. Se disting următoarele opțiuni:
- fulminant - dezvoltarea șocului în 1-2 zile cu un rezultat fatal;
- acut - durează 3-4 săptămâni;
- subacut - 3-4 luni;
- recurentă (perioadele de exacerbare și remisie sunt caracteristice) - 4-6 luni;
- croniosepsis - 12 luni sau mai mult.
Mai multe detalii despre manifestarea diferitelor forme și debitele sunt descrise mai sus.