Mulțumesc
Site-ul oferă informații de referință doar în scop informativ. Diagnosticul și tratamentul bolilor trebuie efectuate sub supravegherea unui specialist. Toate medicamentele au contraindicații. Este necesară consultarea unui specialist!
Informații generale
Glucocorticoizi sunt numiți hormoni steroizi secretați de cortexul suprarenal, precum și analogii lor artificiali utilizați în medicină.Primele mostre din aceste medicamente datează din anii 40 ai secolului XX, iar primii hormoni utilizați au fost hidrocortizonul și cortizon.
În total, cinci hormoni din acest grup au fost studiați până în prezent ( prezentate de gradul de impact asupra proceselor din organism în ordine descrescătoare):
- Hidrocortizon
- Cortizon
- Corticosteronul
- 11-deoxicortizol
- 11-dehidrocorticosteron.
Clasificarea medicamentelor
Toate medicamentele din acest grup sunt împărțite în:- natural ( hidrocortizon si cortizon),
- sintetic.
- halogenat ( beclometazonă, dexametazonă, fluticazonă),
- nehalogenat ( prednisolon, budesonid, clobetasol).
În funcție de durata expunerii, toate medicamentele pot fi împărțite în:
- scurtă acțiune ( cortizon, hidrocortizon),
- actiune de durata medie ( prednisolon, metilprednisolon),
- actiune de lunga durata ( dexametazonă, betametazonă, triamcinolonă).
Acțiune
Oamenii de știință nu au descoperit încă pe deplin mecanismul de acțiune al acestor hormoni asupra organismului. Intrând în celulă prin membrana celulară, hormonul acționează asupra receptorilor sensibili la substanțele steroizi, este trimis împreună cu receptorul către nucleul celular și participă la producerea componentelor proteice speciale implicate în procesul inflamator.Hormonii influențează următoarele procese care apar în organism:
- Metabolismul carbohidraților. Procesarea zahărului în organism se înrăutățește, uneori administrarea de medicamente provoacă diabet zaharat.
- Metabolismul proteinelor. Producția de proteine în oase, mușchi și piele este suprimată. Prin urmare, un pacient care ia aceste medicamente pierde în greutate, are vergeturi pe piele, hemoragii, tăieturi și zgârieturi cicatrici slab și mușchii se atrofiază. Osteoporoza se dezvoltă adesea.
- Metabolismul lipidelor. Există o creștere a cantității de grăsime subcutanată la nivelul feței, gâtului, pieptului și scăderea volumului la nivelul brațelor și picioarelor.
- Metabolismul calciului. Hormonii din această clasă suprimă absorbția calciului de către intestine și accelerează scurgerea acestuia din oase. Prin urmare, există posibilitatea dezvoltării deficienței de calciu.
- Lucrarea inimii și a vaselor de sânge. Sub influența acestor hormoni, permeabilitatea vaselor mici de sânge se înrăutățește. Hormonii tonifică vasele de sânge și contractilitatea mușchiului inimii.
- Proces inflamator. Orice manifestări inflamatorii sunt suprimate, deoarece glucocorticoizii reduc permeabilitatea membranelor celulare la anumite substanțe implicate în procesul inflamator. În plus, pereții vaselor de sânge sunt întăriți, ceea ce inhibă mișcarea celulelor imune în leziune.
- Reglarea imunității. Acești hormoni suprimă răspunsul imun local, motiv pentru care sunt utilizați în transplantul de țesut. Ele suprimă activitatea anumitor celule imunitare ( limfocite și citokine „antiinflamatorii”.), implicate în dezvoltarea unor boli precum meningita și reumatismul.
- Formarea sângelui. Sub influența acestor hormoni, producția de limfocite, eozinofile și monocite scade simultan, iar producția de eritrocite și trombocite crește. Chiar și o singură doză de medicament pentru o zi schimbă imaginea sângelui. Dacă tratamentul a fost pe termen lung, este nevoie de 7 până la 30 de zile pentru a restabili imaginea normală.
- Activitatea glandelor endocrine. Legătura dintre hipotalamus, glanda pituitară și glandele suprarenale este suprimată. Această tulburare devine vizibilă cu cursuri lungi de medicamente. Producția de hormoni sexuali scade și ea, ceea ce duce la dezvoltarea osteoporozei.
Indicatii
- Insuficiență suprarenală de orice origine,
- Terapia de șoc,
- Reumatism,
- leucemie acută limfoblastică și mieloblastică,
- Mononucleoza infectioasa ,
- Stare astmatică,
- Alergii complicate de colagenoză, dermatoze, astm,
- Inflamații de diferite localizări,
- Anemie hemolitică,
- Pancreatita acuta,
- Hepatita virala,
- Transplant de organe și țesuturi,
- Boală autoimună.
Contraindicatii
Absolut:- Boli fungice
- Infecții virale,
- Intoleranță individuală.
- osteoporoza severa,
- Diabet,
- Grad ridicat de insuficiență cardiacă
- Tensiune arterială crescută
- Ulcer gastric sau intestinal
- Probleme mentale.
Dacă vorbim despre salvarea urgentă a vieții pacientului, medicamentele sunt utilizate în orice caz.
Mai multe informații despre medicamentele esențiale
 Cortizon
CortizonFolosit pentru terapia de substituție la pacienții cu insuficiență suprarenală. Produs sub formă de tablete. Se utilizează numai atunci când ficatul funcționează normal. Afectează schimbul de apă și săruri.
Hidrocortizon
Este prescris pentru insuficiența suprarenală. Nu este recomandat pentru edem, disfuncție cardiacă, hipertensiune arterială, deoarece contribuie la retenția de sodiu în organism și la excreția de potasiu. Produs sub formă de lichid pentru injecție, suspensie.
Prednisolon
Un medicament prescris destul de frecvent. Se produce sub formă de tablete, lichid și suspensie injectabilă, pulbere în fiole.
Metilprednisolon
Mai puternic decât prednisolonul, provoacă mai puține efecte secundare și este mai scump. Indicat pacienților care suferă de obezitate, ulcer gastric și boli mintale. Disponibil sub formă de tablete, suspensii, substanțe uscate în sticle.
Dexametazonă
Acesta este unul dintre cele mai puternice medicamente din acest grup. Deoarece medicamentul are multe efecte secundare, nu este utilizat în cure lungi. prescris, printre altele, pentru a atenua starea pacientului în timpul chimioterapiei, precum și pentru a preveni problemele de respirație la copiii prematuri. Disponibil sub formă de tablete și lichid pentru injectare în fiole.
Betametazonă
Este similară ca putere cu dexametazona și are mai puține efecte secundare. Cel mai adesea folosit sub formă de lichid pentru injecție, inclusiv intra-articular și periarticular. Durata de acțiune a unor astfel de injecții poate ajunge la o lună datorită compoziției chimice speciale a medicamentului.
Produs sub formă de tablete, lichid în fiole, suspensii.
Medicamente pentru inhalare
Beclometazonă– medicamentul este utilizat în tratamentul astmului bronșic, ameliorează inflamația și ameliorează alergiile. Când este utilizat ca inhalare, practic nu este absorbit în sânge și nu acționează sistemic.Contraindicatii:
- bronhospasm acut,
- intoleranţă,
- stare astmatică,
- bronșită bacteriană.
Budesonida– terapia principală pentru astmul bronșic, boala pulmonară obstructivă cronică.
Contraindicatii:
intoleranță individuală. Lichidul pentru inhalare este interzis pentru utilizare în tratamentul copiilor sub 16 ani, suspensia este interzisă pentru utilizarea în tratamentul copiilor sub 3 luni și pulberea pentru copiii sub 6 ani.
sarcină, alăptare, boli fungice, virale și bacteriene ale sistemului respirator, tuberculoză.
Medicamentul poate provoca un atac de tuse, uscarea mucoasei bucale, dureri asemănătoare migrenei, stomatită, greață și hiperactivitate.
Medicamentul nu trebuie să intre în contact cu ochii.
Fluticazonă– medicamentul este prescris pentru astmul bronșic și boala pulmonară obstructivă cronică ca tratament principal.
Contraindicatii:
- bronșită non-astmatică,
- intoleranţă,
- bronhospasm acut,
- starea astmatică.
- osteoporoza,
- infectii generale,
- alaptare,
- sarcina.
Acest medicament nu este utilizat pentru ameliorarea atacurilor de astm.
Preparate pentru uz sistemic
 Medicamentele au fost create pentru uz sistemic prednison, cortizon.
Medicamentele au fost create pentru uz sistemic prednison, cortizon.Există destul de multe medicamente care sunt utilizate atât local, cât și sistemic. Acestea includ: betametazonă, dexametazonă, triamcinolonă, fludrocortizon, mazipredonă, metilprednisolon, prednisolon.
Astfel de medicamente sunt utilizate atât sub formă de tablete pentru uz oral, cât și în injecții.
Unguente, creme, lotiuni
Glucocorticoizii pentru uz extern sunt disponibili sub formă de unguente, geluri, creme și loțiuni. prescris pentru anumite boli dermatologice de natură neinfecțioasă.Indicatii:
- dermatita de contact,
- dermatita seboreica,
- lichen plan,
- eritrodermie,
- lupus eritematos discoid.
Cum să alegeți forma de dozare potrivită a medicamentului?
UnguenteÎncep să acționeze mai încet și consistența lor este grasă. Sunt prescrise pentru pielea uscată predispusă la procese de descuamare și plâns.
Creme poate provoca iritații sau uscăciune dacă există răni pe piele. Sunt prescrise pentru fenomene intertriginoase. Această formă nu lasă pete grase și se absoarbe rapid.
Lotiuni indicat pentru conditii umede, foarte convenabil pentru tratarea scalpului.
Toți glucocorticosteroizii utilizați în dermatologie sunt împărțiți în patru grupe în funcție de puterea efectului lor:
- Foarte puternic: calcinonidă, propionat de clobetasol.
- Puternic: budesonid, dexametazonă, flumetazonă, triaminolonă.
- Putere medie: prednisolon.
- Slab: hidrocortizon.
Efecte secundare
Glucocorticosteroizii ameliorează foarte repede multe simptome nedorite ale bolilor. Cu toate acestea, ele provoacă destul de multe efecte secundare. Prin urmare, ele sunt prescrise numai în cazurile în care nu alții nu pot ajuta.În special, multe efecte secundare sunt observate cu utilizarea sistemică a acestor medicamente. Au fost dezvoltate mai multe metode noi pentru utilizarea acestor medicamente, care reduc puțin probabilitatea apariției efectelor nedorite. Dar tratamentul cu aceste medicamente necesită, în orice caz, monitorizarea constantă a stării generale a pacientului.
Atunci când utilizați medicamente hormonale steroizi, este posibil să apară următoarele reacții adverse:
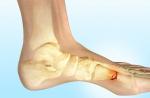
- Din partea aparatului de mișcare: osteoporoză, compresie
Glucocorticoizi sistemici
Glucocorticoizi sistemici
sunt împărțite în mai multe grupe:
■ După origine:
- natural (hidrocortizon);
- sintetice: (prednisolon, metilprednisolon, triamcinolon, dexametazonă, betametazonă).
■ După durata acțiunii:
- medicamente de scurtă durată (hidrocortizon), medie (prednisolon, metilprednisolon) și de lungă durată (triamcinolon, dexametazonă, betametazonă).
Farmacocinetica
Atunci când sunt administrați pe cale orală, glucocorticoizii sunt bine absorbiți din tractul gastrointestinal. Concentrația maximă în sânge este creată după 1,5 ore.
Glucocorticoizii se leagă de proteinele plasmatice:
a) cu α1-globulina (transcortină), formând cu aceasta complexe care nu pătrund în țesuturi, dar creează un depozit al acestor hormoni;
b) cu albumine, formând cu acestea complexe care pătrund în țesuturi. Doar glucocorticoizii liberi sunt activi biologic.
Ele sunt îndepărtate rapid din plasmă, pătrund cu ușurință în barierele histohematice, inclusiv hematoencefal, placentare și în laptele matern, acumulându-se în țesuturi, unde rămân active mult mai mult timp. 25-35% din glucocorticoizii liberi se depun in eritrocite si leucocite. Dacă hidrocortizonul se leagă de transcortină cu 80-85%, de albumină cu 10%, atunci glucocorticoizii sintetici se leagă de proteine cu 60-70%, adică. fracția lor liberă, care pătrunde bine în țesuturi, este mult mai mare. Cantitatea de glucocorticoizi care intră în celule este, de asemenea, influențată de capacitatea acestora de a se lega de receptori intracelulari specifici.
Glucocorticoizii suferă biotransformare în ficat, parțial în rinichi și în alte țesuturi, în principal prin conjugare cu glucuronid sau sulfat. Sunt excretate în bilă și urină prin filtrare glomerulară și sunt reabsorbite în proporție de 80-90% de tubuli. 20% din doză este excretată nemodificat de către rinichi. O mică parte (în medie 0,025%) dintr-o doză de prednisolon administrată intravenos este excretată în laptele matern. În acest caz, scăderea concentrației de glucocorticoid în laptele matern are loc mai rapid decât în serul sanguin. Timpul de înjumătățire (Tabelul 6.2) din plasma (T1/2) al hidrocortizonului este de 60-90 minute, prednison, prednisolon și metilprednisolon - 180-200 minute, triamcinolon și fluocortolon - 210 minute, dexametazonă, betametazonă și parametazonă - 19030 minute. Adică, eliminarea glucocorticoizilor sintetici, în special a celor fluorurati, are loc mai lent, iar aceștia au un efect inhibitor mai mare asupra cortexului suprarenal. Timpul de înjumătățire al hidrocortizonului din țesuturi este de 8-12 ore, prednison, prednisolon și metilprednisolon - 12-36 ore, triamcinolon și fluocortolon - 24-48 ore, dexametazonă și betametazonă - 36-54 ore (până la 72 ore).
De când medicii au aflat la mijlocul secolului trecut că cortexul suprarenal sintetizează glucocorticoizii, medicamentele bazate pe acest grup de hormoni au intrat rapid în medicină. În mod neașteptat, s-a dovedit că până acum un hormon necunoscut trăiește în aproape toate celulele corpului și ajută la combaterea inflamației, suprima imunitatea agresivă, elimină consecințele șocului - și aceasta nu este o listă completă de acțiuni. În zilele noastre, medicamentele pe bază de GCS pot fi găsite sub mai multe forme: tablete, injecții IV și intramusculare, unguente, glucocorticosteroizi inhalatori. De ce sunt aceste medicamente atât de populare în rândul medicilor?
Ce este?
Glucocorticoizi - acesta este un anumit tip de hormon produs de cortexul suprarenal. Ei fac parte din grupul mai mare „corticosteroizi”, o rudă a căruia este mineralocorticoizii. Glucocorticoizii sunt adesea denumiți „glucocorticosteroizi” deoarece cuvintele sunt sinonime.
Glucocorticoizii pot fi găsiți în aproape toate țesuturile corpului uman în cantități variate. Principalul reprezentant al GCS este cortizolul, un derivat al hidrocortizonului. Corticosteronul și cortizonul pot fi observate și în doze mai mici. Acești compuși chimici influențează multe procese negative care au loc în organism.

Opinia expertului
Filimoshin Oleg Alexandrovici
doctor - neurolog, clinica orășenească din Orenburg. Studii: Orenburg State Medical Academy, Orenburg.
Inițial, hormonii naturali erau utilizați în medicină, dar utilizarea lor a fost asociată cu un risc ridicat de efecte secundare, așa că acum chimiștii folosesc corticosteroizi mai avansati. De exemplu, dexametazona sintetizată este de 30 de ori mai eficientă decât cortizolul și, în același timp, este mult mai puțin probabil să provoace reacții adverse atunci când este utilizată.
Cum funcționează?
 Un premiu Nobel poate fi acordat pentru răspunsul la această întrebare, deoarece în momentul de față mecanismul exact de acțiune al GCS este necunoscut. În general, aceștia funcționează în același mod ca toți hormonii - transmit informații altor celule ale corpului despre procesele care au loc în organism. Glanda pituitară este responsabilă pentru eliberarea de glucocorticoizi, care pot elibera în sânge o substanță specială - corticotropina. Atunci când este necesar, acest element chimic ordonă glandelor suprarenale să secrete corticosteroizi. Mai multă corticotropină înseamnă mai mult cortizol și invers.
Un premiu Nobel poate fi acordat pentru răspunsul la această întrebare, deoarece în momentul de față mecanismul exact de acțiune al GCS este necunoscut. În general, aceștia funcționează în același mod ca toți hormonii - transmit informații altor celule ale corpului despre procesele care au loc în organism. Glanda pituitară este responsabilă pentru eliberarea de glucocorticoizi, care pot elibera în sânge o substanță specială - corticotropina. Atunci când este necesar, acest element chimic ordonă glandelor suprarenale să secrete corticosteroizi. Mai multă corticotropină înseamnă mai mult cortizol și invers.
Pune întrebarea ta unui neurolog gratuit
Irina Martynova. A absolvit Universitatea de Medicină de Stat Voronezh, numită după. N.N. Burdenko. Rezident clinic și neurolog al „Policlinicii din Moscova” BUZ VO.

Opinia expertului
Mitruhanov Eduard Petrovici
doctor - neurolog, clinică orășenească, Moscova. Educație: Universitatea Medicală de Stat din Rusia, Instituția de învățământ de la bugetul de stat de formare profesională continuă, Academia Medicală Rusă de Învățământ Postuniversitar a Ministerului Sănătății al Federației Ruse, Universitatea Medicală de Stat din Volgograd, Volgograd.
Modul în care funcționează glucocorticoizii în interiorul celulelor este un mister medical. Se crede că în nucleele tuturor celulelor există receptori speciali, care, atunci când diferite cantități de steroizi intră în ele, încep să se comporte într-un anumit fel. Dar aceasta este doar o presupunere.
Cum afectează ele organismul?
GCS au un spectru larg de acțiune. Direcții principale:
- Antiinflamator. Medicamentele (glucocorticoizii) inhibă puternic inflamația prin reducerea activității enzimelor care distrug țesutul. Sub influența lor, membranele celulare devin mai grosiere, drept urmare schimbul de fluide și elemente chimice între zonele afectate și cele sănătoase scade. Ele suprimă, de asemenea, sinteza proteinelor lipocortinei din acidul arahidonic, care sunt responsabile pentru răspândirea inflamației.
- Efecte asupra altor hormoni. GCS afectează alți mediatori, mai ales insulina. Eliberarea de steroizi în sânge în timpul hipoglicemiei este principala armă a organismului pentru a corecta rapid situația.
- Anti-stres, anti-șoc. Acest grup de hormoni, atunci când este stresat sau în stare de șoc, îi spune măduvei osoase să producă mai multe celule sanguine (în caz de pierdere de sânge) și sistemului cardiovascular să crească tensiunea arterială.
- Efect imunoregulator. La doze mici în sânge, GCS crește ușor imunitatea la doze mari o poate suprima de multe ori, până la 1% eficacitate față de normă. Această proprietate este utilizată pentru a preveni respingerea țesuturilor după transplanturi.
- Anti alergic. Mecanismul acestei acțiuni nu este, de asemenea, complet clar, dar glucocorticoizii fac față în mod eficient manifestărilor alergiilor.
- Efectul asupra metabolismului. Glucocorticosteroizii pot interfera cu metabolismul glucozei, enzimelor glicolitice, glicogenului, diferitelor proteine, grăsimi, sodiu, clor, potasiu, calciu și apă.
Este demn de remarcat faptul că nu in toate aceste cazuri, GCS actioneaza in beneficiul organismului. De exemplu, cu expunerea prelungită la cantități mari de hormon, calciul este spălat din oase, determinând pacientul să dezvolte osteoporoză (creșterea fragilității scheletului).
Când sunt prescrise?
Lista bolilor care sunt tratate cu acești steroizi provine din domeniile lor de acțiune menționate mai sus. Principalele indicații de utilizare sunt următoarele:
- Reacții alergice, cel mai adesea astm. În ciuda faptului că mecanismul de acțiune asupra reacțiilor alergice nu a fost încă clarificat, aproape fiecare astmatic a inhalat glucocorticosteroizi (ICS) în cutii.
- Inflamații neinfecțioase ale pielii. Capacitatea GCS de a reduce inflamația și-a găsit o aplicație largă în dermatologie. În cazul inflamației infecțioase, glucocorticoidul utilizat în tratament trebuie combinat cu un medicament care ucide infecția.
- Anemia, boli ale sistemului hematopoietic. Medicamentele bazate pe aceasta stimulează măduva osoasă să producă celule sanguine.
- Leziuni, boli reumatice. De obicei, un astfel de diagnostic include inflamația, stresul asupra corpului și o încălcare a mecanismelor de apărare ale organismului.
- Perioada după transplantul de țesuturi și organe, radiații și chimioterapie. GCS modifică răspunsul sistemului imunitar la acești factori, ceea ce are un efect pozitiv asupra dinamicii.
- Insuficiență suprarenală. În acest caz, medicamentele au efectul cel mai direct - ele completează lipsa de hormoni din sânge pe care ar trebui să o furnizeze glandele suprarenale.
Pe lângă aceste indicații, există și altele mai specifice. În astfel de cazuri decizia de a utiliza glucocorticosteroizi trebuie luată de un medic cu experiență.
Efecte secundare de la utilizarea GCS
A interfera cu echilibrul hormonal al corpului înseamnă a interfera cu comunicarea normală a părților corpului între ele. Reacțiile adverse de la această acțiune pot fi destul de grave:
- Osteoporoza. Datorită modificărilor metabolismului, calciul este eliminat mai rapid din organism, ceea ce duce la fragilitatea oaselor.
- Instabilitate emoțională, psihoză. Cauzat de modificări în funcționarea glandei pituitare.
- Diabetul cu steroizi. Steroizii cresc nivelul de glucoză din sânge.
- Insuficiență suprarenală. Acest lucru poate părea ciudat, având în vedere că o boală similară este o indicație de utilizare. Dar expunerea pe termen lung la medicamente care conțin corticosteroizi pe corp face ca glandele suprarenale să funcționeze mai puțin eficient, deoarece există deja o mulțime de hormoni în sânge, iar dacă medicamentul este întrerupt brusc, glandele suprarenale nu mai sunt capabile să furnizeze. organismul cu cantitatea necesară de glucocorticosteroizi.
- Sângerări, ulcere. O creștere a producției de celule sanguine duce la o încărcare a sistemului circulator și se poate „defalca”.
- Cu un curs de tratament pe termen lung (mai mult de 1,5 ani) la copii, dezvoltarea sexuală este uneori suprimată din cauza suprimării glandelor suprarenale.
- Obezitate, acnee, față umflată, nereguli menstruale. Aceste efecte secundare sunt cauzate de dezechilibre hormonale.
- Diverse boli oculare.
Reacțiile adverse locale apar atunci când se utilizează unguente și inhalatoare.
Unguentele sunt de obicei provoca pielea uscată din cauza permeabilității celulare scăzute, iar inhalatoarele duc aproape întotdeauna la tuse, gură uscată și răgușeală.
Este de remarcat faptul că aproape toate consecințele utilizării acestor medicamente sunt reversibile. Doar diabetul, întârzierea creșterii la copii și cataracta subcapsulară sunt ireversibile.
Utilizați cu prudență!
 Glucocorticosteroizii sunt un medicament puternic, dar periculos din cauza reacțiilor adverse. Acestea trebuie utilizate pentru un curs cât mai scurt posibil și numai sub supravegherea constantă a unui medic. Cea mai sigură cale este tratamentul într-un spital, sub supravegherea medicilor care pot face analizele necesare, fac ecografie sau ECG dacă este necesar.
Glucocorticosteroizii sunt un medicament puternic, dar periculos din cauza reacțiilor adverse. Acestea trebuie utilizate pentru un curs cât mai scurt posibil și numai sub supravegherea constantă a unui medic. Cea mai sigură cale este tratamentul într-un spital, sub supravegherea medicilor care pot face analizele necesare, fac ecografie sau ECG dacă este necesar.
Medicamentul are un sindrom de sevraj, așa că tratamentul trebuie încheiat fără probleme, reducând treptat doza de medicament. O versiune ușoară a sindromului de sevraj se manifestă prin febră și stare de rău. Severă poate duce la criza Addisoniană.
Contraindicatii
Dacă este necesară o singură utilizare, singura contraindicație absolută este intoleranța individuală a pacientului la GCS. Terapia pe termen lung nu trebuie prescrisă persoanelor cu:
- Diabet;
- sarcina;
- sifilis, tuberculoză, recent vindecat de infecție;
- boala Itsenko-Cushing;
- psihoză;
- boli ale ficatului, rinichilor, tractului gastrointestinal și ale sistemului circulator (fiecare boală este individuală, trebuie să consultați medicul);
Medicamentele glucocorticoide trebuie prescrise copiilor numai în cazuri extreme.
Unguentele și picăturile nu trebuie utilizate dacă există infecții la locurile de utilizare.
Complicații după administrare
Complicațiile frecvente sunt bolile din lista de efecte secundare. Dacă apar, trebuie să reconsiderați doza sau să întrerupeți complet medicamentul.
Auto-medicația cu o doză greșită va duce cel mai probabil la dezechilibru hormonal sau diabet.
Durata de acțiune a GCS
Medicamentele (glucocorticosteroizi) sunt împărțite în trei tipuri: cu acțiune scurtă, cu acțiune medie și cu acțiune lungă. Corticosteroizii cu acțiune scurtă rămân în sânge timp de 2-12 ore, cei cu acțiune medie timp de 0,75-1,5 zile, iar cei cu acțiune prelungită timp de 36 până la 52 de ore.
Durata de acțiune depinde în mare măsură de calea de administrare.
Metode de aplicare
 Metodele de aplicare includ: pastile(glucocorticosteroizi sistemici); injecții(pentru boli articulare sau ca alternativă la tablete); unguent, gel, cremă, tencuieli(glucocorticosteroizi topici); inhalatoare(glucocorticoizi inhalatori).
Metodele de aplicare includ: pastile(glucocorticosteroizi sistemici); injecții(pentru boli articulare sau ca alternativă la tablete); unguent, gel, cremă, tencuieli(glucocorticosteroizi topici); inhalatoare(glucocorticoizi inhalatori).
Glucocorticoizii în tablete sunt utilizați pentru boli pulmonare acute, cum ar fi astmul bronșic, boala pulmonară obstructivă cronică, pneumonia și altele. Medicamentul este aproape complet absorbit din stomac, concentrația maximă în sânge este atinsă după o oră și jumătate.
Când nu este posibil să se administreze pacientului corticosteroizi sistemici sub formă de tablete sau medicamentul trebuie să acționeze mai rapid, se utilizează administrarea intravenoasă sau în țesuturi moi. Aceeași tactică este folosită pentru bolile articulare - corticosteroizii sunt injectați direct în ligamentul deteriorat.
Aplicarea topică pe piele are succes în tratarea inflamației subcutanate și a reacțiilor alergice la nivelul pielii. În plus, atunci când este utilizată corect, această opțiune este destul de sigură în ceea ce privește efectele secundare.
Inhalatoarele livrează o doză de medicament direct în bronhii și plămâni. Acest tip a devenit foarte răspândit printre astmatici, deoarece glucocorticoizii inhalatori sunt cel mai convenabil și eficient mod de a controla astmul.
Lista medicamentelor
Ingredientele active sunt împărțite în funcție de durată în:
- Corticosteroizi cu acțiune scurtă: Alclometazonă, Budesonid, Hidrocortizon, Clobetasol, Cortizon, Mazipredonă, Mometazonă, Flunisolide, Fluocortolon, Fluocinolon acetonid, Fluticazonă, Ciclesonid;
- Corticosteroizi cu durată medie: metilprednisolon, aceponat de metilprednisolon, prednisolon, triamcinolon, fludrocortizon;
- Corticosteroizi cu acțiune prelungită: Beclometazonă, Betametazonă, Dexametazonă.
Glucocorticoizi pentru uz oral
- Budenofalk, Budesonide;
- Decdan, ;
- Dexazonă, Dexametazonă;
- Dexametazonă, Dexametazonă;
- Megadexan, Dexametazonă;
- Fortecortin, Dexametazonă;
- Cortizon, Cortizon;
- , Metilprednisolon;
- Apo-prednison, Prednison;
- Prednisol;
- Prednisolon, Prednisolon;
- Berlincourt, ;
- Polcortolon, Triamcinolon;
- Triamcinolonă, Triamcinolonă;
- Tricort, Triamcinolonă;
- Cortineff, Fludrocortizon.
Glucocorticoizi pentru injectare
- Betametazonă fosfat de sodiu, Betametazonă;
- dipropionat de betametazonă, betametazonă;
- Celeston, Betametazonă;
- Decdan, Dexametazonă;
- Dexazonă, Dexametazonă;
- Dexaben, Dexametazonă;
- Dexafar, Dexametazonă;
- Fortecortin Mono, Dexametazonă;
- , Hidrocortizon;
- Solu-Cortef, Hidrocortizon;
- Urbazon, metilprednisolon;
- Medopred, Prednisolon;
- Prednisolon, Prednisolon;
- Prednisolon fosfat de sodiu, Prednisolon;
- Solyu-Decortin N, Prednisolon;
- , Triamcinolonă;
- Tricort, Triamcinolon.
Glucocorticoizi inhalatori
- Beclazon, Beclometazonă;
- Beclodet 250, Beclometazonă;
- Beclometazonă, Beclometazonă;
- Beclospir, Beclometazonă;
- Bekodisk, Beclometazonă;
- Becotide, Beclometazonă;
- Klenil, Beclometazonă;
- Plibecort, Beclometazonă;
- Rinoclenil, Beclometazonă;
- Benacort, Budesonide;
- Budesonid, Budesonid;
- Asmanex Twistheiler, Mometasone;
- Azmacort, Triacinolonă;
- Ingacort, Flunisolide;
- Alvesco, Cyclesonide.
GCS pentru uz intranazal
- Aldecin, Beclometazonă;
- Nasobek, Beclometazonă;
- Budoster, Budesonide;
- Tafen nazal, Budesonid;
- Desrinit, Mometasone;
- Nosefrină, Mometazonă;
- Sintaris, Funisolide;
- Nazarel, Fluticazonă.
GCS pentru uz local în oftalmologie, ginecologie etc.
- Dexametazonă, Dexametazonă;
- Dexoftan, Dexametazonă;
- , Hidrocortizon;
- , Prednisolon;
- Prednisolon fosfat de sodiu, Prednisolon;
- Rektodelt, Prednison;
- Cortineff, Fludrocortizon.
Unguent, gel sau cremă pentru uz extern
- Afloderm, Alclometazonă;
- Akriderm, Betametazonă;
- Betliben, Betametazonă;
- Betnovate, Betametazonă;
- Celestoderm-B, Betametazonă;
- Apulein, Budesonide;
- Novopulmon E Novolizer, Budesonid;
- Dermovate, Clobetasol;
- Powercourt, Clobetasol;
- Akortin, Hidrocortizon;
- Laticort, Hidrocortizon;
- Lokoid, Hidrocortizon;
- Deperzolon, Mazipredonă;
- Advantan, aceponat de metilprednisolon;
- Mometazonă-Akrikhin, Mometazonă;
- Monovo, Mometasone;
- Uniderm, Mometasone;
- Ultralan, Fluocortolon;
- Sinaflan, acetonidă de fluocinolonă;
- Flucort, acetonid de fluocinolon;
- Fluocinolon acetonid, Fluocinolon acetonid;
- Flucinar, acetonida de fluocinolon.
Glucocorticosteroizii sunt hormoni produși de glandele suprarenale. Ele pot fi găsite în aproape toate țesuturile corpului. Ele îndeplinesc multe funcții, în principal efecte de dezvoltare (în copilărie) și efecte terapeutice. Pentru unele boli, este posibilă creșterea cantității de glucocorticosteroizi din organism prin medicamente pentru a combate inflamația complexă, răspunsul imun sau alte probleme medicale.
6275 0
Indexul descrierilor medicamentelor
BetametazonăHidrocortizon
Metilprednisolon
Prednisolon
Triamcinolonă
Flumetazonă
Nu există INN
- Lorinden A
- Lorinden S
- Triderm
Mecanismul de acțiune și efectele farmacologice
Mecanismul de acțiune al GCS este asociat cu capacitatea lor de a interacționa cu receptorii specifici din citoplasma celulei: complexul steroizi-receptor pătrunde în nucleul celulei, se leagă de ADN, influențând transcrierea unei game largi de gene, ceea ce duce la modificări în sinteza proteinelor, enzimelor și acizilor nucleici. GCS afectează toate tipurile de metabolism și are efecte antiinflamatorii, antialergice, antișoc și imunosupresoare pronunțate.Mecanismul efectului antiinflamator al GCS este de a suprima toate fazele inflamației. Stabilizarea membranelor structurilor celulare și subcelulare, incl. liză, medicamentele antiinflamatoare steroidiene împiedică eliberarea enzimelor proteolitice din celulă, inhibă formarea radicalilor liberi de oxigen și a peroxizilor lipidici în membrane. La locul inflamației, GCS strânge vasele mici și reduce activitatea hialuronidazei, care contribuie la inhibarea etapei de exudare, previne aderarea neutrofilelor și monocitelor la endoteliul vascular, limitează pătrunderea acestora în țesuturi și reduce activitatea macrofagelor. și fibroblaste.
Capacitatea GCS de a inhiba sinteza și eliberarea mediatorilor inflamatori (PG, histamina, serotonina, bradikinina etc.) joacă un rol semnificativ în implementarea efectului antiinflamator. Ele induc sinteza lipocortinelor - inhibitori ai biosintezei fosfolipazei A2 și reduc formarea de COX-2 la locul inflamației. Aceasta duce la o limitare a eliberării acidului arahidonic din fosfolipidele membranelor celulare și la o scădere a formării metaboliților săi (PG, leucotriene și factor de activare a trombocitelor).
GCS sunt capabile să inhibe faza de proliferare, deoarece limitează pătrunderea monocitelor în țesutul inflamat, împiedicând participarea lor la această fază a inflamației, suprimă sinteza mucopolizaharidelor, proteinelor și inhibă procesele de limfopoieză. În caz de inflamație de origine infecțioasă, este indicat să se combine GCS cu terapia antimicrobiană, având în vedere efectul lor imunosupresor.
Efectul imunosupresor al GCS se datorează scăderii numărului și activității limfocitelor T care circulă în sânge, scăderii producției de imunoglobuline și influenței T-helpers asupra limfocitelor B, scăderii conținutului de complement. în sânge, formarea complexelor imune fixe și a unui număr de interleukine, inhibarea formării unui factor care inhibă migrarea macrofagelor.
Efectul antialergic al GCS se datorează scăderii numărului de bazofile circulante, perturbării interacțiunii receptorilor Fc localizați pe suprafața mastocitelor cu regiunea Fc a IgE și componenta C3 a complementului, care împiedică intrarea unui semnal în celulă și este însoțită de o scădere a eliberării histaminei, heparinei și serotoninei din celulele sensibilizate și alți mediatori ai alergiei de tip imediat și previne efectul acestora asupra celulelor efectoare.
Efectul antișoc se datorează participării GCS la reglarea tonusului vascular; pe fondul lor, sensibilitatea vaselor de sânge la catecolamine crește, ceea ce duce la creșterea tensiunii arteriale, modificări ale metabolismului apă-sare, sodiul și apa sunt reținute, volumul plasmatic crește și hipovolemia scade.
Farmacocinetica
Majoritatea corticosteroizilor (cu excepția medicamentelor sintetice de uz local) sunt bine absorbiți din tractul gastrointestinal, indiferent de aportul alimentar. Medicamentele pătrund bine prin membranele mucoase și barierele histohematice, inclusiv. prin BBB și placentă. În sânge, se leagă în mare parte la proteine (60-90%) - transcortină (acest complex nu pătrunde în țesuturi, fiind un fel de depozit de hormoni) și albumină (acest complex pătrunde în țesuturi). GCS sunt metabolizate în primul rând în ficat prin hidroxilare și conjugare, precum și în rinichi și alte țesuturi. Ele sunt excretate în principal de rinichi sub formă de metaboliți inactivi.Locul în terapie
În practica stomatologică, corticosteroizii injectabili sunt utilizați pentru îngrijirea de urgență în condiții de șoc; local (mai rar sistemic) - pentru tratamentul pulpitei și parodontitei, bolilor mucoasei bucale și ale glandelor salivare de natură inflamatorie și alergică, pentru artrita și artroza articulației temporomandibulare, precum și pentru osteomielita, periostita, pemfigus și lichen planus.Tolerabilitate și efecte secundare
Acest grup de medicamente provoacă destul de des reacții adverse: este posibilă suprimarea reactivității organismului, exacerbarea patologiei infecțioase cronice și a bolilor gastrointestinale. Cu utilizarea pe termen lung, este posibilă creșterea tensiunii arteriale, dezvoltarea diabetului steroizi, edem, slăbiciune musculară, distrofie miocardică, sindrom Itsenko-Cushing și atrofie suprarenală.Uneori, la consumul de droguri, se observă agitație, insomnie, creșterea presiunii intracraniene și psihoză. Cu utilizarea sistemică pe termen lung a GCS, este posibilă perturbarea sintezei țesutului osos și a metabolismului calciu-fosfor, ceea ce duce în cele din urmă la osteoporoză și fracturi spontane.
Contraindicatii
- Hipersensibilitate.
- Infecții severe.
- Boli virale și fungice.
- Formă severă de tuberculoză.
- SIDA.
- Ulcer peptic, sângerare gastrică.
- Forme severe de hipertensiune arterială.
- Sindromul Itsenko-Cushing.
- Nefrită.
- Sifilis.
- Diabet.
- Osteoporoza.
- Sarcina.
- Alăptarea.
- Psihoze acute.
- Vârsta copiilor mici.
- Leziuni infecțioase (bacteriene, virale, fungice) ale pielii și mucoaselor.
- Tumori ale pielii.
- Încălcarea integrității pielii și a membranelor mucoase.
- Vârsta copiilor mici.
Interacţiune
GCS sporește efectul bronhodilatator al stimulentelor β-adrenergice și al teofilinei, reduce efectul hipoglicemiant al insulinei și agenților antidiabetici orali și activitatea anticoagulantă a cumarinelor (anticoagulante indirecte).Difenină, efedrina, fenobarbital, rifampicina și alte medicamente care provoacă inducerea enzimelor hepatice microzomale scurtează T1/2 din GCS. Somatotropina și antiacidele reduc absorbția GCS. Atunci când sunt combinate cu glicozide cardiace și diuretice, riscul de aritmii și hipokaliemie crește atunci când sunt combinate cu AINS, crește riscul de afectare gastrointestinală și sângerare gastrointestinală.
Farmacologia clinică a glucocorticosteroizilor.
Ph.D. L.I. DYATCHINA
Până în prezent, s-a acumulat o sumă imensă; experiență în utilizarea glucocorticosteroizilor (GCS). Efectul clinic uimitor, efectul antiinflamator puternic și activitatea imunomodulatoare pronunțată a GCS permit utilizarea lor în multe boli. Expunerea la glucocorticosteroizi; asupra organelor și sistemelor este necesară pentru funcționarea normală a întregului organism în ansamblu.

REGLEMENTAREA ELIBERĂRII DE GLUCOCORTICOSTEROIZI
Principalul GCS endogen este cortizolul, care este sintetizat și secretat de cortexul suprarenal ca răspuns la efectul stimulator al hormonului adrenocorticotrop (ACTH). În mod normal, zilnic se secretă aproximativ 15-30 mg de cortizol. Hormonul este eliberat în impulsuri - 8-10 impulsuri/zi. Nivelul secretiei de cortizol nu ramane constant pe parcursul zilei (concentratia maxima in sange este atinsa la 7-8 a.m., cea minima la miezul noptii). Sub stres (infecție, intervenție chirurgicală, hipoglicemie), sinteza și secreția de GCS crește de aproximativ 10 ori (până la 250 mg/zi).

Reglarea eliberării GCS este controlată de mecanismul hipotalamo-hipofizar. Când concentrația de cortizol liber scade, hipotalamusul eliberează corticotropină, un factor de eliberare care stimulează eliberarea hormonului adrenocorticotrop (corticotropină) în glanda pituitară anterioară. Hormonul adrenocorticotrop (ACTH), la rândul său, determină eliberarea GCS din cortexul suprarenal.
MECANISMUL DE ACȚIUNE AL GLUCOCORTICOSTEROIZII
Efectul hormonilor glucocorticosteroizi asupra celulei se manifestă prin efectul lor asupra aparatului genetic al celulei. Legătura principală în acțiunea glucocorticosteroizilor asupra celulei este interacțiunea lor cu receptorii specifici ai organelor țintă.
GCS sunt substanțe lipidice (derivați de colesterol) și se pot dizolva în membranele celulare. Pătrunderea hormonului în celulă este posibilă nu numai sub formă legată (cu ajutorul unei proteine purtătoare), ci și pasiv. Receptorii pentru steroizi sunt localizați în citoplasma celulelor. Cu toate acestea, densitatea lor în diferite celule nu este aceeași: de la 10 la 100 de receptori sensibili la steroizi, care pot provoca sensibilitate diferită a țesuturilor la GCS. În plus, GCS poate avea tropism diferit pentru GCR. Astfel, cortizolul glucocorticosteroid endogen se leagă preferenţial de GCR-ul membranei citoplasmatice, în timp ce GCS sintetic, dexametazona, se leagă într-o măsură mai mare de GCR citosolic. Numărul de receptori pentru glucocorticosteroizi (GCR) poate varia semnificativ și se poate modifica în timpul terapiei cu GCS.
Următorul pas este mișcarea complexului receptor hormonal (HRC) în nucleul celular. Pătrunderea GRK-urilor în nucleu este posibilă după o restructurare a structurii lor (activare), ceea ce duce la capacitatea lor de a se lega de componentele nucleului.
GRK activat se leagă de o regiune specifică a ADN-ului din nucleu. Complexul GRK-ADN ajută la creșterea sintezei ARN. Studii recente au arătat că efectul hormonilor glucocorticosteroizi asupra biosintezei ARN-ului mesager (ARNm) este pasul principal în implementarea efectelor biologice ale GCS în celulele organelor țintă.
GCS poate avea atât un efect stimulator specific, cât și un efect inhibitor asupra sintezei diferitelor ARN. Efectele multidirecționale se pot manifesta în același organ și, probabil, răspunsul final al celulei la un semnal hormonal depinde de raportul lor. GCS afectează, de asemenea, activitatea ARN polimerazei. A fost descrisă posibilitatea interacțiunii steroizilor cu proteinele cromatinei non-histone, ceea ce duce la o modificare a structurii acestora. Efectul antiinflamator al steroizilor este mediat prin GCR-uri specifice, modificări ale activității GRC și sinteza ARN și proteine (cale nucleară).
EFECTELE FARMACODINAMICE ALE GLUCOCORTICOSTEROIZII
- Efectul antiinflamator al GCS se manifestă sub formă de efecte antiexudative și antiproliferative.
- Efect imunosupresor
- Efect antialergic
- Impact asupra proceselor metabolice
Se determină efectul antiexudativ al GCS o6 (Tabelul nr. 1):
- Efect de stabilizare a membranei și, drept consecință, scăderea permeabilității membranelor celulare și subcelulare (mitocondrii și lizozomi);
- Permeabilitate redusă a peretelui vascular, în special a capilarelor, și vasoconstricție la locul inflamației. Vasoconstricția este un efect specific al GCS asupra patului vascular la locul inflamației. În același timp, efectul lor asupra altor vase poate provoca, dimpotrivă, vasodilatație. Mecanismul acestei acțiuni a GCS nu este pe deplin înțeles, este asociat cu suprimarea eliberării mediatorilor lipidici și a activatorilor sistemului kininului și o scădere a activității hialuronidazei;
- Suprimarea sintezei anumitor citokine implicate în reacții inflamatorii, precum și blocarea sintezei proteinelor receptorilor de citokine;
- Scăderea producției de interleukine (IL): IL-1, IL-3, IL-4, IL-5, IL-b și IL-8, factor de necroză tumorală - alfa (TNF - α), factor de stimulare a coloniilor de macrofage de granulocite ( GM-CSF), prin suprimarea, transcrierea sau reducerea timpului de înjumătățire al ARN-ului mesager;
- Inhibarea migrării mastocitelor și eozinofilelor la locul inflamației. Se știe că glucocorticosteroizii reduc numărul de eozinofile prin suprimarea producției de GM-CSF și IL-5;
- Suprimarea degranulării mastocitelor și a eliberării de amine biologic active (histamină, serotonină, kinine și prostaglandine) din mastocite;
- Reducerea intensității proceselor de generare a energiei în locul inflamației;
- Inhibarea migrării neutrofilelor la locul inflamației, întreruperea activității lor funcționale (chemotactice și fagocitare). GCS provoacă leucocitoză periferică atât după o singură doză (timp de 4-6 ore), cât și cu tratament de lungă durată (în ziua a 14-a) cu o scădere ulterioară a nivelului de leucocite;
- Suprimarea migrației monocitelor prin încetinirea eliberării monocitelor mature din măduva osoasă și reducerea activității lor funcționale.
EFECTUL ANTIINFLAMATOR AL GLUCOCORTICOSTEROIZII
|
Efect anti-exudativ |
|
|
Efect antiproliferativ |
|
În prezent, există o ipoteză că în mecanismul acțiunii antiinflamatorii a GCS este importantă capacitatea acestora de a induce sinteza unora (lipomodulină) și de a suprima sinteza altor proteine (colagen) în celule. Mediatorul efectului antiinflamator al GCS este cel mai probabil lipomodulina (macrocortină, lipocortină), a cărei sinteză are loc sub influența unor concentrații mici ale acestor hormoni în diferite tipuri de celule. Lipomodulina blochează fosfolipaza A2 a membranelor celulare și, prin urmare, perturbă eliberarea acidului arahidonic legat de fosfolipide, care este apoi transformat în prostaglandine, leucotriene și tromboxan. Aceștia din urmă participă activ la procesele de inflamație. Inhibarea leucotrienelor B4 reduce chemotaxia leucocitelor, iar leucotrienele C4 și D4 (substanță cu reacție lentă) reduce capacitatea contractilă a mușchilor netezi, permeabilitatea vasculară și secreția de mucus în căile respiratorii.

Scăderea producției de citokine, în special IL-1, cauzată de GCS, suprimă, de asemenea, activitatea fosfolipazei A2 și, în mare măsură, a ciclooxigenazei-2 (COX-2).
În prezent, monoxidul de azot (NO) este considerat și cel mai important inițiator al răspunsului inflamator. Glucocorticosteroizii reduc producția de oxid nitric prin inhibarea activității enzimei NO sintetazei (NOS), așa cum se arată într-un experiment pe monocite.
O creștere a expresiei endopeptidazei neutre este importantă în implementarea efectului antiinflamator al glucocorticosteroizilor în inflamația neurogenă. Endopeptidaza neutră joacă un rol în descompunerea tahikininei, aceasta din urmă fiind eliberată de terminațiile nervoase senzoriale. Endopeptidazele, după cum au arătat studiile, sunt, de asemenea, responsabile pentru degradarea peptidelor bronhoconstrictoare, cum ar fi bradikinina, tahikinina și endotelina-1.
Efectul antiproliferativ al GCS este asociat cu:
- cu suprimarea lor a sintezei acizilor nucleici;
- diferențierea afectată a fibrocitelor de fibroblaste;
- o scădere a activității lor funcționale, ceea ce duce la inhibarea proceselor de scleroză la locul inflamației.
INFLUENȚA GLUCOCORTICOSTEROIZLOR ASUPRA RĂSPUNSULUI IMUN
Efectul glucocorticosteroizilor asupra sistemului imunitar este mediat de prezența receptorilor specifici de glucocorticoizi pe celulele limfoide. Sub influența steroizilor, numărul de limfocite din sângele periferic scade. Acest lucru se datorează în mare parte redistribuirii limfocitelor din sânge către țesuturi, în primul rând către măduva osoasă și splină. În acest caz, GCS provoacă apoptoza limfocitelor T și B imature sau activate. Există un punct de vedere că efectul imunosupresor al glucocorticosteroizilor se realizează prin controlul numărului absolut de celule limfoide și subpopulațiilor acestora.
Citokinele joacă un rol important în reacțiile imune. Citokina cheie este IL-2, care este implicată în inducerea răspunsurilor imune care apar după interacțiunea unei celule T cu o celulă prezentatoare de antigen. GCS reduce semnificativ producția de IL-2, rezultând o scădere a fosforilării dependente de IL-2 a diferitelor proteine. Aceasta duce la suprimarea proliferării celulelor T. În plus, glucocorticosteroizii suprimă activarea celulelor T prin inhibarea producției de IL-3, IL-4, IL-6 și alte citokine. Deoarece glucocorticosteroizii suprimă citokinele secretate de alte celule, funcția T-helpers, T-supresori, limfocitelor T citotoxice și, în general, reacțiile imunologice scade. În același timp, T-helperii sunt mai sensibili la glucocorticosteroizi decât T-supresorii.
Efectul inhibitor al GCS asupra celulelor B este slab. Dozele moderate și mici de corticosteroizi nu provoacă modificări semnificative ale nivelului de imunoglobuline din sânge. Reducerea conținutului de imunoglobuline se realizează prin prescrierea de doze mari și foarte mari de glucocorticosteroizi (terapie pulsului). Steroizii inhibă activitatea sistemului complement și formarea complexelor imune fixe.
GCS are un efect pronunțat asupra activității macrofagelor și monocitelor. Având în vedere că monocitele și macrofagele joacă un rol semnificativ în dezvoltarea procesului inflamator și în implicarea altor tipuri de celule în acesta, este evident că efectul GCS asupra migrației, secreției și activității funcționale a acestora poate fi decisiv în reacția inflamatorie. în sine.
Alte efecte ale GCS sunt asociate cu inhibarea fagocitozei, eliberarea de substanțe pirogene, scăderea activității bactericide a celulelor, inhibarea secreției de colagenaze, elastaze și activatori ai plasminogenului și eliberarea afectată a factorilor macrofagi care provoacă formarea mucusului.
Principalele efecte imunosupresoare ale GCS sunt reflectate în Tabelul nr. 2.
EFECTUL IMUNOSUPPRESIV AL GLUCOCORTICOSTEROIZII
|
Mecanismele care stau la baza acestui efect |
|
|
Efect imunosupresor |
|
În procesul inflamator imunitar, precum și în dezvoltarea răspunsului la stres, sistemul hipotalamus-hipofizo-suprarenal joacă un rol semnificativ. Multe citokine stimulează sistemul funcțional hipotalamus-hipofizo-suprarenal.
INFLUENȚA GLUCOCORTICOSTEROIZULUI ASUPRA METABOLISMULUI ȚESUTULUI
Efectul GCS asupra metabolismului carbohidraților este de a stimula procesele de gliconogeneză, adică. sinteza glicogenului din produși ai metabolismului proteinelor și azotului. În același timp, rata de utilizare a glucozei de către țesuturi este perturbată prin reducerea pătrunderii acesteia în celulă. Ca urmare, unii pacienți pot prezenta hiperglicemie tranzitorie și glicozurie. Hiperglicemia prelungită duce la epuizarea aparatului insular pancreatic și la dezvoltarea diabetului zaharat „steroid”.
Efectul GCS asupra metabolismului proteinelor se manifestă prin descompunerea crescută a proteinelor în majoritatea organelor și țesuturilor și, mai ales, în țesutul muscular. Consecința acestui lucru este o creștere a conținutului de aminoacizi liberi și de produse de metabolizare a azotului în plasma sanguină. Ulterior, produsele metabolismului proteinelor și azotului sunt utilizate în procesele de gluconeogeneză.
Defalcarea proteinelor din țesutul muscular provoacă pierderea în greutate, atrofia musculară, slăbiciune musculară și creșterea afectată a cartilajului și a țesutului osos. Suprimarea sintezei proteinelor în matricea osoasă a vertebrelor duce la o întârziere a formării scheletului la copii. Procesele distrofice care apar în alte țesuturi sunt însoțite de dezvoltarea de ulcere „steroidiene”, distrofii miocardice și atrofie cutanată (striae).
O creștere a proceselor de catabolism proteic se observă cu utilizarea dozelor terapeutice medii de GCS. Utilizarea unor doze mici de GCS, dimpotrivă, stimulează sinteza albuminei în ficat din aminoacizii liberi din plasma sanguină. Acest lucru este deosebit de important la pacienții cu insuficiență a funcției hepatice proteine-sintetice.
Efectul GCS asupra metabolismului grasimilor se manifesta sub forma actiunii lor lipolitice si in acelasi timp lipogenetice. Efectul lipolitic se observă în grăsimea subcutanată a brațelor și picioarelor efectul lipogenetic se manifestă prin depunerea predominantă de grăsime în peretele abdominal anterior, regiunea interscapulară, pe față și gât. Acest proces este cel mai pronunțat cu utilizarea pe termen lung a corticosteroizilor, duce la o modificare a aspectului pacienților și este descris în literatură ca Cushingoid (față în formă de lună, obezitate de tip hipofizar, toleranță alterată la glucoză etc.). Efectul GCS se manifestă printr-o creștere a conținutului de colesterol și lipoproteine din serul sanguin. GCS accelerează procesul de transformare a carbohidraților în grăsimi, ceea ce contribuie și la dezvoltarea obezității.
Efectul GCS asupra metabolismului apă-mineral este asociat, pe de o parte, cu suprimarea secreției de hormon antidiuretic, care este însoțită de creșterea ratei de filtrare glomerulară, eliberarea de sodiu și apă din organism. În același timp, la pacienții cu insuficiență cardiacă severă, GCS poate stimula sinteza aldosteronului, ceea ce duce la retenția de sodiu și lichide și la creșterea sindromului de edem. Descompunerea proteinelor în țesuturi este însoțită de o creștere a potasiului și calciului în plasma sanguină. Dezvoltarea treptată a hipocaligistiei contribuie la intensificarea proceselor degenerative în țesuturi și, în primul rând, în mușchiul inimii, care poate provoca aritmii cardiace, cardialgie și poate duce la creșterea severității insuficienței cardiace. GCS inhibă absorbția calciului în intestin și crește excreția acestuia în urină. Ca rezultat, eliberarea de calciu din țesutul osos crește, ceea ce contribuie la formarea osteoporozei „steroidiene”. Hipercalciuria și, în același timp, o creștere a conținutului de uree și acid uric în urină duce la dezvoltarea diatezei acidului uric și la exacerbarea gutei la un număr de pacienți care iau corticosteroizi timp îndelungat. Deficitul de calciu în oase poate contribui la fracturi patologice ale oaselor la copii și vârstnici.
Efectul GCS asupra proceselor metabolice tisulare este prezentat în Tabelul #3.
INFLUENȚA GLUCOCORTICOSTEROIZULUI ASUPRA PROCESELOR DE METABOLISM ȚESUTULUI
|
Tipuri de schimburi |
|
|
pentru metabolismul carbohidraților |
|
|
pentru metabolismul proteinelor |
|
|
pentru metabolismul grăsimilor |
|
|
pentru metabolismul apă-mineral |
|
Ar trebui spus despre influența GCS asupra funcțiilor altor organe și sisteme care nu sunt responsabile pentru formarea răspunsului farmacologic principal.
- Administrarea de GCS duce la o creștere a producției de acid clorhidric și pepsină în stomac.
- Efectul GCS asupra organelor endocrine se manifestă prin inhibarea secreției de ACTH și gonadotropină în lobul anterior al glandei pituitare, o scădere a funcției gonadelor cu dezvoltarea amenoreei și infertilității secundare și suprimarea secreția de hormoni tiroidieni.
- GCS în sistemul nervos central poate crește excitabilitatea structurilor corticale ale creierului și poate reduce pragul de convulsii. Au un efect euforic la un număr de pacienți și, în anumite condiții, provoacă dezvoltarea depresiei.
- GCS are efect asupra sângelui periferic (Tabelul nr. 4).
INFLUENȚA GLUCOCORTICOSTEROIZULUI ASUPRA SÂNGELE PERIFERIC
FARMACOCINETICA GLUCOCORTICOSTEROIZII
Atunci când sunt administrate pe cale orală, GCS sunt absorbite în principal în intestinul subțire. Absorbția are loc în părțile proximale (75%) și distale (25%) ale intestinului subțire.
Cortexul suprarenal al unui adult sănătos, sub influența corticotropinei, produce zilnic 15-60 mg cortizol și 1-4 mg corticosteron. Peste 95% din cortizolul plasmatic formează complexe cu proteinele plasmatice, în principal cu alfa globulină care leagă corticosteroizii (transcortina). Afinitatea hormonului pentru transcortină este foarte mare, cu toate acestea, capacitatea de legare a transcortinei este scăzută și atunci când concentrația plasmatică de cortizol crește peste 20 mcg/100 ml, acesta este complet epuizat. În acest caz, transferul medicamentului este efectuat de albumine plasmatice (de la 40 la 90% din GCS din plasma sanguină sunt într-o stare asociată cu albumine). În același timp, numai fracția nelegată (liberă) a GCS este activă fiziologic, care își exercită efectul farmacologic asupra celulelor țintă. Efectele secundare la pacienții care primesc corticosteroizi sunt determinate de cantitatea de fracțiune liberă de GCS. Cu toate acestea, nu există o corelație între timpul de înjumătățire și durata acțiunii fiziologice a unui anumit medicament GCS.
GCS sunt clasificate în medicamente cu acțiune scurtă, intermediară și lungă, în funcție de durata suprimării ACTH după o singură doză. În același timp, timpul de înjumătățire al GCS este mult mai scurt: de la 30 de minute pentru cortizon și 60 de minute pentru prednisolon la 300 de minute pentru dexametazonă.
Interesant este că activitatea farmacologică maximă a GCS are loc într-un moment în care concentrațiile lor de vârf în sânge sunt deja în urma lor. Astfel, conform studiilor de farmacocinetică, concentrația maximă de prednisolon în plasmă este atinsă după 1-3 ore, timpul de înjumătățire este de 2-3,5 ore, iar efectul biologic maxim se dezvoltă în aproximativ 6 ore. Acest lucru sugerează că efectele GCS depind într-o măsură mai mare de inducerea activității enzimatice în interiorul celulei decât de acțiunea lor directă. Perioada de activitate antiinflamatoare a GCS este aproximativ egală cu durata de suprimare a axei hipotalamo-hipofizo-suprarenale - HPA (de la 4 la 8 zile).
În mod normal, nivelurile de cortizol încep să crească la 2 a.m. cu un vârf la 8 a.m. și revin la nivelurile bazale la 12 p.m. Simptomele RA (rigiditate, activitate inflamatorie) scad de obicei la câteva ore după trezire, la vârful sintezei cortizolului. Până de curând, se credea că administrarea GCS dimineața inhibă sinteza ACTH și cortizol într-o măsură mai mică decât noaptea și seara. Recent, au apărut dovezi că o creștere circadiană a nivelurilor IL-6 poate fi, de asemenea, asociată cu o creștere a activității RA dimineața. Fluctuațiile zilnice ale IL-6 sunt observate în mod normal și la pacienții cu RA. În mod normal, concentrația maximă de IL-6 apare puțin mai devreme decât ACTH și cortizol între 1 și 4 dimineața. Cu toate acestea, în RA, vârful IL-6 este întârziat și apare între 2 și 7 dimineața, iar concentrația de IL-6 este semnificativ mai mare decât în mod normal. Prin urmare, administrarea de GCS (5-7,5 mg) noaptea (la aproximativ 2 dimineața) este mai de preferat din punctul de vedere al suprimării secreției de IL-6 și este asociată cu o reducere semnificativ mai pronunțată a duratei dimineții. rigiditate, dureri articulare, indice Lansbury, indice Ritchie.
La pacienții netratați cu RA activă, se observă, de asemenea, o slăbire a sintezei cortizolului bazal și stimulat de corticotropină. Mai mult, aproximativ 10% dintre pacienții cu RA prezintă semne de insuficiență suprarenală. Evident, la acești pacienți ne putem aștepta la o eficacitate mai mare a dozelor mici de GCS decât la pacienții fără un defect în axa HPA.
Diferitele activități ale GCS sunt, de asemenea, determinate de diferitele grade de legare la proteinele plasmatice. Astfel, majoritatea cortizolului natural se leagă, în timp ce doar 3% din metilprednisolon și mai puțin de 0,1% din dexametazonă se leagă de globulina care leagă corticosteroizii.
Enzimele hepatice microzomale metabolizează GCS în compuși inactivi, care sunt apoi excretați de rinichi. Metaboliții sunt excretați în urină sub formă de glucuronide, sulfați și compuși neconjugați. Reacțiile de conjugare apar în primul rând la nivelul ficatului și, într-o măsură mai mică, la rinichi. Metabolismul hepatic crește odată cu hipertiroidismul și este indus de fenobarbital și efedrina Hipotiroidismul, ciroza și tratamentul concomitent cu eritromicină duc la o scădere a clearance-ului hepatic al GCS. La pacienții cu insuficiență hepatocelulară și niveluri scăzute de albumină serică în plasmă, crește concentrația fracției libere de prednisolon, ceea ce contribuie la o dezvoltare mai rapidă a reacțiilor adverse. În timpul sarcinii, dimpotrivă, proporția fracțiunii sale libere scade.
CLASIFICAREA GLUCOCORTICOSteroizilor
În funcție de durata suprimării ACTH după o singură doză, GCS se împart în: a) GCS cu acțiune scurtă - inhibă activitatea ACTH până la 24-36 de ore, b) GCS de durată medie - până la 48 de ore și c) lung -GCS in actiune - peste 48 de ore.
I. NATURAL– Cortizol, Cortizon (Hidrocortizon), Acetat de cortizon – inhibă activitatea ACTH până la 24-36 de ore.
II. SEMI SINTETIC
- Medicamente cu acțiune scurtă - prednisolon, prednison, metilprednisolon (Urbazon, Metipred) - inhibă activitatea AGTG până la 24-36 de ore.
- Medicamentele cu acțiune medie – Triamcinolona (Polcortolone) – inhibă ACTH până la 48 de ore.
- Medicamentele cu acțiune prelungită - betametazona, dexametazona - inhibă ACTH mai mult de 48 de ore.
APLICAREA GLUCOCORTICOSTEROIZILOR
Domeniul clasic de utilizare terapeutică a GCS este procesele patologice generale precum inflamația, alergiile, scleroza și degenerarea derivaților de țesut conjunctiv.
GCS sunt utilizate ca agenți antiinflamatori, antialergici și imunosupresori, precum și ca terapie de substituție pentru insuficiența suprarenală.
Se disting următoarele opțiuni pentru terapia GC:
- Sistem:
- doze terapeutice medii
- terapie alternanta
- terapia cu puls
- terapie „mini-puls”.
- combinate (în primul rând cu substanțe citotoxice)
- Local (administrare intraarticulară, inhalatorie, rectală etc.);
- Local (unguente, picături, aerosoli).
Terapia sistemică cu GCS este una dintre cele mai eficiente metode pentru tratarea unui număr de boli. Utilizarea steroizilor poate îmbunătăți semnificativ prognosticul și poate crește speranța de viață a pacienților.
În tratamentul GCS, se disting în mod convențional următoarele faze:
- Inducție: utilizați corticosteroizi cu acțiune scurtă (prednisolon sau metilprednisolon) într-o doză care corespunde aproximativ la 1 mg/kg greutate corporală pe zi, la intervale de 8 ore.
- Consolidare: implică trecerea la o singură doză din întreaga doză de GCS dimineața.
- Scădere: rata de scădere a GCS depinde de doză. Este posibil să treceți la terapie alternativă.
- Tratament de întreținere: utilizarea dozei minime eficiente de medicamente.
- Prevenirea complicațiilor terapiei GCS: începe cu faza de inducție.
Atunci când se efectuează terapia sistemică cu GCS, este necesar să se țină cont de câteva principii generale ale farmacoterapiei, respectarea cărora poate crește eficacitatea și siguranța tratamentului, precum și reducerea frecvenței efectelor secundare nedorite.
Terapia cu GK trebuie începută numai dacă există indicații stricte și cât mai devreme posibil, fără a încerca să folosiți mai întâi metode de tratament „mai blânde”. În acest caz, terapia hormonală trebuie utilizată împreună cu terapia convențională și nu trebuie prescrisă în locul acesteia. Terapia rațională presupune utilizarea corticosteroizilor cu acțiune scurtă în doza optimă și, dacă este posibil, pe perioada necesară controlului activității procesului.
GCS trebuie prescris numai sub supravegherea medicală a utilizării lor pentru a detecta precoce efectele secundare și a le corecta. Atunci când prescrieți terapia hormonală, nu numai medicul, ci și pacientul trebuie să fie informați în detaliu despre posibilitățile și complicațiile acestei metode de tratament.
- Prednisolonul este considerat standard în rândul GCS și eficiența altor medicamente din acest grup este evaluată în raport cu acesta. Dozele terapeutice medii de GCS per prednisolon sunt de 0,5-1 mg per kg de greutate corporală.
- Atunci când se prescrie GCS, trebuie respectat principiul dozelor echivalente pentru a obține același efect antiinflamator. Doze echivalente: prednisolon – 5 mg: triamcinolon – 4 mg: metilprednisolon – 4 mg: dexametazonă – 0,5 mg: betametazonă – 0,75 mg: hidrocortizon – 25 mg. În acest caz, calculul merge întotdeauna la prednisolon. La transferul pacienților de la administrarea parenterală a GCS la administrarea orală, este necesar să se reducă doza zilnică de 5-6 ori.
- În cazurile în care este de așteptat utilizarea pe termen lung a GCS, pacienții trebuie transferați cât mai repede posibil la o singură doză din întreaga doză dimineața și apoi la un regim alternativ de terapie GCS. La începutul tratamentului, doza zilnică de medicament este de obicei împărțită în 3 doze (faza de inducție), apoi se trece la o singură doză de medicament dimineața (faza de consolidare).
- Alegerea dozei inițiale de GCS, determinarea duratei terapiei și a ratei de reducere a dozei nu trebuie efectuate empiric, ci luând în considerare indicatorii clinici și de laborator standardizați ai activității procesului și a naturii bolii. Când prescrieți terapia GCS, ar trebui să acordați atenție următoarelor:
- doza zilnică necesară trebuie selectată individual, începând cu dozele terapeutice medii minime recomandate de obicei pentru această boală;
- pentru bolile cronice, GCS nu trebuie prescris în doze mari și pe o perioadă lungă de timp, iar atunci când apare remisiunea, utilizarea GCS trebuie oprită;
- în caz de afecțiuni care pun viața în pericol, trebuie prescrise imediat doze mari de corticosteroizi.
- În timpul terapiei hormonale în sângele periferic, există o scădere a numărului de eozinofile, limfocite, eritrocite, o scădere a nivelului de hemoglobină, în timp ce conținutul de leucocite crește din cauza neutrofilelor (până la 12.000). O astfel de hemogramă poate fi interpretată în mod eronat ca o continuare a unei exacerbări a procesului. În același timp, aceste modificări ar trebui considerate favorabile și indicând o doză suficientă de GCS.
- Rata de reducere a dozei de GCS. După obținerea unui efect clinic, doza de GCS trebuie redusă la o doză de întreținere. Pentru a face acest lucru, doza inițială de GCS este redusă treptat la nivelul minim la care se menține efectul pozitiv rezultat. Dacă doza zilnică a cursului de tratament este în intervalul de 15-40 mg/zi în termeni de prednisolon, atunci retragerea trebuie efectuată într-o rată de 2,5-5 mg la fiecare 5-7 zile până la atingerea dozei fiziologice. . Când GCS este prescris în doze de 40 mg sau mai mult, reducerea dozei poate avea loc mai rapid (5 mg și chiar în unele cazuri 10 mg pe săptămână) până la nivelul de 40 mg și apoi așa cum este indicat mai sus. În aceste cazuri, rata de reducere a dozei de GCS este determinată de durata utilizării lor. Cu cât durata cursului de tratament este mai scurtă, cu atât mai rapid este posibilă retragerea GCS. Cu toate acestea, cu cât doza de GCS este mai mică, cu atât perioadele dintre reducerile succesive ale dozei de medicament ar trebui să fie mai lungi. Această tactică vă permite să creați condiții pentru restabilirea funcționalității sistemului hipotalamo-hipofizo-suprarenal deja în timpul retragerii medicamentului.
- În caz de recidivă a bolii se reia terapia hormonală. Doza de GCS este crescută la cea la care pacientul a experimentat stabilizarea procesului. În viitor, retragerea ar trebui efectuată mai atent și treptat. Determinarea duratei terapiei și a ratei de reducere a dozei nu trebuie făcută empiric, ci luând în considerare indicatorii clinici și de laborator standardizați ai activității procesului și a naturii bolii. Există mai multe criterii de laborator pentru determinarea eficacității terapiei GCS: stabilizarea VSH timp de 7 zile scăderea nivelului de proteină C-reactivă, fibrinogen etc.
- Anularea glucocorticosteroizilor. Problemele asociate cu retragerea glucocorticosteroizilor apar după un curs lung de terapie. În acest caz, retragerea mai bruscă a medicamentelor amenință dezvoltarea a două tipuri de complicații. În primul rând, acestea sunt manifestări ale insuficienței suprarenale asociate cu suprimarea sistemului hipotalamo-hipofizo-suprarenal. În al doilea rând, aceasta este o recidivă a procesului inflamator care stă la baza bolii în sine.
- Suprimarea funcției suprarenale depinde de doza de hormoni luate și, într-o măsură și mai mare, de durata terapiei cu glucocorticoizi, precum și de proprietățile medicamentului utilizat și de boala de bază.
- O doză de prednisolon în intervalul 10-15 mg oferă un efect de înlocuire complet și este considerată fiziologică. În acest sens, retragerea medicamentului la o doză fiziologică poate fi efectuată destul de repede. O reducere suplimentară a dozei de GCS ar trebui să aibă loc într-un ritm mult mai lent.
- În timpul tratamentului, trebuie amintit că inhibarea axei hipotalamo-hipofizo-suprarenale persistă la pacienții care au primit chiar și doze mici de GCS (peste 10 mg/zi timp de trei sau mai multe săptămâni) timp îndelungat (până la 1 an) după întreruperea medicamentului.
- Întreruperea rapidă a medicamentului (în decurs de 1-2 zile) se efectuează extrem de rar numai în cazul psihozei acute cu steroizi sau în cazul generalizării infecției cu virus herpes.
- În cazurile în care nu este posibilă evitarea completă a terapiei cu glucocorticosteroizi, pacienții trebuie transferați la doze de întreținere de hormoni, individuale pentru fiecare pacient și corespunzătoare, de regulă, la doze de înlocuire de 5-15 mg de prednisolon pe zi. Hormonii trebuie administrați dimineața (de la 6 la 9 dimineața), ținând cont de bioritmul natural al eliberării lor.
- Există dovezi că nu există o inhibare semnificativă a axei hipotalamo-hipofizo-suprarenale dacă doza de prednisolon nu depășește 10 mg pe zi. În timpul tratamentului cu GCS, apariția reacțiilor adverse este semnificativ mai frecventă la pacienții cărora li se administrează mai mult de 10 mg de prednisolon pe zi. Riscul de reacții adverse este mai mic atunci când doza totală de prednisolon este redusă și medicamentul este luat la un anumit moment. În același timp, tratamentul cu doze mici de GCS poate reduce riscul potențial de osteoporoză din cauza inhibării sintezei IL-6.
- Pentru a reduce doza de GCS, se recomandă combinarea acestora cu AINS și terapia de bază. Cu toate acestea, acest lucru crește probabilitatea de a dezvolta leziuni ulcerative ale tractului gastrointestinal. Pentru a stimula producerea propriilor hormoni, în unele cazuri este posibil să prescrieți ACTH (corticotropină) pe fondul retragerii treptate a GCS.
- Când se utilizează GCS ca terapie de înlocuire pentru insuficiența suprarenală primară (boala Addison), este indicată administrarea simultană a unui glucocorticosteroid și a unui mineralocorticosteroid. Ca corticosteroizi se recomandă acetatul de cortizon sau hidrocortizonul în combinație cu acetatul de deoxicorticosteron sau fludrocortizonul.
În cazul insuficienței suprarenale secundare, datorită secreției de bază păstrate de aldosteron, în majoritatea cazurilor este posibilă utilizarea unui singur GCS. Cu sindromul adrenogenital, pacienții ar trebui să primească doze de întreținere de GCS pe tot parcursul vieții. Pacienții dependenți de hormoni cu dezvoltarea unor boli intercurente severe sau care necesită intervenții chirurgicale trebuie neapărat să primească terapie de substituție cu GCS în doze cu 5-10 mg mai mari decât cele pe care pacienții le iau în mod constant.
PRINCIPALE INDICAȚII PENTRU PRESCRIEREA GLUCOCORTICOSTEROIZII
- Boli reumatice:
- reumatism 2-3 grade. activitatea procesului în prezența carditei reumatice, în special în combinație cu poliartrita și poliserozita - doze terapeutice medii de GCS;
- lupus eritematos sistemic în timpul unei exacerbări (terapie cu puls), în forme cronice - doze terapeutice medii de GCS sau ca terapie de întreținere;
- dermatomiozită sistemică în timpul unei exacerbări - terapie cu puls cu GCS sau ca terapie de întreținere;
- periarterita nodoasă în timpul unei exacerbări - terapie cu puls cu GCS sau ca terapie de întreținere;
- artrita reumatoida in combinatie cu viscerita (sindrom febril, cardita, nefrita, serozita); pentru formele articulare cu progresie rapidă de artrită reumatoidă și un titru ridicat de factor reumatoid - terapia cu puls, apoi, adesea, terapia de întreținere; ineficacitatea terapiei anterioare cu AINS și a terapiei de bază - doze terapeutice medii de GCS, pentru monoartrite - administrare intraarticulară de GCS;
- artrita reumatoidă juvenilă.
Principalele indicații pentru prescrierea GCS pentru bolile reumatismale sunt prezentate în Tabelul nr. 5.
|
Utilizarea GCS în bolile reumatismale |
|||
|
Boli |
Indicatii |
Un drog |
|
|
RA Vasculită reumatoidă |
Ineficacitatea AINS sau contraindicații pentru prescrierea AINS (+ terapie de bază) |
Prev. 10 mg/zi |
– 2 mg/kg/zi |
|
Artrita, activitate scăzută a bolii. |
Prev. 15 mg/zi |
Prev. 1 mg/kg/zi + CP |
|
|
PM/DM |
Vasculita |
Prev. 1 mg/kg/zi |
2 mg/kg/zi |
|
SD |
Miozită, pleurezie, vasculită, |
Prev. 15-60 mg/zi |
|
|
Policondrita recidivanta |
Prev. 0,5 – 1,0 mg/kg/zi |
||
|
Efecte secundare ale liniei de bază |
Săruri de aur, penicilamină, |
Prev. 15 – 60 mg/zi |
|
|
Notă: Prev. – prednisolon. |
|||
- Vasculita sistemica - terapie sistemica cu GCS.
- Cardita (miocardită infecțios-alergică, miocardită Abramov-Fiedler, endocardită septică subacută - fază imunologică) - terapie sistemică cu GCS.
- Boli ale sistemului musculo-scheletic:
- osteoartrita posttraumatică - pentru utilizare pe termen scurt în perioada acută sau pentru administrarea intraarticulară a GCS;
- spondilită anchilozantă (spondilită anchilozantă);
- artrita gutoasă subacută - pentru utilizare pe termen scurt în perioada acută sau pentru administrarea intraarticulară a GCS;
- bursita acuta si subacuta;
- tenosinovita acută nespecifică;
- artrita psoriazica.
- Boli de rinichi (nefrită cronică cu sindrom nefrotic - cea mai indicată utilizare a GCS pentru variantele membranoase și membrano-proliferative; pentru nefrita lupică) - terapie sistemică cu GCS.
- Boli ale tractului gastrointestinal (colită ulcerativă nespecifică, boala Crohn, SPRU) - terapie sistemică cu GCS.
- Boli hepatice (hepatită autoimună) - terapie sistemică cu GCS.
- Boli ale sistemului bronhopulmonar (bronșită obstructivă, astm bronșic alergic, sarcoidoză - terapie sistemică și corticosteroizi inhalatori).
- Boli hematologice: anemie hemolitică dobândită (autoimună), purpură trombocitopenică - terapie sistemică cu GCS.
- Condiții alergice. Controlul afecțiunilor alergice atunci când remediile convenționale sunt ineficiente: rinită alergică sezonieră sau cronică, polipi nazali, astm bronșic (inclusiv afecțiunea bronșică), dermatită de contact, dermatită atopică (neurodermatită), hipersensibilitate la medicamente și boală serică (șoc anafilactic, edem Quincke, sindrom Quincke). Lyell, Steven-Johnson, agranulocitoză medicamentoasă sau alimentară, trombocitopenie, urticarie gigantică).
- Boli oculare: reacții alergice acute și cronice severe și procese inflamatorii la nivelul ochilor și structurilor adiacente, cum ar fi conjunctivita alergică, keratită, ulcer alergic marginal corneean, herpes corneean, irită și iridociclită, corioretinită, inflamație a segmentului anterior, uveită posterioară difuză și coroidită. nevrita retrobulbară, oftalmie simpatică.
- Boli de piele: eczeme (dermatită cronică), în tratamentul cheloizilor și inflamației infiltrante hipertrofice localizate (injectarea de corticosteroizi în zona afectată), lichen plan, psoriazis, granulom inelar, lichen cronic simplu (neurodermatită), lupus eritematos discoid, necrobioză lipoidica la diabetici, alopecie cuibărită, psoriazis, eritem nodos și altele - terapie locală cu GCS.
- Boli tumorale: tratamentul paliativ al leucemiei și limfomului la adulți, leucemie acută infantilă.
- Tulburări endocrine: insuficiență suprarenală primară sau secundară, insuficiență suprarenală acută, adrenectomie bilaterală, hiperplazie suprarenală congenitală, tiroidita acută și criză tireotoxică, hipercalcemie asociată cu cancer.
- Conditii de soc: hemodinamice, traumatice, endotoxice, cardiogene (infarct).
- Edemul cerebral (creșterea presiunii intracraniene) - GCS sunt necesare ca adjuvant pentru reducerea sau prevenirea edemului cerebral asociat cu traumatisme cerebrale chirurgicale sau de altă natură, accident vascular cerebral, tumori cerebrale maligne primare sau metastatice. Utilizarea glucocorticosteroizilor nu trebuie considerată ca înlocuitor al tratamentului neurochirurgical.
- Prevenirea respingerii alogrefei renale. Medicamentul este utilizat în combinație cu imunosupresoare utilizate în mod obișnuit.