Широкое распространение артериальной гипертензии (АГ) среди населения и ее роль в развитии сердечно-сосудистых осложнений определяют актуальность проведения своевременной и адекватной антигипертензивной терапии. Многочисленные контролируемые исследования показали высокую эффективность медикаментозных методов вторичной профилактики АГ в снижении частоты возникновения инсультов, сердечной и почечной недостаточности, в том числе и при мягкой АГ.
В клиническую практику для лечения АГ ингибиторы ангиотензинпревращающего фермента (иАПФ) широко вошли с 70-х годов прошлого века, став антигипертензивными препаратами первого ряда в лечении АГ.
Оригинальность препаратов данного класса состоит в том, что они впервые предоставили врачу возможность активно вмешиваться в ферментативные процессы, протекающие в ренин-ангиотензин-альдостероновой системе (РААС).
Действуя через блокаду образования ангиотензина II (АII), иАПФ оказывают влияние на систему регуляции артериального давления (АД) и в конечном итоге приводят к уменьшению отрицательных моментов, связанных с активацией рецепторов АII 1-го подтипа: они устраняют патологическую вазоконстрикцию, подавляют клеточный рост и пролиферацию миокарда и гладкомышечных клеток сосудов, ослабляют симпатическую активацию, уменьшают задержку натрия и воды.
Кроме воздействия на прессорные системы регуляции АД, иАПФ действуют и на депрессорные системы, повышая их активность за счет замедления деградации вазодепрессорных пептидов — брадикинина и простагландина Е 2 , которые вызывают релаксацию гладких мышц сосудов и способствуют продуцированию вазодилатирующих простаноидов и высвобождению эндотелийрелаксирующего фактора.
Эти патофизиологические механизмы обеспечивают основные фармакотерапевтические эффекты иАПФ: антигипертензивное и органопротекторное действие, отсутствие значимого влияния на углеводный, липидный и пуриновый обмен, уменьшение продукции альдостерона корой надпочечников, уменьшение выработки адреналина и норадреналина, подавление активности АПФ, снижение содержания АII и повышение содержания брадикинина и простагландинов в плазме крови.
В настоящее время в клиническую практику внедрены иАПФ 3-го поколения. Препараты из группы иАПФ отличаются между собой:
- по химической структуре (наличие или отсутствие сульфгидрильной группы);
- фармакокинетическим свойствам (наличие активного метаболита, особенность элиминации из организма, продолжительность действия, тканевая специфичность).
В зависимости от наличия в молекуле иАПФ структуры, взаимодейст-вующей с активным центром АПФ, различают:
- содержащие сульфгидрильную группу (каптоприл, пивалоприл, зофеноприл);
- содержащие карбоксильную группу (эналаприл, лизиноприл, цилазаприл, рамиприл, периндоприл, беназеприл, моэксиприл);
- содержащие фосфинильную/фосфорильную группу (фозиноприл).
Наличие сульфгидрильной группы в химической формуле иАПФ может определять степень связывания его с активным центром АПФ. В то же время именно с сульфгидрильной группой связывают развитие некоторых нежелательных побочных эффектов, таких как нарушение вкуса, кожная сыпь. Эта же сульфгидрильная группа вследствие легкого окисления может быть ответственна за более короткую продолжительность дейст-вия препарата.
В зависимости от особенностей метаболизма и путей элиминации, иАПФ подразделяются на три класса (Opie L., 1992):
Класс I — липофильные лекарства, неактивные метаболиты которых имеют печеночный путь выведения (каптоприл).
Класс II — липофильные пролекар-ства:
- Подкласс IIА — препараты, активные метаболиты которых выводятся преимущественно через почки (квинаприл, эналаприл, периндоприл и др.).
- Подкласс IIВ — препараты, активные метаболиты которых имеют печеночный и почечный пути элиминации (фозиноприл, моэксиприл, рамиприл, трандолаприл).
Класс III — гидрофильные лекар-ства, не метаболизирующиеся в организме и выводящиеся почками в неизмененном виде (лизиноприл).
Большинство иАПФ (исключение — каптоприл и лизиноприл) являются пролекарствами, биотрансформация которых в активные метаболиты происходит главным образом в печени, в меньшей мере — в слизистой оболочке желудочно-кишечного тракта и внесосудистых тканях. В связи с этим у больных с печеночной недостаточностью образование активных форм иАПФ из пролекарств может существенно снижаться. Ингибиторы АПФ в виде пролекарств отличаются от неэстерифицированных препаратов несколько более отсроченным началом действия и увеличением продолжительности эффекта.
По продолжительности клинического эффекта иАПФ делятся на препараты:
- короткого действия, которые необходимо назначать 2-3 раза в сутки (каптоприл);
- средней продолжительности дейст-вия, которые необходимо принимать 2 раза в сутки (эналаприл, спираприл, беназеприл);
- длительного действия, которые в большинстве случаев можно принимать 1 раз в сутки (квинаприл, лизиноприл, периндоприл, рамиприл, трандолаприл, фозиноприл и др.).
Гемодинамические эффекты иАПФ связаны с влиянием на сосудистый тонус и заключаются в периферической вазодилатации (cнижение пред- и постнагрузки на миокард), снижении общего периферического сопротивления сосудов и системного АД, улучшении регионарного кровотока. С ослаблением воздействия АII на системную и внутрипочечную гемодинамику связаны кратковременные эффекты иАПФ.
Долгосрочные эффекты обусловлены ослаблением стимулирующих эффектов АII на рост, пролиферацию клеток в сосудах, клубочках, канальцах и интерстициальной ткани почек при одновременном усилении антипролиферативных эффектов.
Важным свойством иАПФ является их способность оказывать органопротекторные эффекты , обусловленные устранением трофического действия АII и снижением симпатического влияния на органы-мишени, а именно:
- кардиопротекторное действие: регрессия миокарда левого желудочка, замедление процессов ремоделирования сердца, антиишемическое и антиаритмическое действие;
- ангиопротекторное действие: усиление эндотелийзависимой вазодилатации, торможение пролиферации гладкой мускулатуры артерий, цитопротекторное действие, анти-тромбоцитарный эффект;
- нефропротекторное действие: увеличение натрийуреза и уменьшение калийуреза, снижение внутриклубочкового давления, торможение пролиферации и гипертрофии мезангиальных клеток, эпителиальных клеток почечных канальцев и фибробластов. Ингибиторы АПФ превосходят другие антигипертензивные средства по нефропротекторной активности, которая, по крайней мере, частично, не зависит от их антигипертензивного эффекта.
Преимуществом иАПФ перед некоторыми другими классами антигипертензивных лекарственных средств являются их метаболические эффекты, заключающиеся в улучшении метаболизма глюкозы, повышении чувст-вительности периферических тканей к инсулину, антиатерогенных и противовоспалительных свойствах.
В настоящее время накоплены данные о результатах многочисленных контролируемых исследований, подтверждающих эффективность, безопасность и возможность благоприятных защитных эффектов долгосрочной терапии иАПФ у больных с сердечно-сосудистыми заболеваниями в отношении органов-мишеней.
Ингибиторы АПФ характеризуются хорошим спектром переносимости. При их приеме могут возникать специфические (сухой кашель, «гипотония первой дозы», нарушение функ-ции почек, гиперкалиемия и ангионевротический отек) и неспецифические (нарушение вкуса, лейкопения, кожная сыпь и диспепсия) побочные эффекты.
На кафедре клинической фармакологии и фармакотерапии факультета послевузовского профессионального образования врачей ММА им. И. М. Сеченова накоплен большой опыт изучения различных иАПФ у больных АГ, в том числе при сочетании ее с другими заболеваниями внутренних органов.
Особого внимания заслуживают иАПФ пролонгированного действия лизиноприл и фозиноприл. Первый из них — активный препарат, который не подвергается биотрансформации и выводится почками в неизмененном виде, что имеет значение у больных с заболеваниями желудочно-кишечного тракта и печени. Второй препарат (фозиноприл) имеет активные липофильные метаболиты, позволяющие ему хорошо проникать в ткани, обеспечивая максимальную органопротекторную активность препарата. Двойной путь (печеночный и почечный) элиминации метаболитов фозиноприла имеет значение у больных с почечной и печеночной недостаточностью. Накоплены результаты многочисленных клинических исследований, продемонстрировавших эффективность, хорошую переносимость, безопасность и возможность улучшения прогноза заболевания у больных АГ ( ).
Эффективность и переносимость лизиноприла у больных АГ
Препараты лизиноприла, имеющие-ся в аптечной сети РФ, представлены в .
Антигипертензивная эффективность и переносимость иАПФ лизиноприла в суточной дозе 10-20 мг изучена у 81 больного АГ I-II степени, в том числе в сочетании с хроническими обструктивными заболеваниями легких (ХОБЛ). Лизиноприл применялся в таблетках по 10 и 20 мг. Начальная доза составила 10 мг однократно в сутки. При недостаточной антигипертензивной эффективности по данным амбулаторных измерений АД доза лизиноприла повышалась до 20 мг однократно в сутки; в дальнейшем при необходимости дополнительно назначали гидрохлортиазид по 25 мг/сут (однократно утром). Продолжительность лечения — до 12 нед.
Всем больным проводилось суточное мониторирование АД (СМАД) с использованием осциллометрических регистраторов Schiller BR 102 по общепринятой методике. По данным СМАД рассчитывали усредненные показатели систолического АД (САД) и диастолического АД (ДАД) в дневные и ночные часы, частоты сердечных сокращений (ЧСС). Вариабельность АД оценивали по стандартному отклонению варьирующей величины. Для оценки суточных изменений АД рассчитывали степень ночного снижения АД, равную процентному отношению разницы среднедневного и средненочного уровня АД к среднедневному. В качестве показателей нагрузки давлением оценивали процент гипертонических величин АД в различные периоды суток (в период бодрствования — более 140/90 мм рт. ст., в период сна — более 125/75 мм рт. ст.).
Критериями хорошей антигипертензивной эффективности лизиноприла служили: снижение ДАД до 89 мм рт. ст. и менее и нормализация среднесуточного ДАД по результатам СМАД; удовлетворительной — снижение ДАД на 10 мм рт. ст. и более, но не до 89 мм рт. ст.; неудовлетворительной — при снижении ДАД менее чем на 10 мм рт. ст.
По данным опроса, осмотра, лабораторных и инструментальных (ЭКГ, исследование функции внешнего дыхания — ФВД) методов исследования у всех больных оценивалась индивидуальная переносимость и безопасность лизиноприла, анализировалась частота развития и характер побочных реакций, время их возникновения в процессе долгосрочной терапии.
Переносимость препаратов оценивалась как хорошая при отсутствии побочных эффектов; удовлетворительная — при наличии побочных эффектов, не потребовавших отмены препарата; неудовлетворительная — при наличии побочных явлений, потребовавших отмены препарата.
Статистическая обработка результатов проводилась с использованием программы Еxcel. Достоверность измерений оценивалась по парному t-критерию Стьюдента при р < 0,05.
На фоне монотерапии лизиноприлом в суточной дозе 10 мг антигипертензивный эффект был отмечен у 59,3% больных. При увеличении дозы лизиноприла до 20 мг/сут эффективность составила 65,4%.
По данным СМАД при длительной непрерывной терапии наблюдалось достоверное снижение среднесуточного АД и показателей гипертонической нагрузки. Снижение показателей гипертонической нагрузки является немаловажным, если принимать во внимание подтвержденную прогностическую значимость этих показателей в отношении поражения органов-мишеней, включая гипертрофию миокарда левого желудочка. Сопоставление результатов, полученных при СМАД, через 4 и 12 нед терапии позволяет сделать вывод о том, что при долгосрочной терапии лизиноприлом не наблюдается развития толерантности к препарату и снижения его антигипертензивной эффективности.
Важным является то, что на фоне терапии лизиноприлом увеличилось число лиц с нормальным суточным профилем АД, значительно снизилось количество больных с профилем АД типа non-dipper. Ни у одного больного не отмечалось чрезмерного снижения САД или ДАД в ночные часы.
Переносимость терапии лизиноприлом в целом была хорошей. У большинства больных на фоне лечения улучшалось самочувствие: уменьшились головные боли, повысилась толерантность к физическим нагрузкам, улучшилось настроение, что свидетельствует о повышении качест-ва жизни больных. Сухой кашель был отмечен в 11,1% случаев, диспепсия — в 1,2%, преходящие умеренные голов-ные боли — в 4,9%. Отмена препарата из-за плохой переносимости потребовалась в 2,4% случаев.
Клинически значимых изменений по данным лабораторных методов исследования на фоне терапии лизиноприлом не отмечено.
Для больных АГ в сочетании с ХОБЛ важным является факт отсутствия негативного влияния антигипертензивных средств на показатели ФВД. Ухудшения показателей ФВД не отмечено, что свидетельствует об отсутствии негативного влияния препарата на тонус бронхов.
Итак, лизиноприл в суточной дозе 10-20 мг характеризуется хорошей переносимостью, низкой частотой побочных эффектов, отсутствием влияния на процессы метаболизма, благоприятным действием на суточный профиль АД. Возможность применения лизиноприла 1 раз в день повышает приверженность больных к терапии и снижает стоимость лечения.
Эффективность и переносимость фозиноприла у больных АГ
Торговые названия препаратов фозиноприла, доступных в аптечной сети РФ, представлены в .
Антигипертензивная эффективность и переносимость иАПФ фозиноприла в суточной дозе 10-20 мг была изучена у 26 больных АГ I-II степени. Фозиноприл применялся в таблетках по 10 и 20 мг. Начальная доза составила 10 мг однократно в сутки с последующим повышением до 20 мг/сут при недостаточной антигипертензивной эффективности по данным амбулаторных измерений АД. В дальнейшем при необходимости дополнительно назначали гидрохлортиазид по 25 мг/сут (однократно утром). Продолжительность лечения составила 8 нед.
Методы оценки эффективности и переносимости длительного лечения больных мягкой и умеренной АГ фозиноприлом были сравнимы с методами, перечисленными выше в исследовании лизиноприла.
СМАД проводилось больным с использованием портативных регистраторов TONOPORT IV, осуществляющих регистрацию АД, либо аускультативным, либо осциллометрическим методом до начала лечения и через 8 нед терапии фозиноприлом по общепринятой методике и с последующим анализом полученных результатов.
На фоне терапии фозиноприлом через 2 нед антигипертензивный эффект был отмечен у 15 (57,7%) больных: у 5 (19,2%) — АД нормализовалось, у 10 (38,5%) — ДАД снизилось более чем на 10% от исходного уровня. Недостаточную эффективность антигипертензивной терапии наблюдали у 11 больных (42,3%), что послужило поводом для увеличения первоначальной дозы фозиноприла. Через 8 нед монотерапии фозиноприлом нормализация ДАД была отмечена у 15 (57,7%) больных. Комбинированная терапия фозиноприлом и гидрохлортиазидом позволила достаточно контролировать АД еще у 8 (30,8%) больных. Неудовлетворительный эффект отмечен у 3 (11,6%) больных. По нашим данным, эффективность монотерапии фозиноприлом зависела от длительности и степени АГ. Так, в группе с низкой эффективностью монотерапии преобладали пациенты с более длительным анамнезом АГ.
По данным СМАД терапия фозиноприлом у больных АГ в течение 2 мес приводила к достоверному уменьшению среднесуточных показателей САД и ДАД без изменения ЧСС. Характер суточных кривых АД после лечения фозиноприлом не изменился. Показатели нагрузки «гипертоническими» величинами в период бодрствования достоверно снизились: для САД — на 39%, для ДАД — на 25% (p < 0,01). В период сна данные показатели уменьшились на 27,24 и 23,13% соответственно (p < 0,01).
В процессе лечения фозиноприлом у больных зарегистрированы следующие побочные эффекты: изжога при приеме фозиноприла в дозе 10 мг на 7-е сутки лечения — у одного больного (3,9%); головокружение и слабость через 1-2 ч после первого приема 10 мг фозиноприла — у одного больного (3,9%); головная боль, слабость после увеличения дозы фозиноприла до 20 мг — у одного больного (3,9%); крапивница, зуд кожных покровов, развившиеся на 11-й день лечения фозиноприлом в дозе 10 мг — у одной больной (3,9%). Эти побочные эффекты, за исключением последнего случая, не потребовали отмены фозиноприла. Жалобы на изжогу отмечены у одного пациента, принимавшего 10 мг фозиноприла утром натощак. После изменения времени приема препарата (после завтрака) изжога больного не беспокоила.
Анализ безопасности терапии фозиноприлом свидетельствует об отсутст-вии клинически значимых изменений функции почек и печени на фоне терапии фозиноприлом.
Результаты нашего исследования согласуются с данными многочисленных контролируемых исследований эффективности и переносимости терапии фозиноприлом в суточной дозе 10-20 мг и в сочетании с гидрохлортиазидом у больных АГ.
Поиск индивидуального подхода к лечению АГ остается актуальной проблемой кардиологии.
Для практикующего врача важно уметь правильно применить тот или иной препарат в той или иной клинической ситуации. Пролонгированные иАПФ удобны для длительного лечения больных АГ, так как возможность однократного приема препарата в сутки значительно повышает приверженность больных к выполнению назначений врача.
Результаты многочисленных исследований показали, что комбинация иАПФ с диуретиком (либо гипотиазид, либо индапамид) позволяет увеличить эффективность антигипертензивной терапии, особенно у больных с умеренной и выраженной АГ, без ухудшения ее переносимости, при этом возможно снижение суточных доз обоих препаратов.
Достоинствами иАПФ являются мягкое постепенное снижение АД без резких колебаний антигипертензивного эффекта в сочетании с широким спектром органопротекторных эффектов и положительным влиянием на степень сердечно-сосудистого риска.
По вопросам литературы обращайтесь в редакцию.
Ж. М. Сизова
,
Т. Е. Морозова
, доктор медицинских наук, профессор
Т. Б. Андрущишина
ММА им. И. М. Сеченова, Москва
3
1 ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), Москва
2 ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России, Москва
3 KГМА - филиал ФГБОУ ДПО РМАНПО Минздрава России, Казань
Для цитирования:
Ермолаева А.С., Дралова О.В., Максимов М.Л. Ингибитор АПФ третьего поколения фозиноприл в лечении пациентов с сердечно-сосудистыми заболеваниями // РМЖ. 2014. №12. С. 906
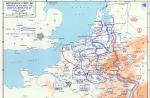
Сердечно-сосудистые заболевания являются основной причиной смерти вЕвропе исоставляют более 4,3млн смертей ежегодно. Артериальная гипертензия (АГ) относится кчислу наиболее распространенных сердечно-сосудистых заболеваний (около 40% взрослого населения РФимеют повышенный уровень АД) иявляется важнейшим фактором риска развития основных сердечно-сосудистых осложнений, таких как инфаркт миокарда иострое нарушение мозгового кровообращения, определяющих высокую смертность виндустриально развитых странах .
Ренин-ангиотензин-альдостероновая система (РААС) рассматривается как основной фактор регуляции АД и гомеостаза, играет центральную роль в возникновении АГ и ее последствий, выступает в качестве непременного участника сердечно-сосудистого континуума, начиная с этапа воздействия факторов риска, потенциирования развития атеросклероза, эндотелиальной дисфункции, ишемической болезни сердца (ИБС), гипертрофии ЛЖ, ремоделирования миокарда и завершая финальной сердечной недостаточностью, а также развитием хронической болезни почек (ХБП) .
В настоящее время для лечения АГ рекомендованы 5 основных классов антигипертензивных препаратов: ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов ангиотензина II (БРА), блокаторы медленных кальциевых каналов (БМКК), b-адреноблокаторы (БАБ), диуретики . На фоне антигипертензивной терапии возможно изменение активности РААС. Одним из путей снижения ее активности является подавление синтеза ангиотензина II .
иАПФ представляют собой высокоэффективные препараты, широко используемые в лечении сердечно-сосудистых заболеваний: АГ, ИБС, хронической сердечной недостаточности (ХСН). Актуальность их применения в практике лечения заболеваний сердечно-сосудистой системы обусловлена эффектами блокады нейрогуморальных систем, вазо-, кардио- и нефропротективными свойствами .
В течение последних лет неуклонно растет количество иАПФ, дифференцирующихся по фармакокинетическим свойствам, продолжительности действия, активности исходного препарата и степени тканевой биодоступности. По химическому строению препараты различаются по тому, какая химическая группа (сульфгидрильная, карбоксиалкильная, фосфинильная или гидроксамовая) в их молекуле связывается с ионом цинка в активных центрах ангиотензинпревращающего фермента .
В основе клинически значимых фармакологических эффектов иАПФ лежит их способность подавлять активность фермента (АПФ или кининаза II), превращающего ангиотензин I в. ангиотензин II, и таким образом влиять на функционирование РААС. Ангиотензин II считается основным эффекторным звеном РААС . Ангиотензин II, активируя АТ1-рецепторы, обладает мощным вазоконстрикторным действием. Под воздействием ангиотензина II происходит сокращение гладкомышечных клеток, усиливается сократимость миокарда, повышается продукция альдостерона, а также экскреция катехоламинов из мозгового вещества надпочечников и симпатических нервных окончаний. Ангиотензин II также регулирует транспорт натрия с помощью эпителиоцитов кишечника и почек. В дополнение к физиологическим функциям локально продуцированный ангиотензин II вызывает воспаление, пролиферацию клеток, митоз, апоптоз, миграцию и дифференцирование клеток, регулирует генную экспрессию биоактивных веществ и активирует множественные внутриклеточные сигнальные пути, многие из которых способствуют повреждению тканей .
иАПФ снижают секрецию альдостерона и вазопрессина, препятствуют разрушению брадикинина. Брадикинин, накапливаясь в эндотелии, действуя через β 2-рецепторы брадикинина, вызывает релаксацию гладких мышц сосудов и способствует высвобождению зависимого от эндотелия релаксирующего фактора и вазоактивных простагландинов (простациклина и простагландина Е2). Кроме того, под влиянием иАПФ снижается синтез других сосудосуживающих и антинатрийуретических веществ (норадреналина, аргинина-вазопрессина, эндотелина-1), участвующих в патогенезе кардиальной дисфункции и АГ. Основные органопротективные эффекты иАПФ обусловлены блокадой АПФ в различных тканях (например, сосудах, почках, сердце) .
Различают следующие основные фармакологические эффекты иАПФ: гемодинамические, нейрогуморальные, антипролиферативные, почечные и др. .
Гемодинамический эффект иАПФ реализуется через их способность снижать общее периферическое сосудистое сопротивление, вызывать натрийурез, однако влияние на ЧСС невелико. Уменьшение тонуса периферических сосудов также происходит в результате блокады тканевого АПФ, что приводит к уменьшению содержания ангиотензина II в. органах-мишенях (например, сосудистой стенке). У пациентов с нормальным и повышенным АД без сердечной недостаточности иАПФ практически не влияют на минутный объем сердца и ударный объем. В отличие от других вазодилататоров иАПФ не вызывают рефлекторной тахикардии, по-видимому, за счет воздействия на барорецепторы, усиления парасимпатической активности и, возможно, уменьшения симпатической активности. Также не происходит изменений ЧСС во время физической нагрузки. Применение иАПФ улучшает способность кардиомиоцитов к релаксации. иАПФ уменьшают гипертрофию левых отделов сердца у пациентов с ИБС, АГ, страдающих инсулинонезависимым сахарным диабетом (СД) и сердечной недостаточностью. Также иАПФ уменьшают эндотелиальную дисфункцию. Данное свойство связывают с ослаблением вазоконстрикции и усилением выработки оксида азота в результате увеличения образования брадикинина при блокаде АПФ .
У пациентов с ХСН иАПФ улучшают клиническую симптоматику, качество жизни, замедляют прогрессирование болезни и улучшают прогноз, а также предотвращают наступление клинически выраженной декомпенсации. Это обусловлено их способностью вызывать как артериальную, так и венозную вазодилатацию. Венозная вазодилатация повышает емкость венул, уменьшает нагрузку на правое предсердие, вследствие этого уменьшается давление в легочной вене, снижается нагрузка объемом левого желудочка и уменьшается застой по малому кругу кровообращения .
Артериальная вазодилатация приводит к уменьшению периферического сосудистого сопротивления и увеличению сердечного выброса. Короткий курс приема иАПФ сопровождается уменьшением содержания ангиотензина II, однако по механизму отрицательной обратной связи увеличивается выброс ренина и уровень ангиотензина I. Ангиотензин II обладает мощным вазоконстрикторным действием на мускулатуру гладкомышечных клеток, усиливает сократимость миокарда, стимулирует продукцию альдостерона, активирует экскрецию катехоламинов из мозгового вещества надпочечников и из симпатических нервных окончаний, стимулирует симпатическую нервную систему, усиливает жажду и желание употреблять соленую пищу. Также ангиотензин II регулирует транспорт натрия с помощью эпителиоцитов кишечника и почек. Кроме того, иАПФ уменьшают содержание в плазме эпинефрина, норэпинефрина и вазопрессина .
Помимо этого, к повышению уровня ангиотензина I приводит увеличение концентрации брадикинина, а также активация альтернативных путей превращения ангиотензина I в. ангиотензин II. Таким образом, применение иАПФ повышает уровень кининов, простациклина и окиси азота. При длительном применении иАПФ уменьшается выработка альдостерона, в норме стимулируемая гиперкалиемией, гипермагниемией и АКТГ, что приводит к усилению выведения натрия и воды .
При длительном применении иАПФ возникает антипролиферативный эффект: снижение гипертрофии мышечного слоя сосудистой стенки и миокарда, уменьшение пролиферации внеклеточного матрикса. Возможными механизмами действия иАПФ на уменьшение гипертрофии миокарда считаются: механическая причина за счет уменьшения преднагрузки и постнагрузки, а также уменьшение симпатической активности и снижение стимуляции роста. Кроме того, иАПФ уменьшают образование коллагена за счет уменьшения содержания ангиотензина II, который действует как непосредственно на фибробласты, так и косвенно за счет стимуляции секреции альдостерона. Торможение роста и пролиферации гладкомышечных клеток и фибробластов в медии артерий приводит к увеличению их просвета, а также восстановлению и улучшению эластичности артериальной стенки. Таким образом, нормализуется центральная гемодинамика и снижается периферическое сосудистое сопротивление .
Известны относительно новые данные по объяснению антифибротического действия иАПФ на миокард при АГ. Исследователи считают, что этот эффект иАПФ является результатом блокады гидролиза N-ацетил-серил- аспартил-лизил-пролина, приводящей к уменьшению пролиферации фибробластов, воспалительных клеток, экспрессии трансформирующего фактора роста и отложению коллагена. Помимо этого, иАПФ препятствуют апоптозу кардиомиоцитов .
иАПФ оказывают благоприятный эффект на почки, т. к. расширяют преимущественно эфферентные артериолы и меньше влияют на афферентные. Таким образом снижается внутриклубочковое давление, уменьшается протеинурия, увеличивается почечный кровоток с незначительным изменением скорости клубочковой фильтрации. Несмотря на уменьшение сосудистого сопротивления в клубочках, скорость клубочковой фильтрации остается неизмененной или увеличивается вместе с фильтрационной фракцией. В результате улучшения почечной гемодинамики возрастает натрийурез, уменьшается выработка альдостерона, что приводит к замедлению прогрессирования нефропатии .
РААС играет важную роль в патогенезе и прогрессировании атеросклероза. Таким образом, при назначении иАПФ замедляется развитие атеросклероза вследствие блокады образования ангиотензина II и увеличения концентрации брадикинина и оксида азота, которые улучшают эндотелиальную функцию .
В опубликованном сравнительном анализе трех исследований (HOPE, EUROPA, PEACE) по влиянию иАПФ у 29 805 пациентов с наличием атеросклероза, но без дисфункции левого желудочка, на показатели общей смертности, фатальных и нефатальных сердечно-сосудистых событий показано, что назначение иАПФ приводит к достоверному снижению общей (7,8 против 8,9%, p=0,0004) и сердечно-сосудистой (4,3 против 5,2%, p=0,0002) смертности, нефатальных инфарктов миокарда (5,3 против 6,4%, p=0,0001), мозговых инсультов (2,2 против 2,8%, p=0,0004), сердечной недостаточности (2,1 против 2,7%, p=0,0007) и проведению аортокоронарного шунтирования (6,0 против 6,9%, p=0,0036). Авторы заключили, что назначение иАПФ должно быть рассмотрено у всех пациентов с промежуточным риском при наличии атеросклеротического процесса .
Таким образом, иАПФ показаны для лечения АГ (класс IA). У больных АГ первичной целью лечения является контроль АД, который может быть достигнут с помощью различных препаратов, снижающих риск сердечно-сосудистых осложнений при длительной терапии. иАПФ рассматривают также в качестве средств первой линии у больных с сердечной недостаточностью, систолической дисфункцией левого желудочка или СД, перенесших ИМ или инсульт, а также у пациентов группы высокого риска коронарной болезни сердца .
За последние десятилетия исследованы более 30 химических соединений, относящихся к классу иАПФ. Одним из наиболее эффективных, безопасных и экономичных иАПФ является фозиноприл натрия (Моноприл). Клинически важным отличием фозиноприла от многих других иАПФ является наличие в его химической формуле остатков фосфинильной кислоты. Эта особенность структуры придает препарату ряд уникальных свойств, отличающих его от других препаратов данного класса, и позволяет отнести его к третьей, наиболее современной, генерации иАПФ .
Фозиноприл является пролекарством и действует после всасывания и трансформации (в печени, слизистой ЖКТ, почках, кровяном русле) в активный метаболит — фозиноприлат, который связывается с белками плазмы крови (95-98%). Период полувыведения фозиноприла составляет 12-15 ч, что обусловливает его длительное антигипертензивное действие и прием 1 р./сут. Препарат отличается чрезвычайно высокой липофильностью — индекс липофильности фозиноприлата составляет более 2,0 ЕД, тогда как у эналаприлата — 0,108 ЕД. Это облегчает проникновение фозиноприлата через клеточные мембраны и позволяет подавлять активность не только циркулирующей, но и тканевой РААС в сердце, легких, почках и головном мозге. Экспериментально показано, что фозиноприлат ингибирует АПФ в сердечной мышце в большей степени, чем рамиприлат и эналаприлат, что лежит в основе более выраженного (по сравнению с другими иАПФ) гипотензивного и кардиопротективного эффектов. В отличие от других иАПФ (каптоприла, эналаприла, лизиноприла и др.), которые выводятся из организма преимущественно почками, для фозиноприла характерны два основных пути элиминации — почечный и печеночный (с желчью) в соотношении 1:1. Причем при снижении функции почек увеличивается выведение активного метаболита с желчью и, наоборот, при печеночной недостаточности возрастает его экскреция с мочой . Это делает препарат наиболее эффективным у пожилых, а также у пациентов с патологией печени и почек.
Клинически значимым преимуществом фозиноприла, отличающим его от большинства других иАПФ, является хорошая переносимость. Так, у больных с ХСН II-IV функционального класса по классификации NYHA частота побочных эффектов при применении фозиноприла и плацебо практически не отличалась. Отмечается крайне низкая частота возникновения сухого кашля. Отмечено, что сухой кашель, вызываемый другими иАПФ, ослабевает или даже полностью исчезает при переходе на фозиноприл. Так, в двойном слепом сравнительном исследовании с эналаприлом показано достоверно более редкое возникновение кашля при назначении фозиноприла. В это исследование были включены 179 больных, уже прекративших прием иАПФ из-за развития кашля. Попытка возобновления лечения была гораздо более успешной при выборе фозиноприла — повторное развитие кашля наблюдалось более чем вдвое реже по сравнению с эналаприлом. Также при его применении наблюдается меньшее число клинических и биохимических побочных эффектов, особенно в «группах риска» — у пожилых гипертоников или больных СД. Фозиноприл отличает и удобный режим дозирования — однократный прием обеспечивает 24-часовой контроль АД (соотношение остаточного к пиковому эффекту — 64%) и предотвращает его повышение в ранние утренние часы. Начальная суточная доза фозиноприла при АГ составляет 10 мг однократно с возможным последующим увеличением до 20-40 мг. При ХСН начальная суточная доза — 5-10 мг (у больных с гипотонией — 2,5-5 мг), средняя терапевтическая — 10-20 мг, максимальная — 20-40 мг .
В исследовании FOPS (757 больных старше 60 лет) целевой уровень АД за 12 нед. лечения фозиноприлом был достигнут у 80% пациентов, причем части из них дополнительно назначали 12,5 мг гидрохлоротиазида для достижения лучшего терапевтического результата. В исследовании FLIGHT (19 432 больных с АГ, 989 из них — старше 75 лет) через 12 нед. от начала лечения целевое АД было достигнуто у 79,8% пациентов. Отмечено, что антигипертензивная активность фозиноприла постепенно возрастает в первые несколько недель лечения, АД чаще достигает целевых уровней без проявления элементов компенсаторных нарушений сердечного ритма, а отмена препарата не приводит к быстрому подъему АД. Действие фозиноприла, как правило, не зависит от возрастно-половых особенностей и массы тела больных .
При проведении российской программы ФЛАГ (Фозиноприл при Лечении Артериальной Гипертонии) оценивалась вероятность достижения целевых уровней АД у больных с мягкой и умеренной АГ в амбулаторных условиях при монотерапии фозиноприлом (10-20 мг/сут) или его сочетании с гидрохлоротиазидом. Всего в исследование были включены 2557 пациентов, из которых 26,7% составили лица старше 60 лет. Целевое АД достигнуто у 62,1% пациентов. Побочные эффекты отмечены у 8,3% больных, причем только у 5,2% потребовалась отмена препаратов .
В исследование ФАГОТ (Фармакоэкономическая оценка использования иАПФ фозиноприла в амбулаторном лечении больных Артериальной Гипертензией Осложненного Течения) были включены 2596 пациентов с мягкой или умеренной АГ и наличием двух факторов риска сердечно-сосудистых осложнений. Сравнивалась эффективность монотерапии фозиноприлом или его сочетания с гидрохлоротиазидом и общепринятой терапии (диуретиками, БАБ, антагонистами кальция) у пациентов разного возраста. Целевое АД при приеме фозиноприла и гидрохлоротиазида достигнуто у 67,8% пациентов. Показано, что скорость достижения гипотензивного эффекта и его выраженность при применении фозиноприла не различаются у пациентов пожилого и молодого возраста, но выше, чем при использовании традиционной схемы лечения. По сравнению с другими препаратами фозиноприл выгодно отличала простота приема и затратная экономичность .
Фозиноприл является эффективным в предупреждении и обратном развитии гипертрофии левого желудочка (ЛЖ) при АГ, т. е. он не только снижает АД, но и способствует регрессу структурного ремоделирования камер сердца. В течение 9 мес. масса миокарда ЛЖ снижается у лиц с выраженной гипертрофией на 5 г, а в группе сравнения — нарастает. Подобное наблюдение очень важно, поскольку гипертрофия стенки ЛЖ — один из ключевых предикторов сердечно-сосудистых катастроф. Препарат также благоприятно воздействует на течение атеросклероза сонных артерий. Показано, что толщина комплекса интима-медиа в этом участке сосудистого русла через 36 нед. регулярного приема препарата снижается на 0,0278±0,03 мм, в то время как вне приема фозиноприла данный показатель только увеличивается.
Результаты двойного слепого плацебо-контролируемого исследования PHYLLIS продемонстрировали тормозящий эффект терапии фозиноприлом (20 мг/сут) на прогрессирование атеросклероза сосудов каротидного бассейна, т. е. антиатерогенное действие. В исследовании участвовали 508 больных АГ с бессимптомным атеросклеротическим поражением сонных артерий и их крупных ветвей. Средний срок наблюдения составил 2,6 года. Толщина комплекса интима-медиа, как и зона атеросклеротического поражения, у больных, принимавших фозиноприл, достоверно и сходно уменьшалась. Таким образом, уже в нескольких исследованиях продемонстрировано, что фозиноприл оказывает антиатерогенное действие у больных АГ, по крайней мере на отдельных участках сосудистого русла .
Фозиноприл также способен улучшать диастолическую функцию ЛЖ у молодых лиц с мягкой АГ без гипертрофии стенки ЛЖ. В исследовании приняли участие 66 молодых людей (средний возраст 36 лет) со средней продолжительностью АГ, согласно медицинской документации, 5,4 года. Доза фозиноприла составила 20 мг/сут. Группа контроля получала комбинацию гидрохлоротиазида и гидралазина. Монотерапия фозиноприлом продемонстрировала неоспоримые преимущества в нормализации диастолической функции ЛЖ и профилактике гипертрофии ЛЖ .
Для подтверждения собственного нефропротективного эффекта фозиноприла, не связанного со снижением АД, проведено исследование PREVEND IT (Prevention of Renal Vascular End-Stage Disease Intervention Trial). Исследование включало 854 пациента с микроальбуминурией, которым назначали 2 препарата в течение 46 мес.: правастатин и фозиноприл, каждый из которых имел плацебо-контроль. Основной целью данного исследования была оценка влияния фозиноприла и правастатина на сердечно-сосудистые осложнения и почечную недостаточность у больных с микроальбуминурией, нормальным уровнем АД и общего холестерина. За первые 3 мес. уровень альбуминурии существенно снизился у больных, получавших фозиноприл, что сохранялось на протяжении 4 лет наблюдения. Применение правастатина не сопровождалось изменением микроальбуминурии. В сравнении с плацебо фозиноприл уменьшил риск инсульта, но не влиял на риск инфаркта миокарда .
Применение фозиноприла — длительно действующего иАПФ, характеризующегося взаимно компенсирующимися путями экскреции с мочой и желчью, — сопряжено с минимальным риском кумуляции при хронической почечной недостаточности, в т. ч. выраженной (клиренс эндогенного креатинина <30 мл/мин). Аргументом в пользу выбора именно этого препарата у больных ХСН с исходными гиперкреатининемией и/или снижением СКФ является установленный в клинических исследованиях минимальный по сравнению с другими иАПФ риск нарастания сывороточных концентраций креатинина и калия. У пожилых больных с изолированной систолической АГ (исследование FOPS), у которых вероятность провокации ухудшения функции почек иАПФ максимальна, применение фозиноприла не было сопряжено с появлением признаков почечной недостаточности. Безопасность фозиноприла с точки зрения влияния на функцию почек установлена и в крупных отечественных контролируемых исследованиях (проект «Три Ф») .
При сравнении фозиноприла и нифедипина в виде длительно действующей гастроинтестинальной терапевтической системы (ГИТС) у 241 больных с паренхиматозными заболеваниями почек и хронической почечной недостаточностью, у которых за предшествующий год наблюдалось удвоение уровня креатинина плазмы крови, проводилось лечение фозиноприлом 10-20 мг/сут в сравнении с нифедипином продленного действия 30-60 мг/сут. Конечными точками в исследовании выступали удвоение уровня креатинина и необходимость в гемодиализе. Через 3 года наблюдения 36% больных в группе, получавшей нифедипин, и 21% пациентов (p<0,05) в группе, получавшей фозиноприл, достигли конечной точки. При этом уровень протеинурии на фоне лечения фозиноприлом уменьшился на 57% от исходного, в группе терапии нифедипином — возрос на 7% .
Заключение. иАПФ фозиноприл (Моноприл) — эффективный современный препарат, который позволяет не только достичь целевого уровня АД у пациентов с АГ, но также имеет доказанные кардио-, вазо- и нефропротективные эффекты и способен тормозить атеросклеротический процесс. Фозиноприл (Моноприл) может служить препаратом выбора в качестве гипотензивной терапии АГ у лиц всех возрастных групп. Для обеспечения оптимального органопротективного эффекта фозиноприл может с успехом применяться как в монотерапии, так и в комбинации, в т. ч. с тиазидными диуретиками или антагонистами кальция. Соединяя в себе разностороннюю эффективность, хорошую переносимость и простоту использования, фозиноприл может быть рекомендован для терапии пациентов с АГ, в т. ч. в сочетании с ХБП, ИБС и ХСН.
Литература
- Диагностика и лечение артериальной гипертензии: Российские рекомендации (четвертый пересмотр) // Системные гипертензии. 2010. № 3. С. 5-26.
- Чазова И.Е., Ратова Л. Г. Комбинированная терапия артериальной гипертонии: Руководство по артериальной гипертонии / Под ред. Е. И. Чазова, И. Е. Чазовой. М.: Медиа Медика, 2005. С. 784.
- Остроумова О.Д., Максимов М. Л. Выбор комбинации ингибиторов АПФ и диуретиков в лечении артериальной гипертензии в новой редакции российских рекомендаций: фокус на лечение пожилых пациентов // Фарматека. 2011. № 8. С. 42-49.
- Кобалава Ж.Д., Котовская Ю.В., Моисеев В. С. Артериальная гипертония. Ключи к диагностике и лечению: Серия «Библиотека врача-специалиста ». М.: ГЭОТАР-Медиа, 2009. 864 с.
- Карпов Ю. А. Лечение больных сердечно-сосудистыми заболеваниями: роль блокады ренин-ангиотензиновой системы с помощью сартанов // РМЖ. 2009. № 23. С. 1548-1554.
- Мухин Н.А., Моисеев В.С., Кобалава Ж.Д. и др. Кардиоренальные взаимодействия: клиническое значение и роль в патогенезе заболеваний сердечно-сосудистой системы и почек // Тер. архив. 2004. № 6. С. 39-47.
- Медведев И.Н., Кумова Т.А., Гамолина О. В. Роль ренин-ангиотензин-альдостероновой системы в развитии артериальной гипертонии // Российский кардиологический журнал. 2009. № 4. С. 82-84.
- Jacoby D.S., Rader D. J. Renin -angiotensin system and atherothrombotic disease: from genes to treatment // Arch. Intern. Med. 2003. Vol. 163(10). P. 1155-1164.
- Остроумова О.Д., Максимов М. Л. Место ингибиторов ангиотензин-превращающего фермента в лечении артериальной гипертонии у различных групп пациентов // Кардиоваскулярная терапия и профилактика. 2010. № 9 (7). С. 90-96.
- ESH-ESC Guidelines Committee. 2013 guidelines for the management of arterial hypertension // J. Hypertens. 2013. Vol. 31. P. 1281-1357.
- Клиническая фармакология / Под ред. В. Г. Кукеса. М.: ГЭОТАР-Медиа, 2013. 1056 с.
- Чазов Е.И., Чазова И. Е. Руководство по артериальной гипертонии. М., 2005. 734 с.
- Арутюнов Г.П., Чернявская Т. К. Проблемы нефропротекции у пациентов с артериальной гипертонией. Значение показателя микроальбуминурии для врача общей практики // Качество жизни. Медицина. 2005. № 3. С. 22-27.
- Рациональная фармакотерапия сердечно-сосудистых заболеваний: Рук. для практикующих врачей / Под общ. ред. Е. И. Чазова, Ю. Н. Беленкова. М.: Литтерра, 2005. 972 с. (Рациональная фармакотерапия: Сер. рук. для практикующих врачей; Т. 6).
- Таяновская Ю.В., Лелюк В.Г., Кутузова А.Б. и др. Методология и прикладное значение исследования функции эндотелия в общеклинической практике и клинике радиационной медицины // Эхография. 2001. Т. 2, № 4. С. 384-396.
- Беленков Ю.Н., Мареев В.Ю., Агеев Ф. Т. Эндотелиальная дисфункция при сердечной недостаточности: возможности терапии ингибиторами ангиотензинпревращающего фермента // Кардиология. 2001. № 5. С. 100-104.
- Метелица В. И. Клиническая фармакология сердечно-сосудистых лекарственных средств. М.: Миа, 2005. 926 с.
- Клиническая фармакология: национальное руководство (Серия «Национальные руководства»). М.: ГЭОТАР-Медиа, 2014. 976 с.
- Stella A., Zanchetti A. Control of renal renin release // Kidney Int. 1987. Vol. 31 (Suppl. 20). P. 89-94.
- Диагностика и лечение в кардиологии: учебн. пособие для студ. медвузов / Под ред. Майкла Х. Кроуфорда; пер. с англ. яз.; под общ. ред. акад. РАМН Р. Г. Оганова. М.: МЕДпресс-информ, 2007. 800 с.
- Алмазов В.А., Беркович О.А., Ситникова М.Ю. и др. Эндотелиальная дисфункция у больных с дебютом ишемической болезни сердца в разном возрасте // Кардиология. 2001. № 5. С. 26-29.
- Griendling K.K. et al. Angiotensin II signaling in vascular smooth muscle // New concepts — Hypertension. 1997. Vol. 29. P. 366-373.
- Карпов Ю. А. Ингибиторы ангиотензинпревращающего фермента в моно- и комбинированной терапии артериальной гипертонии // РМЖ. 2009. № 18. С. 1122-1127.
- Taddei S., Virdis A., Chiadoni L., Salvetti A. The role of endothelium in human hypertension // Curr. Opin. Nephrol. Hypertens. 1998. № 7. Р. 20-39.
- Ратманова А. Ингибиторы РААС в нефропротекции. Целесообразна ли комбинация ингибиторов АПФ и БРА? // Med. Review. 2008. № 3 (03). С. 74-80.
- Freedman J.E., Loscalzo J. Nitric oxide and its relationship to thrombotic disorders // J. Thromb. Haemost. 2003. Vol. 1(6). Р. 1183-1188.
- Шишкин А.Н., Лындина М. Л. Эндотелиальная дисфункция и артериальная гипертензия // Артериальная гипертензия. 2008. Т. 14. № 4. С. 315-319.
- Преображенский Д.В., Маревич А.В., Романова Е.И. и др. Микроальбуминурия: диагностическое, клиническое и прогностическое значение (часть вторая) // Российский кардиологический журнал. 2000. № 4. С. 78-85.
- С. А. Бойцов, А. М. Уринский, Р. Л. Кузнецов, Ю. М. Поздняков Структура факторов риска, поражений органов-мишеней и метаболических изменений у больных артериальной гипертензией в различных возрастных группах — Кардиология. — 2009. — № 4. — С. 19-24.
- Белоусов Ю.Б., Леонова М.В., Тарасов А.В. и др. Оценка органопротективных эффектов современных антигипертензивных препаратов // Вестник РГМУ. 2006. № 4 (51). С. 22-27.
- Преображенский Д.В., Савченко М.В., Кектев В.Г., Сидоренко Б. А. Фозиноприл — первый представитель нового поколения ингибиторов ангиотензинпревращающего фермента // Кардиология. 2000. № 5. C. 75-81.
- Краснова Е. А. Фозиноприл в лечении артериальной гипертензии // РМЖ. 2006. № 4.
- Отрохова Е. В. Фозиноприл в лечении и профилактике хронической сердечной недостаточности у больных артериальной гипертензией: проблема оптимального выбора ингибитора ангиотензинпревращающего фермента // Фарматека. 2006. № 20. С. 28-32.
- Агеев Ф.Т., Мареев В. Ю. Моноприл (фозиноприл) в лечении сердечно-сосудистых заболеваний // РМЖ. 2000. Т. 8. С. 11-16.
- Geluk C.A., Asselbergs F.W., Hillege H.L. et at. Impact of statins in microalbuminuric subjects with the metabolic syndrome: a substudy of the PREVEND Intervention Trial // Eur. Heart J. 2005. Vol. 26(13). P. 1314-1320.
- Huang K., Dai G. The effect and mechanism of forsinopril on ventricular hypertrophy of SHR and left ventricular pressure overloading rat // J. Huazriong. Univ. Sci Technolog. Med. Sci. 2002. Vol. 22. P. 17-20.
- Hui K.K., Duchin K.L., Kripalani K. et al. Pharmacokinetics of fosinopril in patients with various degrees of renal function // Clin. Pharmacol. Ther. 1991. Vol. 49. P. 457-467.
- Ford N.F. et al. Single-dose and steady-state pharmacokinetics of fosinopril and fosinoprilat in patients with hepatic impairment // J. Clin. Pharmacol. 1995. Vol.35. P. 145-150.
- Deedwania P. C. Clinical profile of fosinopril, a novel phosphinic acid ACE inhibitor, for the treatment of heart failure // Heart Failure. 1995. Vol. 11. P. 3.
- Levinson B., Graney W.F., DeVault A.R. et al. Age is not reason for dose adjustment for fosinopril in hypertension. // Am. J. Hypertens. 1989. Vol. 2 (pt2). 8A.
- Tatti P., Pahor M., Byington R.P. et al. Outcome results of the fosinipril vs amlodipine cardiovascular events randomized trial (FACET) in patients with hypertension and NIDDM // Diabetes Care. 1998. Vol. 21. P. 597-603.
- Стуров Н. В. Место ингибитора АПФ фозиноприла в лечении артериальной гипертонии // Трудный пациент. 2007. № 2.
- Vetter W. Treatment of senile hypertension: the Fosinopril in Old Patients Study (FOPS) // AJH. 1997. Vol. 10. S. 255-261.
- Berdah J., Guest M., Salvador M. Study of the efficacy and safety of fosinopril in general practice in 19,435 hypertensive patients (FLIGHT Study) // Ann. Cardiol. Angiol. 1998. Vol. 47(3). P. 169-175.
- Карпов Ю. А. Фозиноприл при лечении артериальной гипертонии (ФЛАГ): российская программа оценки практической достижимости целевых уровней артериального давления // РМЖ. 2001. Т. 9. № 10. С. 406-410.
- Чазова И. Е. Первые результаты исследования ФАГОТ // Consihum Medicum. 2002. Т. 4. № 11. С. 596-598.
- Tasic I.S., Mijalkovic D., Djordjevic D. et al. Effect of fosinopril on progression of the asymptomatic carotid atherosclerosis and left ventricular hypertrophy in hypertensive patients // Srp. Arh. Celok. Lek. 2006. Vol. 134(3-4). P. 106-113.
- Zanchetti A., Crepaldi G., Bond M.G. et al. Different effects of antihypertensive regimens based on fosinopril or hydrochlorothiazide with or without lipid lowering by pravastatin on progression of asymptomatic carotid atherosclerosis: principal results of PHYLLIS- a randomized double-blind trial // Stroke. 2004. Vol. 35(12). P. 2807-2812.
- Chang N.C., Shih C.M., Bi W.F. et al. Fosinopril improves left ventricular diastolic function in young mildly hypertensive patients without hypertrophy // Cardiovasc. Drugs Ther. 2002. Vol. 16(2). P. 141-147.
- Мухин Н.А., Фомин В.В., Моисеев С.В., Хамхоева М. С. Хроническая сердечная недостаточность и поражение почек: перспективы лечения // Consilium Medicum. 2008. № 09.
- Sica D.A., Cutler R.E., Parmer R.J. et al. Comparison of the steady-state pharmacokinetics of fosinopril, lisinopril and enalapril in patients with chronic hepatic and renal insufficiency // Clin. Pharmacokinet. 1991. Vol. 20. P. 420-427.
- Vetter W. Treatment of senile hypertension. The Fosinopril in Old Patiets Study (FOPS) // Am. J. Hypertens. 1997. Vol. 10. S. 255-261.
- Карпов Ю.А., Мареев В.Ю., Чазова И. Е. Российские программы оценки эффективности лечения фозиноприлом больных с артериальной гипертонией и сердечной недостаточностью. Проект Три Ф (ФЛАГ, ФАСОН, ФАГОТ) // Сердечная недостаточность. 2003. № 4 (5). С. 2-6.
»» №1 1999 ПРОФЕССОР Ю.Н. ЧЕРНОВ, ЗАВЕДУЮЩИЙ КАФЕДРОЙ КЛИНИЧЕСКОЙ ФАРМАКОЛОГИИ С КУРСОМ ФУВ ВОРОНЕЖСКОЙ МЕДИЦИНСКОЙ АКАДЕМИИ ИМЕНИ Н.Н. БУРДЕНКО
Г.А. БАТИЩЕВА, ЗАВЕДУЮЩАЯ КУРСОМ КЛИНИЧЕСКОЙ ФАРМАКОЛОГИИ, КАНДИДАТ МЕДИЦИНСКИХ НАУК
ПРОФЕССОР В.М. ПРОВОТОРОВ, ЗАВЕДУЮЩИЙ КАФЕДРОЙ ФАКУЛЬТЕТСКОЙ ТЕРАПИИ, ЛАУРЕАТ ПРЕМИИ СОВЕТА МИНИСТРОВ СССР
С.Ю. ЧЕРНОВ, АСПИРАНТ КАФЕДРЫ ФАКУЛЬТЕТСКОЙ ТЕРАПИИ
Ингибиторы ангиотензин-превращающего фермента (АПФ) - группа лекарственных средств, применение которых с начала 70-х годов позволило достигнуть определенных успехов в лечении больных с сердечно-сосудистой патологией.
В настоящее время применяется уже около 50 препаратов группы ингибиторов АПФ . Опыт их использования при артериальной гипертонии, сердечной недостаточности, ишемической болезни сердца, диабетической нефрологии одновременно ставит вопросы, связанные с оптимизацией фармакотерапии. В первую очередь это определение особенностей индивидуальной реакции на прием ингибиторов АПФ, прогноз проводимого лечения, четкие противопоказания, разработка системы мониторирования фармакодинамических эффектов, определение критериев отмены.
Фармакологическое действие ингибиторов АПФ обусловлено их влиянием на функциональное состояние ренин-ангиотензин-альдостероновой системы. При этом ингибиторы АПФ обладают необходимой структурой, позволяющей им взаимодействовать с атомом цинка в молекуле ангиотензин-превращающего фермента. Это сопровождается его инактивацией и подавлением активности циркулирующей (плазменной) и тканевой (локальной) ангиотензиновых систем.
Препараты группы отличаются по выраженности и продолжительности ингибирующего влияния на ангиотензин I-превращающий фермент: в частности, рамиприл в организме превращается в активный метаболит - рамиприлат, сродство которого к ангиотензин I-превращающему ферменту в 42 раза выше, а комплекс рамиприл-фермент в 72 раза стабильнее, чем каптоприл-фермент .
Сродство активного метаболита квинаприла - квинаприлата к ангиотензин I-превращающему ферменту в 30-300 раз сильнее, чем лизиноприла, рамиприлата или фозиноприлата .
Ингибирование ангиотензин I-превращающего фермента имеет дозозависимый характер. В частности, периндоприл в дозе 2 мг ингибирует на 80% ангиотензин I-превращающий фермент на пике действия и на 60% - через 24 часа. При увеличении дозы периндоприла до 8 мг его ингибирующая способность возрастает соответственно до 95% и 75% .
Блокада выработки локального ангиотензина II может зависеть от степени проникновения препаратов в ткани - ингибиторы АПФ, обладающие высокой липофильностью, легче проникают в ткани и подавляют активность ангиотензин I-превращающего фермента.
При изучении способности ингибиторов АПФ ингибировать ангиотензин I-превращающий фермент в тканях легких, сердца, почек, надпочечников и в аорте было установлено, что трандалоприл, рамиприл и периндоприл превосходят эналаприл по способности снижать образование ангиотензина II в тканях этих органов.
По данным М. Ondetti (1988) самый высокий индекс липофильности у активного метаболита квинаприла - квинаприлата по сравнению с эналаприлатом, рамиприлатом, периндоприлатом. При этом квинаприлат подавляет активность ангиотензин I-превращающего фермента в плазме, легких, почках, сердце, не изменяя активности ангиотензин I-превращающего фермента в головном мозге и яичках .
Другой ингибитор АПФ - периндоприл (или его активная форма) проникает через гематоэнцефалический барьер, снижая активность АПФ в головном мозге .
Фармакологическое действие ингибиторов АПФ, вызывая торможение превращения ангиотензина I в активный вазоконстрикторный ангиотензин II, ведет к уменьшению уровня ангиотензина II в плазме с уменьшением высвобождения норадреналина из пресинаптических окончаний симпатических нервных волокон .
Блокада эффектов ангиотензина II ограничивает высвобождение кальция из саркоплазматического ретикулума , что уменьшает вазоконстрикторную реакцию гладкомышечных клеток .
При лечении ингибиторами АПФ происходит изменение баланса вазоактивных соединений в пользу сосудорасширяющих биологически активных веществ, что достигается за счет ограничения активности кининазы, идентичной АПФ, и повышения уровня брадикинина.
Воздействие брадикинина на брадикининовые рецепторы сосудистого эндотелия способствует высвобождению эндотелийзависимого релаксирующего фактора - окиси азота и вазодилатирующих простагландинов (простагландин Е2, простациклин) .
В механизме гипотензивного действия ингибиторов АПФ важное значение имеет уменьшение продукции и высвобождение альдостерона из надпочечников, что влияет на регуляцию калий-натриевого обмена и содержание в организме жидкости. Данный эффект ингибиторов АПФ ведет к уменьшению накопления натрия в сосудистых гладкомышечных клетках и ограничению избыточной вазоконстрикции, что особенно выражено при солезависимой артериальной гипертонии .
Учитывая, что содержание АПФ в эндотелии сосудов намного превышает его количество в циркулирующей крови, предполагается, что эндотелий сосудов является основной точкой приложения ингибиторов АПФ . Курсовая терапия препаратами группы вызывает структурные изменения артериальной стенки: уменьшение гипертрофии гладкомышечных клеток с ограничением количества избыточного коллагена. Достоверно увеличивается просвет периферических артерий , обратному развитию подвергается гипертрофия мышечной оболочки артерий и артериол , что связано с торможением миграции и пролиферации гладкомышечных клеток , со снижением образования в эндотелии сосудов эндотелина, оказывающего влияние на продукцию фактора роста эндотелия .
Тканевые эффекты ингибиторов АПФ проявляются уменьшением гипертрофии миокарда с изменением соотношения миоцитов и коллагена в пользу миоцитов .
Клиническими наблюдениями установлено, что сосудорасширяющее действие ингибиторов АПФ может проявляться в различных сосудистых бассейнах на уровне артериол, венул, сосудов микроциркуляции.
Установлена возможность снижения сосудистого сопротивления в малом круге кровообращения , в системе портального кровотока , регионального кровообращения в почках .
Увеличение диаметра крупных периферических артерий (с 13% до 21%) отмечено на фоне приема каптоприла и рамиприла. При этом рамиприл приводил к выраженному увеличению объемной скорости кровотока . Улучшение функции эндотелия коронарных сосудов показано при длительном, 6-месячном назначении квинаприла .
Системный гапотензивный эффект препаратов группы проявляется в снижении систолического и диастолического артериального давления при воссстановлении хроноструктуры суточного АД.
Как показали клинические исследования, однократный суточный прием эналаприла (эднит) приводит к улучшению показателей суточного мониторирования АД . При фармакотерапии рамиприлом систолическое АД снижается преимущественно в дневное, а диастолическое - как в дневное, так и в ночное время . Курсовое применение моэксиприла у больных мягкой и умеренной артериальной гипертензией снижает среднесуточное АД без изменения характера кривой АД и вариабельности частоты сердечных сокращений. При этом действие препарата более выражено в дневное время .
Важно, что чем выше сродство препарата к АПФ, тем меньше его терапевтическая доза, продолжительнее гипотензивный эффект и меньше колебания АД в течение суток .
Ингибитор АПФ короткого действия каптоприл оказывает антигипертензивный эффект в течение первого часа после приема, а общая продолжительность действия препарата составляет 6 часов . Максимальная хроночувствительность к каптоприлу (капотен) выявлена утром, в полдень и ранние вечерние часы .
В связи с быстротой развития гипотензивного эффекта каптоприл можно использовать в качестве средства для купирования гипертонических кризов. При этом действие препарата проявляется через 5-7 минут, а снижение АД через 15 минут .
В отличие от каптоприла ингибиторы АПФ второго поколения оказывают антигипертензивное действие в период до 24 часов. Максимальный эффект эналаприла отмечается через 4-6 часов, лизиноприла через 4-10 часов, квинаприла через 2-4 часа после приема .
Отмечена индивидуальная особенность реакции АД при назначении ингибиторов АПФ у больных сердечной недостаточностью: при трехмесячной курсовой терапии положительная динамика суточного АД отмечалась у больных сердечной недостаточностью с артериальной гипертензией, тогда как при фармакотерапии больных без артериальной гипертензии достоверных изменений суточного профиля АД не происходило .
Индивидуальная реакция АД на введение ингибиторов АПФ у больных артериальной гипертонией может зависеть от уровня суточной секреции альдостерона, адреналина, норадреналина.
Гипотензивный эффект на прием эналаприла (ренитек) больше выражен у больных с высокими показателями экскреции альдостерона, адреналина, норадреналина при уменьшении концентрации альдостерона и натрия в плазме крови. Напротив, у больных без гипотензивного эффекта уровень гормонов в крови и моче к концу двухнедельного лечения существенно не отличался от исходного, а экскреция натрия с мочой даже уменьшалась . Недостаточный гипотензивный эффект ингибиторов АПФ также отмечен у пациентов с увеличением индекса массы тела, в этих случаях требуется применения более высоких доз препаратов .
Предполагается, что при низкой реабсорбции натрия и высоком уровне циркулирующего ренина степень гипотензивного эффекта ингибиторов АПФ должна быть более высокой, поскольку в этом случае уменьшение периферической вазоконстрикции связано со снижением образования циркулирующего ангиотензина II .
Сердечно-сосудистые эффекты ингибиторов АПФ наряду со снижением тонуса артериол включают венодилатирующее действие с перераспределением крови в сосуды нижних конечностей. При этом у больных может возрастать реакция на ортостатическую пробу с появлением постуральной гипотонии .
Снижение системного АД с уменьшением посленагрузки одновременно с уменьшением венозного возврата крови к сердцу вызывает уменьшение давления наполнения желудочков. Кардиопротекторнос действие ингибиторов АПФ также обусловлено их влиянием на локальную ренин-ангиотензиновую систему с воздействием на гипертрофию, дилатацию, ремоделирование миокарда, а также на структуру сосудистой стенки коронарных артерий .
Ингибиторы АПФ увеличивают коронарный резерв за счет уменьшения гипертрофии медиального слоя интрамуральных коронарных артерий , а курсовая терапия каптоприлом улучшает релаксационные свойства миокарда, уменьшая гипоперфузию миокарда при пробе на введение дипиридамола (по результатам нагрузочной сцинтиграфии миокарда) .
Назначение ингибиторов АПФ у больных хронической сердечной недостаточностью (ХСН) увеличивает скорость и силу сокращения субэндо- и субэпикардиальных слоев, повышая скорость раннего диастолического наполнения левого желудочка, что способствует увеличению толерантности к физической нагрузке .
Трандалоприл (гоптен) в лечении больных ХСН не только улучшает гемодинамические показатели, но и снижает асинхронию и повышает чувствительность к нитроглицерину .
Имеются данные о более благополучном течении ремоделирования у больных, у которых в первые 24 часа после инфаркта миокарда проводили терапию ингибиторами АПФ .
Как показали клинические исследования, эналаприл (эднит) после 16-недельной терапии наряду со снижением среднесуточных показателей систолического и диастолического АД способствует уменьшению массы миокарда левого желудочка .
Ингибиторы АПФ - единственная группа препаратов, о которых известно, что они способны улучшать прогноз жизни больных хронической сердечной недостаточностью: по данным 32 рандомизированных исследований применение ингибиторов АПФ позволило снизить смертность в среднем на 23% и уменьшить общее число случаев госпитализации в связи с декомпенсацией ХСН на 35% . В сравнительных исследованиях показано преимущество терапии ингибиторами АПФ (эналаприл) по сравнению с фармакотерапией дигоксином . Более того, применение ингибиторов АПФ при лечении ХСН позволяет достигнуть положительной динамики состояния при предшествующей малоэффективной терапии .
Использование рамиприла , эналаприла на ранних стадиях сердечной недостаточности устраняет диастолическую дисфункцию миокарда за счет периода раннего наполнения, способствуя при длительном приеме сохранению функции левого желудочка .
Длительная курсовая терапия ингибиторами АПФ улучшает сократительную функцию миокарда, достоверно снижая конечный диастолический объем и конечный систолический объем с увеличением сердечного выброса и фракции выброса . При этом отмечена коррекция патологической асинхронии миокарда правого и левого желудочков .
Ингибиторы АПФ используются у больных акромегалией при устранении гиперсоматотропинемии до и после радикального лечения, поскольку показана возможность регресса гипертрофии левого желудочка .
Применение каптоприла позволяет повысить эффективность электростимуляционной кардиомиопластики у больных тяжелой сердечной недостаточностью в отдаленные сроки наблюдения - через 6-12 месяцев, приводя к уменьшению преходящих и стабильных дефектов перфузии миокарда . Оценка индивидуальной реакции больных на применение ингибиторов АПФ позволила установить, что влияние на регресс гипертрофии левого желудочка тем больше, чем выше исходная масса миокарда , а эффективность применения ингибиторов АПФ при ХСН II-III класса наиболее выражена у пациентов с исходно низкой фракцией выброса.
Представляет клинический интерес тот факт, что при лечении хронического легочного сердца применение ингибиторов АПФ (престариум в суточной дозе 2-4 мг) также более эффективно у больных с исходно увеличенными размерами правого предсердия и правого желудочка при гипокинетическом типе гемодинамики .
Улучшение показателей сократительной функции миокарда правых отделов сердца наряду со снижением давления в легочной артерии показано при приеме каптоприла , престариума , рамиприла , лизиноприла . Достоверное улучшение сократительной способности миокарда правых отделов сердца сопровождается улучшением функции внешнего дыхания с увеличением показателей пробы Тиффно .
Шестимесячный прием периндоприла у больных ХСН улучшает бронхиальную проходимость крупных, средних и мелких бронхов. При этом увеличение проходимости в мелких бронхах более выражено у курящих пациентов .
Положительную динамику функции внешнего дыхания при лечении ХСН у больных с ревматическими пороками сердца авторы связывают с уменьшением венозного застоя в малом круге кровообращения в результате снижения пред- и постнагрузки .
Существуют данные о том, что ингибиторы АПФ могут снижать гипоксическую вазоконстрикцию , однако появление ирритативного кашля, как одного из побочных эффектов, может ограничивать их применение.
Кроме того, при приеме ингибиторов АПФ в ряде случаев у пациентов с бронхолегочной патологией возможно ухудшение течения заболевания.
Лечение эналаприлом артериальной гипертензии у больных с сопутствующим обострением хронического бронхита может увеличивать обструкцию средних и мелких бронхов, что отчасти связано с холинергическим дисбалансом , а использование престариума у пациентов с гиперкинетическим типом гемодинамики может повышать давление в легочной артерии .
При клиническом применении ингибиторов АПФ также необходимо учитывать состояние функции почек, поскольку в почках присутствуют все составляющие тканевой ренин-ангиотензиновой системы, а снижение образования циркулирующего и локального ангиотензина II с уменьшением тонуса выносящих артериол влияет на скорость клубочковой фильтрации .
Показано нефропротекторное действие ингибиторов АПФ при лечении больных диабетической нефропатией , артериальной пшертензией , гломерулонефритом , волчаночным нефритом , склеродермией .
При назначении ингибиторов АПФ важное значение имеет корригирующее действие препаратов на уровень системной и клубочковой гипертензии, а также длительность сохранения антипротеинурического действия после их отмены. Данный эффект может сохраняться до 6 месяцев, что определяет необходимость повторного курса фармакотерапии ингибиторами АПФ не менее двух раз в год .
Клиническими наблюдениями обоснована необходимость предварительного контроля состояния функционального почечного резерва (ФПР) и определения наличия микроальбуминурии при назначении ингибиторов АПФ. Фармакотерапия прогностически неблагоприятна, если у больного снижен ФПР и в моче обнаруживаются почечные изоферменты карбоновых эстераз, что свидетельствует об ишемии проксимальных канальцев почек .
Осторожно следует назначать ингибиторы АПФ больным со сниженным ФПР и нормоальбуминурией, что указывает на работу почек в условиях высокого градиента внутриклубочкового гидростатического давления, а уменьшение системного и клубочкового давления при использовании ингибиторов АПФ у таких больных может вызвать ухудшение перфузии почек .
Существует точка зрения, что назначение ингибиторов АПФ не показано для профилактики развития диабетической нефропатии, поскольку у больных с сохраненным ФПР и нормоальбуминурией введение препаратов этой группы может приводить к гиперфильтрации и ухудшению функционального состояния почек .
Применение ингибиторов АПФ при реноваскулярном стенозе может быть альтернативой хирургическому вмешательству в случае монолатерального стеноза, который сопровождается ренинзависимой гипертонией .
При билатеральном стенозе введение ингибиторов АПФ исключено из-за опасности пре- и постгломерулярной вазодилатации и риска критического снижения локального почечного кровотока .
Влияние ингибиторов АПФ на состояние регионального кровообращения отмечено и в отношении портального кровотока. В частности, курсовая терапия каптоприлом, эналаприлом, периндоприлом у больных портальной гастропатией приводит к уменьшению ранимости и кровоточивости слизистой с исчезновением эрозий и язв .
Ингибиторы АПФ могут влиять на состояние микроциркуляторного русла: курсовая терапия каптоприлом ограничивает проявления венозного застоя с уменьшением диаметра венул и увеличением артерио-венулярного соотношения до 1:3 . При этом наряду с ускорением кровотока выявлен положительный гемореологический эффект каптоприла (тензиомина): уменьшение внутрисосудистой агрегации с достоверным снижением АДФ-индуцированной агрегации , уменьшение уровня растворимых комплексов фибрин-мономеров, продуктов деградации фибриноген-фибрина.
Увеличение фибринолитической активности крови также установлено на фоне 6-месячного приема периндоприла . Курсовая терапия престариумом в суточной дозе 4 мг, оказывает влияние на плазменное и сосудисто-тромбоцитарное звено гемостаза, снижая активность фактора Виллебранта , а кратковременное применение эналаприла у здоровых людей ограничивает изменения гемостаза на физическую нагрузку .
Наряду с положительным влиянием на показатели гемостаза ингибиторы АПФ способствуют нормализации водного обмена, включая содержание свободной и связанной воды, ионов калия, натрия во фракциях крови.
Среди фармакологических эффектов ингибиторов АПФ можно отметить возможность влияния на липидный, углеводный и пуриновый обмены.
Лечение ингибиторами АПФ приводит к снижению инсулинорезистентности и улучшению метаболизма глюкозы, что связывают с увеличением образования брадикинина и улучшением микроциркуляции.
Оптимизация транспорта инсулина и глюкозы к тканям с повышением чувствительности клеток к инсулину и увеличением утилизации глюкозы под влиянием фармакотерапии ингибиторами АПФ может быть настолько выраженной, что требует гликемического контроля .
Положительное влияние ингибиторов АПФ на липидный обмен у больных артериальной гипертонией с сахарным диабетом , при лечении больных с постменопаузальной гипертонией проявляется умеренной тенденцией к уменьшению уровня холестерина, триглицеридов при снижении индекса атерогенности. Ингибиторы АПФ могут способствовать метаболическому обеспечению (ЛДГ, Г-6-ФДГ) транспорта кислорода, активизируя процессы синтеза макроэргических соединений в эритроцитах.
Ингибиторы АПФ увеличивают экскрецию почками уратов, поэтому являются препаратами первого выбора у больных артериальной гипертонией в сочетании с подагрой. Однако особенности индивидуальной реакции на их прием у отдельных пациентов могут приводить к образованию подагрических камней .
Реакции лекарственного взаимодействия ингибиторов АПФ изучены еще недостаточно. Отмечено усиление антигипертензивного действия при сочетании ингибиторов АПФ с гипотиазидом , при трехкомпонентной схеме: коринфар-ретард + корданум + каптоприл , при проведении комбинированной терапии: эналаприл + бета-блокаторы или в сочетании с антагонистами кальция 2-го поколения (исрадипином, амлодипином) .
Одновременное назначение эналаприла и лозартана сопровождается снижением активности натрийуретического пептида (на 17,8%) и эндотелеина (на 24,4%).
В постгоспитальном периоде инфаркта миокардадля ограничения прогрессирования сердечной недостаточности наиболее эффективна комбинированная терапия эналаприлом в сочетании с бета-блокаторами .
Сочетание капотена с амиодароном позволяет повысить антиаритмический эффект до 93,8 %, при этом исчезают "пробежки" желудочковой тахикардии и достоверно урежается частота желудочковых экстрасистол .
Говоря о неблагоприятных реакциях лекарственного взаимодействия ингибиторов АПФ следует отметить, что наряду с препаратами лития и калия побочное действие ингибиторов АПФ могут усиливать цитостатики и интерферон, при сочетании с которыми увеличивается частота возникновения нейтропении и агранулоцитоза .
Терапия НПВС, приводящая вследствие ингибирования синтеза простагландинов к сужению в почках приносящей артериолы, в сочетании с ингибиторами АПФ, устраняющими сужение выносящей артериолы, ухудшает клубочковую фильтрацию и ведет к нарушению функции почек .
Среди побочных эффектов ингибиторов АПФ возможны появление кашля (0,7-25%), ангионевротического отека (0,1-0,2%), кожной сыпи (1-5%), нарушение вкуса и синдрома "обожженного языка" (0,1-0,3%).
К нарушениям вкусовых ощущений при фармакотерапии ингибиторами АПФ предрасполагает дефицит цинка, связанный с патологией печени .
Среди побочных эффектов нередко отмечают слабость, тошноту, головокружение, запоры, но они не служат причиной отмены препарата, коррекция дозы и уровня АД позволяет устранить эти явления .
Артериальная гипотония на прием первой дозы отмечается у 10% больных, особенно при наличии ХСН, однако при фармакотерапии периндоприлом гипотензивный эффект первой дозы отсутствует .
Возникновение протеинурии на введение ингибиторов АПФ отмечается у 3,5% больных, принимавших каптоприл, у 0,72% - получавших моэксиприл, и у 1,4% - на прием эналаприла, что, как правило, связано с уменьшением внутриклубочкового давления. Препаратом выбора считается спираприл, при назначении которого уровень креатинина не меняется, даже если клиренс менее 30 мл/мин. К редким побочным эффектам ингибиторов АПФ относятся нейтропения, агранулоцитоз. Описаны случаи возникновения апластической анемии на прием лизиноприла.
Ингибиторы АПФ противопоказаны при беременности, поскольку ведут к недостатку амниотической жидкости, неонатальной анемии и гипоплазии легких у плода. В первые три месяца беременности возможно фетотоксическое действие .
Экспериментально доказана возможность развития аномалии почек при введении эналаприла в неонатальном периоде .
При клиническом применении ингибиторов АПФ важно учитывать особенности фармакокинетики. Так, при назначении препаратов второго поколения (пролекарства) у больных с сопутствующей патологией печени удлиняется время, в течение которого концентрация препарата в плазме достигает максимума .
Установлена связь окислительного метаболизма с выраженностью гипертензивного эффекта ИАПФ. При этом месячная курсовая фармакотерапия эналаприлом не дает эффекта у 45% больных, которые являются "медленными окислителями" .
Среди многочисленных вопросов, касающихся применения ингибиторов АПФ, до конца не ясна тактика отмены препаратов, что связано с увеличением активности ренина плазмы на фоне фармакотерапии ингибиторами АПФ и возможностью развития синдрома отмены.
Требует дальнейшего исследования аспект профилактического назначения ингибиторов АПФ у лиц, имеющих генетически детерминированную повышенную активность АПФ, поскольку эти люди рассматриваются как группа риска развития ИБС .
Сложную задачу представляет определение критериев прогноза эффективности терапии ингибиторами АПФ, что особенно актуально для препаратов второго поколения, клиническое применение которых позволяет оценивать эффект не ранее 4 недель курсовой терапии. Учитывая высокую стоимость препаратов второго поколения, это имеет и социально-экономическую значение.
Перспективным является дальнейшее изучение фармакологического действия ингибиторов АПФ во взаимосвязи с определением показателей перекисного окисления липвдов, состоянием антиоксидантной системы и уровнем эйкозаноидов в организме.
В заключение можно отметить, что проблема эффективного применения ингибиторов АПФ до конца не решена. Уточнение индивидуальных особенностей реакции на введение ингибиторов АПФ необходимо для выбора тактики назначения препаратов с целью оптимизации фармакотерапии.
Лиетратура
1. Александров A.A. АПФ - ингибиторы: возраст клинического совершеннолетия. В мире лекарств. 1998, 1, с. 21.
2. Арутюнов Г.П., Вершинин A.A., Степанова Л.В. и др. Влияние длительной терапии ингибитором АПФ эналаприлом (ренитеком) на течение постгоспитального периода острого инфаркта миокарда. Клиническая фармакология и фармакотерапия. 1998, 2, с. 36-40.
3. Ахмедова Д. А., Казанбиев Н.К., Атаева 3.Н. и др. Влияние комбинированной терапии на ремоделирование левого желудочка гипертонического сердца. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 15.
4. Балахонова Н.П., Авдеев В.Г., Кузнецов Н.Е. и др. Применение каптоприла (ацетен фирмы "Вокхардт") при гипертонической болезни и застойной сердечной недостаточности. Клиническая медицина. 1997, 75, 1, с. 42-43.
5. Белоусов Ю.Б., Тхостова Э.Б. Клиническое применение ингибиторов ангиотензинпревращающего фермента Берлиприл®5. М. "Универсум Паблишинг". 1997, с. 28.
6. Борисенко А.П., Гвоздев Ю.Н., Аксенова Т.Н. и др. Амиодарон и капотен в лечении прогностически опасных аритмий у больных с хронической недостаточностью кровообращения. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 28.
7. Бугрова О.В., Багирова В.В., Рыбина О.И. Влияние ренитека на состояние почечного функционального резерва у больных системной красной волчанкой и системной склеродермией. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 34.
8. Гиляровский С.P., Орлов В.А. Терапевтическая тактика при возникновении побочных эффектов ингибиторов АПФ. Клиническая фармакология и фармакотерапия. 1997, 4, с. 74-83.
9. Гукова С.П., Фомичева Е.В., Ковалев Ю.Р. Роль структурного полиморфизма гена ангиотензинпревращающего фермента в развитии инфаркта миокарда. Клиническая медицина. 1997, 75,9, с. 36-38.
10. Гургенян С.В., Адальян К.Г., Ватинян С.Х. и др. Регрессия гипертрофии левого желудочка под влиянием ингибитора ангиотензинпревращающего фермента эналаприла у больных гипертонической болезнью. Кардиология. 1998, 38, 7, с. 7-11.
11. Демидова И.В., Терещенко С.Н., Моисеев B.C. и др. Влияние ингибитора АПФ периндоприла на функцию внешнего дыхания у больных хронической сердечной недостаточностью. Тезисы докладов Пятого Российского нацинального конгресса "Человек и лекарство". Москва, 1998, с. 58.
12. Дитятков А.Е., Тихонов В.А., Евстафьев Ю.А. и др. Применение рамиприла в лечении легочной гипертензии при туберкулезе. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 61.
13. Зонис Б.Я. Антигипертензивная терапия у больных сахарным диабетом. Русский медицинский журнал. 1997, 6, 9, с. 548-553.
14. Ивлева А.Я. Клиническое применение ингибиторов ангиотензинпревращающего фермента и антагонистов ангиотензина II. М., 1998, из-во "Миклош", с. 158.
15. Какалия Э., Белоусов Ю.Б., Быков А.В. и др. Эффективность каптоприла (тензиомина) при длительном лечении артериальной гипертонии. Советская медицина. 1991, 10, с. 45-48.
16. Карпов Р.С., Павлюкова Е.Н., Таранов С.В. и др. Опыт длительной терапии больных с синдромом X. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 90.
17. Кахновский И.М., Фомина М.Г., Остроумов Е.Н. и др. Гоптен (трандолаприл) при лечении хронической сердечной недостаточности у больных ишемической болезнью сердца. Терапевтический архив. 1998, 70, 8, с. 29-33.
18. Кислый Н.Д., Пономарев В.Г., Малик М.А. и др. Ингибиторы АПФ у больных с портальной гастропатией. Клиническая фармакология и фармакотерапия. 1997, 2, с. 42-43.
19. Кобалава Ж.Д., Морылева О.Н., Котовская Ю.В. и др. Артериальная гипертония после менопаузы: лечение ингибитором АПФ моэксиприлом. Клиническая фармакология и фармакотерапия. 1997,4, с. 63-74.
20. Коротков Н.И., Ефимова Е.Г., Шутемова Е.А. и др. Влияние престариума на состояние гемодинамики больных хроническим обструктивным бронхитом. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 103.
21. Коц Я.И., Вдовенко Л.Г., Бадамшина Н.Б. и др. Диастолическая функция левого желудочка у больных с сердечной недостаточностью в процессе лечения ингибитором ангиотензинконвертирующего фермента рамиприлом и антагонистом рецепторов ангиотензина II козааром. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 105.
22. Кукес В.Г., Игнатьев В.Г., Павлова Л.И. и др. Клиническая эффективность коринфар-ретарда в сочетании с корданумом, триампуром, капотеном у больных артериальной гипертонией. Клиническая медицина. 1996, 74, 2, с. 20-22.
23. Кукушкин С.К., Лебедев А.В., Маношкина Е.Н. и др. Сравнительная оценка антигипертензивного эффекта рамиприла и каптоприла методом 24-часового амбулаторного мониторирования АД. Клиническая фармакология и фармакотерапия. 1997,3, с. 27-28.
24. Кутырина И.М., Тареева И.Е., Швецов М.Ю. и др. Опыт применения рамиприла у больных волчаночным нефритом. Клиническая фармакология и фармакотерапия. 1997, 2, с. 25-26.
25. Мазур Н.А. Органные поражения, нарушения метаболизма при артериальной гипертонии и влияние на них гипотензивной терапии. Терапевтический архив. 1995, 67, 6, с. 3-5.
26. Маланьина К.С., Некрутенко Л.А., Хлынова О.В. Влияние престариума на сосудисто-тромбоцитарный гемостаз у больных гипертонической болезнью. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 130.
27. Марков В.А., Гавина А.В., Колодин М.И. и др. Влияние периндоприла в сочетании с тромболизисом на размеры левого желудочка и клиническое течение инфаркта миокарда. Клиническая фармакология и фармакотерапия. 1997, 1, с. 30-31.
28. Моисеев B.C. Ингибиторы АПФ и нефропатия. Клиническая фармакология и фармакотерапия. 1997, 4, с. 67-69.
29. Ольбинская Л.И., Пинская Э.В., Большакова Т.Д. и др. Активность некоторых систем нейрогуморальной регуляции, состояние электролитного баланса и клиническая эффективность ренитека у больных гипертонической болезнью. Терапевтический архив. 1996, 68, 4, с. 54-57.
30. Ольбинская Л.И., Андрушишина Т.Б., Захарова В.Л. Антигипертензивная эффективность по данным суточного мониторирования АД, безопасность и влияние на морфофункциональные показатели сердца ингибитора ангиотензинпревращающего фермента эднита у больных гипертонической болезнью. Кардиология. 1997, 37, 9, с. 26-29.
31. Ольбинская Л.И., Андрушишина Т.Б. Влияние нового ингибитора ангиотензинпревращающего фермента моэксиприла на суточные ритмы артериального давления у больных гипертонической болезнью. Терапевтический архив. 1997, 69, 3, с. 58-61.
32. Ольбинская Л.И., Сизова Ж., Царьков И. Лечение хронической сердечной недостаточности ингибиторами ангиотензинпревращающего фермента. Врач. 1998, 8, с. 11-15.
33. Орлова Л.А., Мареев В.Ю., Синицын В.Г. и др. Влияние ингибитора ангиотензинпревращающего фермента эналаприла и сердечного гликозида дигоксина на ремоделирование левого желудочка. Кардиология. 1997, 37, 2, с. 4-9.
34. Пекарская М.В., Ахмедов Ш.Д., Кривощеков Е.В. и др. Применение капотена при лечении больных, перенесших операцию электростимуляционной кардиомиопластики. Кардиология. 1998, 38, 7, с. 21-23.
35. Пекарский С.Е., Воротцова И.Н., Мордовян В.Ф. Уменьшение гипертрофии левого желудочка и динамика параметров суточного мониторирования АД под влиянием рамиприла у больных эссенциальной артериальной гипертонией. Терапевтический архив. 1997, 69, 4, с. 18-20.
36. Пекарский С.Е., Кривоногов Н.Г., Грисс С.В. и др. Особенности ренопротективного действия рамиприла у больных гипертонической болезнью. Клиническая фармакология и фармакотерапия. 1997, 1, с. 26-29.
37. Рязанова С.Э. Лечение сердечной недостаточности у больных хроническим легочным сердцем. Российский медицинский журнал. 1997, 3, с. 57-62.
38. Савенков М.П., Иванов С.Н. Изменение функции внешнего дыхания у больных хроническим бронхитом при применении эналаприла и лозартана. Тезисы докладов Третьего Российского национального конгресса "Человек и лекарство". Москва, 1996, с. 197.
39. Свиридов A.A., Погонченкова И.В., Задионченко В.А. Гемодинамические эффекты синоприла при лечении больных хроническим легочным сердцем. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 188.
40. Силоренко Б.А., Сополева Ю. В. Ингибитор ангиотензинпревращающего фермента моэксиприл в лечении артериальной гипертензии у женщин в период после менопаузы. Кардиология. 1997, 37, 6, с. 87-92.
41. Сидоренко В.А., Преображенский Д.В. Диапазон клинического применения ингибитора ангиотензинпревращающего фермента квинаприла. Кардиология. 1998, 3, с. 85-90.
42. Смирнова И.Ю., Дементьева Н.Г., Малыхин А.Ю. и др. Фармакокинетический подход к оптимизации антигипертензивной терапии эналаприлом. Всерос. науч. конф. "От materia medica к современным медицинским технологиям". 1998, с. 163.
43. Сотникова Т.И., Федорова Т.А., Рыбакова М.К. и др. Эффективность тензиомина в лечении больных с хронической сердечной недостаточностью. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 201.
44. Стипаков Е.Г., Стипакова А.В., Шутемова Е.А. и др. Престариум в терапии системной и легочной гипертонии у больных хроническими обструктивными заболеваниями легких. Тезисы докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 205.
45. Терещенко С.Н., Дроздов В.Н., Левчук Н.Н. и др. Изменение плазменного звена гемостаза при лечении периндоприлом у больных с застойной сердечной недостаточностью. Клиническая фармакология и фармакотерапия. 1997, 4, с. 83-87.
46. Терещенко С.Н., Дроздов В.Н., Демидова И.В. и др. Ингибитор ангиотензинпревращающего фермента периндоприл при лечении застойной сердечной недостаточности. Терапевтический архив. 1997, 69, 7, с. 53-56.
47. Терещенко С.Н., Кобалава Ж.Д., Демидова И.В. и др. Изменение суточного профиля артериального давления у больных с застойной сердечной недостаточностью при терапии ингибитором ангиотензинпревращающего фермента периндоприлом. Терапевтический архив. 1997, 69, 12, с. 40-43.
48. Тихонов В.П., Туренко Е.В. Эффективность лечения капотеном больных артериальной гипертонией в зависимости от состояния почек. Тезисы докладов Третьего Российского национального конгресса "Человек и лекарство". Москва, 1996, с. 220.
49. Тхостова Э.Б., Пронин А.Ю., Белоусов Ю.Б. Применение эналаприла у больных мягкой и умеренной артериальной гипертонией по данным суточного мониторирования АД. Кардиология. 1997, 37, 10, с. 30-33.
50. Фатенков В.Н., Фатенков О.В., Щукин Ю.В. и др. Ингибиторы ангиотензинпревращающего фермента в лечении сердечной недостаточности у больных ИБС. Тезисы Докладов Пятого Российского национального конгресса "Человек и лекарство". Москва, 1998, с. 223.
51. Фазулзянов А.А., Андреев В.М., Фазулзянова Г.Н. Механика дыхания, альвеолярная вентиляция, вентиляционно-перфузионные отношения при коррекции сердечной недостаточности строфантином и капотеном. Казанский медицинский журнал. 1995, LXXVI, 6, С.417-419.
52. Федорова Т.А., Сотникова Т.И., Рыбакова М.К. и др. Клинико-гемодинамические и гемореологические эффекты каптоприла при сердечной недостаточности. Кардиология. 1998, 38,5, с. 49-53.
53. Филатова Н.П. Применение периндоприла (престариума) при артериальной гипертонии. Терапевтический архив. 1995, 67, 9, с. 81-83.
54. Филатова Е.В., Вихерт О.А., Рогоза Н.М. и др. Сравнение влияния капотена (каптоприла) и рамиприла на суточный профиль артериального давления и периферическую гемодинамику больных гипертонической болезнью в сочетании с сахарным диабетом. Терапевтический архив. 1996, 68, 5, с. 67-70.
55. Фукс А.Р. Влияние ломира и энапа на диастолическую функцию левого желудочка у больных артериальной гипертензией. Клиническая фармакология и фармакотерапия. 1997, 1, с. 27-28.
56. Хлынова О. В., Гуев А.В., Щекотов В. В. Динамика показателей венозного и центрального кровообращения у больных артериальной гипертонией при лечении эналаприлом. Клиническая фармакология и фармакотерапия. 1998, 1, с. 59-61.
57. Шестакова М.В., Шереметьева С.В., Дедов И.И. Тактика применения ренитека (ингибитора ангиотензинпревращающего фермента) для лечения и профилактики диабетической нефропатии. Клиническая медицина. 1995, 73, 3, с. 96-99.
58. Шустов С.Б., Баранов В.Л., Кадин Д.В. Влияние ингибитора ангиотензинпревращающего фермента периндоприла на состояние миокарда левого желудочка у больных акромегалией после радикального лечения. Кардиология. 1998, 38, 6, с. 51-54.
59. Щербань Н.Н., Пахомова С.П., Каленский В.X. и др. Сравнение эффективности сублингвального применения капотена и празозина в лечении гипертонических кризов. Клиническая медицина. 1995, 73, 2, с. 60.
60. Bertoli L., Lo Cicero S., Busnardo I. et al. Effects of captopril on hemodynamics and blood gases in chronic obstructive lung disease with pulmonary hypertension. Respiration 49, 251-256, 1986.
61. Campese V. M. Salt sensitivity in hypertension. Renae and cardiovascular implications. Hypertension 23, 531-550, 1994.
62. Derkx F H M., Tan-Thong L., Wenting G. J. et al. Assynchronous changes in prorenin and renin secretion after captopril in patients with renal artery stenosis. Hypertension 5, 244-256, 1983.
63. Fabris В., Chen В., Pupie V. et al. Inhibition of angiotensin-converting enzyme (ACE) in plasma and tissue. J. Cardiovasc Pharmacol, 1990, 15, Suppl., 6-13.
64. Gibbons G.H. Endotelial function as a determinant of vascular function and structure: A new therapeutic target. Am J. Cardiol, 1997, 79, 5a, 3-8.
65. Glasser Stephen P. The time course of left ventricular remodeling after acute myocardial infarction. Am. J. Cardial, 1997, 80, 4, 506-507.
66. Guron Gregor, Adams Michael A., Sundelin Brigitta, Friberg Peter. Neonatal angiotensin-converting enzyme inhibition in the rat induces persistent abnormalities in renal function and hystology. Hypertension, 1997, 29, 1 ,Pt 1, 91-97.
67. Ikeda Uichi, Shimada Kazujuki. NO and cardiac failure. Clin. Cardiol, 1997, 20, 10, 837-841.
68. Johnston C.I. Tissue angiotensin converting enzyme in cardie and vascular hypertrophy, repair and remodeling. Hypertension, 1994, 23, 258-268.
69. Johnston C.I., Fabris В., Yamada A. et al. Comparative studies off tissue inhibition by angiotensin-converting enzyme inhibitors. J. Hypertens, 1989, 7, Suppl. 5, 11-16.
70. Lindpaintner К., Jin M., Wilhelm M. J. et al. Intracardiac generation of angiotensin and its physiologic role. Circulacion, 77, (Suppl.1), 1988, 1-18.
71. Luseher Т., Wensel R., Morean P., Tacase H. Vascular protective effects of SCE inhibitors and calcium antagonists: Theoretical basis for a combination therapy in hypertension and ofther cardiovascular diseases. Cardiovasc Drugs Ther, 1995, 9, 509-523.
72. Mancini G. В. J.; Henry G. P., Macay C. et al Angiotensin converting enzyme inhibition with quinapril improves endothclial vasomotor dysfunction in patients with coronary artery disease. The TREND study. Circulation, 1996, 94, 258-265.
73. Me Areavey D., Robertson J.I.S. Angiotensin converting enzyme inhibitors and moderate hypertension. Drugs, 1990, 40, 326-345.
74. Morgan К.G. The role of calcium in the control of vascular tone as assessed by the Ca++ indicator aequorin. Cardiovasc Drugs Ther 4, 1990, 1355-1362.
75. Ondetti M.A. Structural relationships of angiotensin-converting enzyme inhibitors to pharmacological activity. Circulation, 1988, - 77, Suppl. 1, 74-78.
76. Pedram Ali, Razandi Mahnaz, An Ren - Ming. Vasoactive peptides modulate vascular endothelial cell growth factor production and endothelial cell proliferation and invasion. J. Biol. Chem., 1997, 272, 27, 17097-17103.
77. Perella M. A., Hildebrand G.F.L. Margulis K.B. Endotelium - derived relaxing factor in regulation of basal cardio - pulmonary and renal function. Am J. Physiology, 261, 1991, 323-328.
78. Pratt R.E. ltoh H., Gibbons G.H., Dzan V. J. Role ofangiotensine in the control of vascular smooth muscle cell growth. J. Of Vsc. Med. And Biol., 1991, 3, 25-29.
79. Prisco D., Paniccia R., Bandinelli B. Short-term ACE inhibition may influence exercise-induced changes in haemostasis in healthy subjects. Fibrinolysis, 1997, 11, 4, 187-192.
80. Schror К. Role of prostaglandins in the cardiovascular effects of bradykinine and the angiotensin-converting enzyme inhibitors. J. Cardiovasc Pharmacol, 1992, 20 (Suppl. 9), 68, 73.
81. Simpson P. С. Kariya К., Kams L. R. et. al. Adrenergic hormones and control of cardiac myocyte growth. Mollecular and Cellular Biochem, 1991, 104, 35-43.
82. Van Belle Eric, Vallet Beno Jt, Anffray Jean-Luc, Bauters Christophe et al. NO syntehesis is involved in structural and functional effects of ACE inhibitors in injured arteries. Am J. Physiology, 1997, 270, 1,2, 298-305.
Ингибиторы АПФ (ИАПФ) - медикаменты нового поколения, действие которых направлено на снижение артериального давления. В настоящее время в фармакологии представлено свыше 100 видов таких препаратов.
Все они обладают общим механизмом действия, но отличаются друг от друга по структуре, способу выведения из организма и длительности воздействия. Общепринятая классификация ИАПФ отсутствует, и все деления этой группы препаратов являются условными.
Условная классификация
По способу фармакологического действия существует классификация, которая делит ингибиторы АПФ на три группы:
- ИАПФ с сульфгидрильной группой;
- ИАПФ с карбоксильной группой;
- ИАПФ с фосфинильной группой.
Классификация основана на таких показателях, как способ выведения из организма, период полувыведения и т.д.
К лекарственным препаратам 1 группы относятся:
- Каптоприл (Капотен);
- Беназеприл;
- Зофеноприл.
Эти препараты имеют показания к применению пациентам, у которых гипертония сочетается с ишемической болезнью сердца. Они быстро всасываются в кровь. Для более эффективного действия их принимают за 1 час до приёма пищи, чтобы ускорить процесс всасываемости. В некоторых случаях ингибиторы АПФ могут быть назначены вместе с диуретиками. Медикаменты этой группы также можно принимать диабетикам, пациентам с лёгочной патологией и сердечной недостаточностью.
С осторожностью следует относиться к приёму пациентам с заболеванием мочевыделительной системы, так как лекарство выводится почками.
Перечень препаратов 2 группы:
- Эналаприл;
- Квинаприл;
- Ренитек;
- Рамиприл;
- Трандолаприл;
- Периндоприл;
- Лизиноприл;
- Спираприл.
Ингибиторы АПФ, содержащие карбоксильную группу, имеют механизм более длительного действия. Подвергаются метаболическому превращению в печени, оказывая сосудорасширяющий эффект.
Третья группа: Фозиноприл (Моноприл).
Механизм действия Фозиноприла направлен преимущественно на контролирование утренних подъёмов АД. Его относят к препаратам последнего поколения. Он обладает длительным воздействием (около суток). Выводится из организма при помощи печени и почек.
Существует условная классификация ингибиторов АПФ нового поколения, которые представляют собой комбинацию с диуретиками и с антагонистами кальция.

Ингибиторы АПФ в комбинации с диуретиками:
- Капозид;
- Эланаприл Н;
- Ирузид;
- Скоприл плюс;
- Рамазид Н;
- Аккузид;
- Фозикард Н.
Комбинация с диуретиком обладает эффектом более быстрого действия.
Ингибиторы АПФ в комбинации с антагонистами кальция:
- Корипрен;
- Эквакард;
- Триапин;
- Эгипрес;
- Тарка.
Механизм действия этих медикаментов направлен на усиление растяжимости крупных артерий, что особенно важно для пожилых гипертоников.
Таким образом, комбинирование препаратов предусматривает усиление действия лекарства при недостаточной эффективности ИАПФ в отдельности.
Преимущества
Преимуществом препаратов ИАПФ является не только их способность снижать артериальное давление: основной механизм их действия направлен на защиту внутренних органов больного. Они хорошо воздействуют на миокард, почки, сосуды головного мозга и т.д.

При гипертрофии миокарда ингибиторы АПФ более интенсивно сокращают сердечную мышцу левого желудочка в отличие от других препаратов от гипертонии.
ИАПФ улучшают функцию почек при хронической почечной недостаточности. Также отмечено, что эти препараты улучшают общее состояние больного.
Показания
Основные показания к применению:
- гипертония;
- инфаркт миокарда;
- атеросклероз;
- дисфункция левого желудочка;
- хроническая сердечная недостаточность;
- ишемическая болезнь сердца;
- диабетическая нефропатия.
Как принимать ингибиторы АПФ
Запрещено во время приёма ИАПФ употреблять заменители соли. В состав заменителей входит калий, который задерживается в организме препаратами против гипертензии. Не следует применять в пищу продукты, обогащённые калием. К ним относятся картофель, грецкие орехи, курага, морская капуста, горох, чернослив и фасоль.
Во время лечения ингибиторами нельзя принимать такие противовоспалительные нестероидные средства, как Нурофен, Бруфен и т. п. Данные медикаменты задерживают в организме жидкость и натрий, тем самым снижая эффективность ИАПФ.

Очень важно при постоянном приёме препаратов АПФ контролировать уровень артериального давления и функцию почек. Не рекомендуется самостоятельно отменять препараты без консультации с врачом. Непродолжительный курс лечения ингибиторами может не проявить своей эффективности. Только при длительном лечении лекарство способно регулировать уровень АД и быть весьма действенным при таких сопутствующих заболеваниях, как сердечная недостаточность, ишемическая болезнь сердца и т.д.
Противопоказания
У ингибиторов АПФ существуют как абсолютные, так и относительные противопоказания.
Абсолютные противопоказания:
- беременность;
- лактация;
- гиперчувствительность;
- гипотония (ниже 90/60 мм);
- стеноз почечных артерий;
- лейкопения;
- тяжёлый аортальный стеноз.
Относительные противопоказания:
- умеренная артериальная гипотония (от 90 до 100 мм);
- тяжёлая хроническая почечная недостаточность;
- тяжёлая анемия;
- хроническое легочное сердце в стадии декомпенсации.
Показания к применению с вышеперечисленными диагнозами определяются лечащим специалистом.
Побочные эффекты
Ингибиторы АПФ чаще всего хорошо переносимы. Но иногда могут проявляться и побочные действия лекарства. К ним относят головную боль, тошнота, головокружения и утомляемость. Не исключено и появление артериальной гипотензии, усугубление почечной недостаточности, возникновение аллергических реакций. Реже встречаются такие побочные эффекты, как сухой кашель, гиперкалиемия, нейтропения, протеинурия.
Не стоит самостоятельно назначать себе ингибиторы АПФ. Показания к применению определяются сугубо врачом.
© Использование материалов сайта только по согласованию с администрацией.
Ингибиторы АПФ (иАПФ, ингибиторы ангиотензинпревращающего фермента, англ. – ACE) составляют большую группу фармакологических средств, применяемых при сердечно-сосудистой патологии, в частности - . На сегодняшний день они являются и наиболее популярными, и наиболее доступными в ценовом отношении средствами лечения гипертонии.
Перечень ингибиторов АПФ чрезвычайно широк. Они отличаются по химическому строению и названиям, но принцип действия у них одинаков - блокада фермента, при помощи которого образуется активный ангиотензин, вызывающий стойкую гипертонию.
Спектр действия ингибиторов АПФ не ограничивается сердцем и сосудами. Они положительно влияют на работу почек, улучшают показатели липидного и углеводного обмена, благодаря чему успешно применяются диабетиками, людьми пожилого возраста с сопутствующими поражениями других внутренних органов.
Для лечения артериальной гипертензии ингибиторы АПФ назначают в виде монотерапии, то есть поддержание давления достигается приемом одного лекарства, либо в виде комбинации с препаратами из других фармакологических групп. Некоторые ингибиторы АПФ сразу представляют собой комбинированные препараты (с мочегонными, антагонистами кальция). Такой подход облегчает для пациента прием препаратов.
Современные иАПФ не только прекрасно сочетаются с препаратами из других групп, что особенно важно для возрастных пациентов с сочетанной патологией внутренних органов, но и оказывают ряд положительных эффектов - нефропротекция, улучшение кровообращения в коронарных артериях, нормализация обменных процессов, поэтому их можно считать лидерами в процессе лечения гипертонии.
Фармакологическое действие иАПФ
Ингибиторы АПФ блокируют действие ангиотензин-превращающего фермента, необходимого для превращения ангиотензина I в ангиотензин II. Последний способствует спазму сосудов, за счет которого увеличивается общее периферическое сопротивление, а также продукции альдостерона надпочечниками, который вызывает задержку натрия и жидкости. Как следствие этих изменений возрастает .

Ангиотензин-превращающий фермент в норме содержится в плазме крови и в тканях. Плазменный фермент обуславливает быстрые реакции сосудов, например, при стрессе, а тканевый отвечает за долговременные эффекты. Препараты, блокирующие АПФ, должны инактивировать обе фракции фермента, то есть важной характеристикой их будет способность проникать в ткани, растворяясь в жирах. От растворимости в конечном счете зависит эффективность лекарства.
При нехватке ангиотензин-превращающего фермента не запускается путь образования ангиотензина II и не происходит увеличения давления. Кроме того, иАПФ приостанавливают распад брадикинина, необходимого для расширения сосудов и снижения давления.
Длительный прием препаратов из группы иАПФ способствует:
- Уменьшению общего периферического сопротивления сосудистых стенок;
- Снижению нагрузки на сердечную мышцу;
- Уменьшению артериального давления;
- Улучшению кровотока в коронарных, мозговых артериях, сосудах почек и мышц;
- Снижению вероятности развития .
Механизм действия ингибиторов АПФ включает защитное действие в отношении миокарда. Так, они предотвращают появление , а если она уже есть, то систематическое употребление этих лекарств способствует ее обратному развитию с уменьшением толщины миокарда. Также они препятствуют перерастяжению камер сердца (дилатация), которое лежит в основе сердечной недостаточности, и прогрессированию фиброза, сопровождающего гипертрофию и ишемию сердечной мышцы.

механизм действия иАПФ при хронической сердечной недостаточности
Оказывая благоприятное действие на сосудистые стенки, иАПФ тормозят размножение и увеличение размеров мышечных клеток артерий и артериол, препятствуя спазму и органическому сужению их просветов при длительной гипертонии. Важным свойством этих препаратов можно считать усиление образования оксида азота, который противостоит атеросклеротическим отложениям.
Ингибиторы АПФ улучшают многие показатели обмена. Они облегчают связывание с рецепторами в тканях, нормализуют обмен , повышают концентрацию , необходимого для правильной работы мышечных клеток, и способствуют выведению натрия и жидкости, избыток которых провоцирует подъем артериального давления.
Важнейшей характеристикой любого гипотензивного средства является его влияние на почки, ведь примерно пятая часть больных гипертензией умирают в конечном итоге от их недостаточности, связанной с артериолосклерозом на фоне гипертонии. С другой стороны, при симптоматической почечной гипертензии пациенты уже имеют ту или иную форму почечной патологии.
Ингибиторы АПФ обладают неоспоримым преимуществом - они лучше всех остальных средств защищают почки от губительного действия повышенного давления. Это обстоятельство и послужило причиной их столь широкого распространения для лечения первичной и симптоматической гипертензии.
Видео: базисная фармакология ИАПФ
Показания и противопоказания к иАПФ
Ингибиторы АПФ применяются в клинической практике на протяжении тридцатилетия, на постсоветском пространстве они стремительно распространились в начале 2000-х, заняв прочную лидирующую позицию среди других гипотензивных средств. Главный повод к их назначению - артериальная гипертензия, а одно из весомых преимуществ - эффективное снижение вероятности осложнений со стороны сердечно-сосудистой системы.

Основными показаниями к применению ингибиторов АПФ считают:
- Сочетание гипертонии с и диабетическим нефросклерозом;
- Почечную патологию с высоким давлением;
- Гипертензию при застойной ;
- Недостаточность сердца со сниженным выбросом из левого желудочка;
- Систолическую дисфункцию левого желудочка без учета показателей давления и наличия или отсутствия клиники нарушения сердечной деятельности;
- Острый инфаркт миокарда после стабилизации давления или состояние после перенесенного инфаркта, когда фракция выброса левого желудочка менее 40% или есть признаки систолической дисфункции на фоне инфаркта;
- Состояние после перенесенного инсульта при высоком давлении.
Долговременное применение иАПФ приводит к значительному уменьшению риска цереброваскулярных осложнений (инсульты), инфаркта сердца, сердечной недостаточности, а также сахарного диабета, что выгодно отличает их от антагонистов кальция или диуретиков.
Для длительного приема в качестве монотерапии вместо бета-адреноблокаторов и мочегонных, иАПФ рекомендованы следующим группам пациентов:
- Тем, у кого бета-блокаторы и мочегонные вызывают выраженные побочные реакции, не переносятся либо неэффективны;
- Лицам, предрасположенным к диабету;
- Больным с уже установленным диагнозом диабета типа II.
В качестве единственного назначенного лекарства ингибитор АПФ эффективен на I-II стадиях гипертонии и у большинства молодых больных. Однако эффективность монотерапии составляет около 50%, поэтому в ряде случаев возникает необходимость дополнительного приема бета-адреноблокатора, антагониста кальция или мочегонного. Комбинированная терапия показана на III стадии патологии, у пациентов с сопутствующими заболеваниями и в пожилом возрасте.
Перед тем, как назначить средство из группы иАПФ, врач проведет детальное исследование для исключения заболеваний или состояний, которые могут стать препятствием к приему этих лекарств. При их отсутствии выбирается тот препарат, который у данного больного должен быть наиболее эффективным исходя из особенностей его метаболизма и пути выведения (через печень либо почки).
Дозировка иАПФ подбирается индивидуально, опытным путем. Сначала назначается минимальное количество, затем доза доводится до среднетерапевтической. При начале приема и весь этап корректировки дозы следует регулярно измерять давление - оно не должно превышать норму или стать слишком низким в момент максимального действия лекарства.
В целях избежать больших колебания давления от гипотонии до гипертонии прием препарата распределяется на протяжении суток таким образом, чтобы давление по возможности не «прыгало». Снижение давления в период максимального действия лекарства может превышать его уровень в конце периода действия принятой таблетки, но не более, чем в два раза.
Специалисты не рекомендуют принимать максимальные дозы ингибиторов АПФ, так как в этом случае существенно возрастает риск побочных реакций и снижается переносимость терапии. При неэффективности средних доз лучше добавить в лечение антагонист кальция или диуретик, сделав схему терапии комбинированной, но без увеличения дозы иАПФ.

Как к любым лекарственным средствам, к ингибиторам АПФ есть противопоказания. Эти средства не рекомендуются к приему беременными женщинами, так как возможно нарушение кровотока в почках и расстройство их функции, а также возрастание уровня калия в крови. Не исключено негативное воздействие на развивающийся плод в виде пороков, выкидышей и внутриутробной гибели. Учитывая выведение препаратов с грудным молоком, при их применении в период лактации кормление грудью нужно прекратить.
В числе противопоказаний также:
- Индивидуальная непереносимость иАПФ;
- обеих почечных артерий или одной из них при единственной почке;
- Тяжелая стадия почечной недостаточности;
- любой этиологии;
- Детский возраст;
- Уровень систолического артериального давления ниже 100 мм.
Особую осторожность нужно соблюдать больным циррозом печени, гепатитом в активной фазе, атеросклерозом венечных артерий, сосудов ног. Ввиду нежелательного лекарственного взаимодействия, иАПФ лучше не принимать одновременно с индометацином, рифампицином, некоторыми психотропными препаратами, аллопуринолом.
Не глядя на хорошую переносимость, иАПФ все же могут вызывать побочные реакции. Наиболее часто пациенты, длительно их принимающие, отмечают эпизоды , сухой кашель, аллергические реакции, расстройства в работе почек. Эти эффекты называют специфическими, а к неспецифическим относят извращение вкуса, нарушение пищеварения, сыпь на коже. В анализе крови возможно обнаружение анемии и лейкопении.
Видео: опасное сочетание – иАПФ и спиронолактон
Группы ингибиторов ангиотензин-превращающего фермента
Наименования препаратов для снижения давления широко известны большому числу пациентов. Кто-то длительно принимает один и тот же, кому-то показана комбинированная терапия, а часть пациентов вынуждены менять один ингибитор на другой на этапе подбора эффективного средства и дозы для снижения давления. К ингибиторам АПФ относятся эналаприл, каптоприл, фозиноприл, лизиноприл и др., отличающиеся между собой фармакологической активностью, временем действия, способом выведения из организма.
В зависимости от химического строения выделяют различные группы ингибиторов АПФ:
- Препараты с сульфгидрильными группами (каптоприл, метиоприл);
- Дикарбоксилат-содержащие иАПФ (лизиноприл, энам, рамиприл, периндоприл, трандолаприл);
- иАПФ с фосфонильной группой (фозиноприл, церонаприл);
- Препараты с гиброксамовой группой (идраприл).

Список препаратов постоянно расширяется по мере того, как накапливается опыт применения отдельных из них, а новейшие средства проходят клинические испытания. Современные иАПФ имеют небольшое число побочных реакций и хорошо переносятся абсолютным большинством пациентов.
Ингибиторы АПФ могут выводиться почками, печенью, растворяться в жирах или воде. Большинство из них превращаются в активные формы только после прохождения по пищеварительному тракту, но четыре препарата сразу представляют собой активное лекарственное вещество - каптоприл, лизиноприл, церонаприл, либензаприл.
По особенностям метаболизма в организме иАПФ делятся на несколько классов:
- I - растворимые в жирах каптоприл и его аналоги (альтиоприл);
- II - липофильные предшественники иАПФ, прототип которых - эналаприл (периндоприл, цилазаприл, моэксиприл, фозиноприл, трандолаприл);
- III - гидрофильные препараты (лизиноприл, церонаприл).
Препараты второго класса могут иметь преимущественно печеночный (трандолаприл), почечный (эналаприл, цилазаприл, периндоприл) пути выведения либо смешанный (фозиноприл, рамиприл). Эта особенность учитывается при назначении их пациентам с расстройствами работы печени и почек для исключения риска поражения этих органов и серьезных побочных реакций.
Ингибиторы АПФ не принято делить на поколения, но все же условно это деление происходит. Новейшие препараты практически не отличаются по строению от более «старых» аналогов, но кратность приема, доступность для тканей могут отличаться в лучшую сторону. Кроме того, усилия фармакологов направлены на уменьшение вероятности побочных эффектов, и новые препараты в целом переносятся больными лучше.
Одним из наиболее давно применяемых иАПФ является эналаприл . Он не обладает пролонгированным действием, поэтому пациент вынужден его принимать несколько раз в сутки. В связи с этим многие специалисты считают его устаревшим. Вместе с тем, эналаприл и по сей день показывает прекрасный терапевтический эффект при минимуме побочных реакций, поэтому он по-прежнему остается одним из самых назначаемых средств этой группы.
К ингибиторам АПФ последнего поколения можно отнести фозиноприл, квадроприл и зофеноприл.
Фозиноприл содержит фосфонильную группу и выводится двумя путями - через почки и печенью, что позволяет назначать его больным с нарушением работы почек, которым иАПФ из других групп могут быть противопоказаны.
Зофеноприл по химическому составу близок к каптоприлу, но обладает пролонгированным действием - его нужно принимать один раз в сутки. Длительный эффект дает зофеноприлу преимущество перед другими иАПФ. Кроме того, этот препарат оказывает антиоксидантное и стабилизирующее в отношении мембран клеток действие, поэтому прекрасно защищает сердце и сосуды от неблагоприятных влияний.
Другим пролонгированным препаратом является квадроприл (спираприл) , который хорошо переносится больными, улучшает работу сердца при застойной его недостаточности, снижает вероятность осложнений и продлевает жизнь.
Преимуществом квадроприла считают равномерный гипотензивный эффект, сохраняющийся весь период между приемом таблеток благодаря длительному периоду полувыведения (до 40 часов). Эта особенность практически исключает вероятность сосудистых катастроф в утренние часы, когда действие иАПФ с более коротким полувыведением заканчивается, а больной еще не принял очередную дозу лекарства. К тому же, если пациент забудет принять очередную таблетку, гипотензивный эффект будет сохранен до того момента следующих суток, когда он про нее все же вспомнит.
Благодаря выраженному протективному эффекту в отношении сердца и сосудов, а также длительному действию, зофеноприл многие специалисты считают лучшим для лечения пациентов с сочетанием гипертонии и ишемии сердца. Часто эти заболевания сопутствуют друг другу, а изолированная гипертензия сама по себе способствует ишемической болезни сердца и ряду ее осложнений, поэтому вопрос одновременного воздействия сразу на оба заболевания очень актуален.
К ингибиторам АПФ нового поколения, помимо фозиноприла и зофеноприла, относят также периндоприл, рамиприл и квинаприл . Их главным преимуществом считают пролонгированное действие, которое очень облегчает пациенту жизнь, ведь для поддержания нормального давления достаточно лишь однократного приема препарата ежедневно. Стоит также отметить, что масштабные клинические исследования доказали их положительную роль в увеличении продолжительности жизни больных гипертонией и ишемической болезнью сердца.
При необходимости назначения ингибитора АПФ перед врачом стоит нелегкая задача выбора, ведь препаратов насчитывается более десятка. Многочисленные исследования показывают, что более старые препараты не имеют существенных преимуществ перед новейшими, а эффективность их практически одинакова, поэтому специалист должен опираться на конкретную клиническую ситуацию.
Для длительной терапии гипертензии подойдет любой из известных препаратов, кроме каптоприла, который и по сей день применяется только для купирования гипертонических кризов. Все остальные средства назначаются для постоянного приема в зависимости от сопутствующих заболеваний:
- При диабетической нефропатии - лизиноприл, периндоприл, фозиноприл, трандолаприл, рамиприл (в уменьшенных дозах из-за более медленного выведения у больных со сниженной почечной функцией);
- При патологии печени - эналаприл, лизиноприл, квинаприл;
- При ретинопатии, мигрени, систолической дисфункции, а также для курильщиков препарат выбора - лизиноприл;
- При сердечной недостаточности и дисфункции левого желудочка - рамиприл, лизиноприл, трандолаприл, эналаприл;
- При сахарном диабете - периндоприл, лизиноприл в сочетании с мочегонным (индапамид);
- При ишемической болезни сердца, в том числе - в остром периоде инфаркта миокарда назначаются трандолаприл, зофеноприл, периндоприл.
Таким образом, нет большой разницы, какой именно ингибитор АПФ выберет врач для долгосрочного лечения гипертонии - более «старый» или последний из синтезированных. К слову, в США наиболее часто выписываемым остается лизиноприл - один из первых препаратов, применяемых уже около 30 лет.
Пациенту важнее понять, что прием иАПФ должен быть систематическим и постоянным, даже пожизненным, а не в зависимости от цифр на тонометре. Для того, чтобы давление поддерживалось на нормальном уровне, важно не пропускать очередную таблетку и не менять самостоятельно ни дозировку, ни наименование препарата. При необходимости, врач назначит дополнительно или , но ингибиторы АПФ при этом не отменяются.
Видео: урок по ингибиторам АПФ
Видео: ингибиторы АПФ в программе “Жить здорово”