Антифосфолипидный синдром (синоним: синдром антифосфолипидных антител; АФС) – аутоиммунное состояние, вызванное антителами, которые направлены против фосфолипидов клеточных мембран. Впервые синдром был описан в 1983 году британским ревматологом Грэмом Хьюджем. Антифосфолипидный синдром повышает риск возникновения тромбов (сгустков крови) как в артериях, так и в венах. В статье мы разберем: АФС – что это такое, причины возникновения и признаки.
При некоторых заболеваниях в организме вырабатываются антитела, способные атаковать фосфолипиды – компоненты клеточных мембран, что приводит к развитию тромбозов
Антифосфолипидный синдром характеризуется образованием антител к компонентам собственных клеточных мембран (фосфолипидам). Фосфолипиды – важные строительные блоки клеточных мембран в организме человека: они содержатся в тромбоцитах, в нервных клетках и в клетках кровеносных сосудов. Поскольку многие патогены очень похожи на структуры организма, может случиться так, что иммунная система потеряет возможность различать «друзей» и «врагов».
Исследования показывают, что до 5% человеческого населения имеют антитела к фосфолипидам в крови. У женщин значительно чаще развивается антифосфолипидный синдром, чем у мужчин. Средний возраст возникновения синдрома варьируется от 25 до 45 лет.
В международной классификации болезней 10-го пересмотра (МКБ-10) синдром антифосфолипидных антител обозначается кодом D68.6.
Причины
Причины возникновения АФС до конца не изучены. В медицине выделяют 2 формы антифосфолипидного синдрома (АФС): первичную и вторичную. Первичная форма антифосфолипидного синдрома не обусловлена конкретным органическим заболеванием.
Гораздо более распространенным является вторичный фосфолипидный синдром, который сопровождает некоторые заболевания и состояния. При этом АФС развивается вследствие того, что патогены имеют на своей поверхности образования, которые похожи на структуры человеческих клеток. В результате иммунная система образует антитела, которые связывают и устраняют как патоген, так и собственные липиды организма. Такой процесс называется «молекулярной мимикой».
Причиной вторичного АФС могут быть:
- аутоиммунные заболевания (системная красная волчанка, хронический полиартрит, склеродермия, псориатический артрит и др.);
- ряд вирусных или бактериальных инфекций: ВИЧ, гонорея, сифилис, эпидемический паротит и болезнь Лайма;
- ревматоидный артрит;
- дефицит витамина D, витамина Е и цистеина может повысить риск развития аутоиммунных заболеваний;
- в редких случаях АФС при беременности появляется вследствие множественной миеломы или гепатита;
- очень редкой причиной является длительное применение противоэпилептических препаратов, хинина и интерферона.
Факторы риска

Люди, злоупотребляющие алкогольными напитками, входят в группу риска по возможности заболевания антифосфолипидным синдромом
Основные факторы риска:
- курение;
- избыточный вес;
- обезвоживание;
- длительное применение противозачаточных средств (таблетки);
- недостаток физической активности;
- злоупотребление алкогольными напитками;
- питание с избыточным количеством продуктов, богатых витамином К – капуста, шпинат и сыр;
- злоупотребление арахидоновой кислотой и растительными омега-6 жирными кислотами, которое содержатся в пищевых маслах.
Классификация
Выделяют четыре клинико-лабораторных формы АФС:
- Первичная.
- Вторичная.
- Катастрофическая (за короткое время развиваются множественные тромбозы внутренних органов, приводящие к полиорганной недостаточности).
- АФЛ-негативная (не определяются серологические маркеры заболевания).
Симптоматика
Два основных симптома, характерных для антифосфолипидного синдрома:
- артериальный и венозный тромбоз;
- тромбоцитопения.
Венозный тромбоз чаще всего встречается в нижних конечностях, но может также возникать и в других частях венозной системы. Артериальные тромбозы встречаются преимущественно в сосудах головного мозга, но могут также появляться в артериях других органов.
В зависимости от местоположения тромбоза фосфолипидный синдром приводит к различным осложнениям: легочная эмболия, сердечные приступы, инфаркты почек и инсульты. Точные механизмы образования тромбов не полностью изучены.
Другим распространенным симптомом, особенно в случае первичного антифосфолипидного синдрома, является тромбоцитопения – снижение количества тромбоцитов, что характеризуется повышенной склонностью к кровотечениям. У пациентов может возникнуть парадоксальное кровотечение в коже. У женщин с фосфолипидным синдромом увеличивается риск раннего выкидыша.
Визуальные признаки АФЛ включают синеватое обесцвечивание конечностей и кожные язвы, которые могут возникать в различных частях тела.
Антифосфолипидный синдром является распространенной причиной инсульта у молодых пациентов. Если у пациента в возрасте до 45 лет возникает инсульт при отсутствии факторов риска (артериальной гипертонии, расстройства метаболизма липидов), следует исключить антифосфолипидный синдром.
Важно понимать, что не все пациенты с антифосфолипидными антителами страдают от тромботических осложнений. В крупномасштабном исследовании, в котором 360 пациентов с фосфолипидными антителами наблюдались в течение 4-летнего периода, только 9% имели венозный тромбоз. В других исследованиях сообщалось о более высокой частоте венозного и артериального тромбоза.
Диагностика

Основным способом диагностики антифосфолипидного синдрома является выявление в плазме крови антител
Симптомы антифосфолипидного синдрома не позволяют точно поставить диагноз, поскольку они также могут быть связаны с другими заболеваниями. Для выявления антифосфолипидного синдрома необходимо провести дополнительные лабораторные обследования.
В 2006 году группа экспертов перечислила критерии, которые по-прежнему актуальны и которые должны использоваться для окончательной диагностики антифосфолипидного синдрома:
- один или несколько артериальных и венозных тромбозов в ткани или органе. Сгустки крови должны быть подтверждены методами визуализации или гистологическим исследованием;
- одна или несколько необъяснимых внутриутробных смертей плода после 10-й недели беременности;
- несколько преждевременных родов морфологически нормальных новорожденных на 34-й неделе беременности или позже;
- три или более необъяснимых спонтанных аборта у женщины до 10-й недели беременности.
Лабораторные анализы и показатели антифосфолипидного синдрома:
- повышенная концентрация антикардиолипиновых антител в крови по меньшей мере в двух анализах с интервалом не менее 12 недель;
- положительный тест на волчаночный антикоагулянт (в соответствии с рекомендациями международного медицинского сообщества) в плазме крови;
- повышенная концентрация антител против бета-2-гликопротеина-1 в двух измерениях с интервалом в 3 месяца.
У 30-50% пациентов умеренно уменьшается количество тромбоцитов в крови (70 000-120 000/мкл); только в 5-10% случаях количество тромбоцитов ниже 50 000/мкл. У 1% пациентов возникает гемолитическая анемия и тромбоцитопеническая пурпура.
Окончательный диагноз «антифосфолипидный синдром» может быть поставлен только в том случае, если наблюдается хотя бы один клинический и лабораторный критерий.
Лечение антифосфолипидного синдрома

Аспирин препятствует сгущению тромбоцитов и противодействует развитию тромбозов и эмболий
Из-за отсутствия крупных и, соответственно, значимых клинических исследований на предмет причин заболевания, риска тромбоза и терапии, существует нехватка ясности относительно правильных стратегий лечения, даже в экспертных кругах.
Основные направления в терапии АФС – это лечение острого тромбоза и предотвращение повторного тромбирования сосудов. Пациентов следует лечить быстро, так как может возникнуть парадоксальное кровотечение. Позднее лечение может осложнить течение болезни.
Если отсутствуют абсолютные противопоказания, рекомендуется лечение с помощью ацетилсалициловой кислоты в низкой дозе. Аспирин препятствует сгущению тромбоцитов и, таким образом, может противодействовать развитию тромбозов и эмболий. Однако до сих пор не существует четких результатов исследования.
Аспирин дополняется введением гепарина, который предотвращает свертывание крови. С этой целью применяется также Маркумар (непрямой антикоагулянт).
В качестве профилактики дальнейших тромбозов и эмболий следует проводить долгосрочную антикоагулянтную терапию. Самые эффективные средства – кумарины, которые связаны с повышенным риском осложнений. Пожизненная антикоагуляция кумаринами рекомендуется только для пациентов с фосфолипидным синдромом и тяжелыми тромбоэмболическими осложнениями.
У всех пациентов с антифосфолипидным синдромом важно устранить возможные факторы, повышающие риск тромбоза: рекомендуется полностью отказаться от курения.
Вторичные формы требуют эффективного лечения основного заболевания.
Риск рецидивирующего тромбоза и окклюзии, к сожалению, высокий у пациентов с подтвержденным фосфолипидным синдромом. Поэтому им необходимо в долгосрочной перспективе (иногда – пожизненно) принимать антикоагулянт с антагонистом витамина К.
Предполагается, что статины оказывают умеренный противотромбозный эффект. Статины рекомендуются для пациентов с фосфолипидным синдромом, если у них повышена концентрация липидов в крови.
Женщины с антифосфолипидным синдромом должны воздерживаться от использования эстрогенсодержащих лекарств, которые применяют для предотвращения нежелательной беременности и лечения менопаузальных проблем. Употребление эстрогенов значительно увеличивает риск закупорки сосудов.
Лечение беременных с АФЛ

Девушкам с осложнениями беременности низкомолекулярный Гепарин вводится один раз в день
Беременные женщины являются пациентками высокого риска, с которыми необходимо обращаться с особой осторожностью. Если у женщины с антифосфолипидным синдромом не было тромбоза или осложнений при предыдущих беременностях, рекомендуется лечение с помощью ацетилсалициловой кислоты.
Исследования показывают, что комбинированное лечение (Аспирин + гепарин) может снизить риск дальнейшего спонтанного аборта. Некоторые международные исследовательские группы рекомендуют использовать низкомолекулярный гепарин.
Иногда требуется введение гепарина и Аспирина в низких дозах (100 мг в день). Хотя гепарин имеет гораздо меньшую продолжительность действия, чем Маркумар, и его следует вводить под кожу, он действует намного эффективнее.
Через два-три дня после родов гепариновая терапия возобновляется и продолжается в течение 6 недель, если в прошлом возникали тромбоэмболические осложнения. Если проводится амниоцентез или кесарево сечение, терапия гепарином должна быть прервана вечером перед процедурой.
В дополнение к терапии гепарином гинеколог часто прописывает прогестины, чтобы компенсировать недостаточность желтого тела. Кроме того, последовательное ношение компрессионных чулок 2 класса может улучшить состояние женщины.
Пациенткам с осложнениями беременности низкомолекулярный гепарин также вводится один раз в день. Низкомолекулярный гепарин, в отличие от Маркумара, не преодолевает плаценту и, следовательно, не влияет на плод.
Осложнения
Антифосфолипидный синдром является одним из относительно распространенных аутоиммунных заболеваний. Осложнения АФЛ в основном развиваются при беременности вследствие развития тромбоза сосудов плаценты. К таким осложнениям относятся:
- выкидыши и преждевременные роды;
- замирание плода и его внутриутробная гибель;
- преждевременная отслойка плаценты;
- аномалии развития плода;
- женское бесплодие;
- эклампсия;
- гестозы.
При отсутствии лечения осложнения беременности на фоне АФЛ возникают в 80% случаев.

Людям с антифосфолипидным синдромом курение противопоказано
Независимо от формы антифосфолипидного синдрома все больные с этим диагнозом должны вести образ жизни, который снижает риск тромбоэмболических осложнений: рекомендуется отказаться от табакокурения и употребления других психотропных средств.
Необходимо больше двигаться на свежем воздухе, принимать достаточное количество жидкости и не злоупотреблять спиртными напитками. Клинические рекомендации во многом зависят от состояния больного.
Пациентки с фосфолипидным синдромом должны воздерживаться от использования эстрогенсодержащих контрацептивов, поскольку они могут способствовать развитию тромбоза.
Беременность должна быть тщательно спланирована из-за повышенного риска выкидыша. Лечение синдрома необходимо корректировать во время беременности, чтобы предотвратить спонтанные аборты и не подвергать опасности плод. Женщины, которые хотят забеременеть, должны знать о возможных рисках и вариантах лечения во время беременности.
Прогноз и профилактика
Антифосфолипидный синдром коррелируют у пожилых людей со слабоумием. Болезнь также повышает риск развития почечных заболеваний (почечная недостаточность, почечный инфаркт), инсульта, ишемии миокарда.
Уровень смертности в течение 10 лет среди пациентов с АФЛ составляет 10%: это означает, что 10% больных погибнут в результате осложнений синдрома антифосфолипидных антител в течение следующих 10 лет.
Менее благоприятен прогноз у женщин, страдающих множественными сосудистыми тромбозами вскоре после родов. Существует опасность множественного сужения крупных и более мелких сосудов. Массивное сужение сосудов может ухудшить доставку крови к жизненно важным органам. Если в результате сужения просвета сосудов отказывает орган, пациент может погибнуть. Чем чаще пациент испытывает тромбоз во время его жизни, тем хуже прогноз.
Не существует методов профилактики антифосфолипидного синдрома. Косвенно можно предотвратить только развитие осложнений. При использовании антикоагулянтов следует избегать конкурентных видов спорта, использовать мягкие зубные щетки или электрическую бритву. Об употреблении новых лекарств нужно заблаговременно сообщать лечащему врачу, поскольку некоторые из них могут влиять на свертываемость крови.
В случае инсульта, сердечного приступа или кровоизлияния в легкие необходимо вызвать “скорую помощь”. Внезапное появление мочи в нижнем белье указывает на инфаркт почек, который также следует лечить немедленно.
Совет! При возникновении любых сомнений необходимо обращаться за консультацией квалифицированного специалиста. Чем раньше начинается лечение, тем лучше прогноз, поскольку с каждым новым тромбозом возрастает риск развития летального исхода.
Своевременное обращение к специалисту поможет предотвратить осложнения и, в некоторых случаях (вторичный антифосфолипидный синдром), полностью избавиться от недуга.
Для цитирования:
Насонов Е.Л. Профилактика и лечение антифосфолипидного синдрома: современные рекомендации и перспективы // РМЖ. 2004. №6. С. 377
ГУ Институт ревматологии РАМН, Москва
ГУ Институт ревматологии РАМН, Москва
А нтифосфолипидный синдром (АФС) - клинико-лабораторный симптомокомплекс, характеризующийся венозными и артериальными тромбозами, патологией беременности и некоторыми другими реже встречающимися клиническими проявлениями и лабораторными нарушениями, патогенетически связанными с синтезом антифосфолипидных антител (аФЛ) .
Профилактика и лечение АФС - сложная и недостаточно разработанная проблема . Это объясняется неоднородностью патогенетических механизмов, лежащих в основе АФС, отсутствием достоверных клинических и лабораторных показателей, позволяющих прогнозировать риск рецидивов тромбоза. В настоящее время не существует общепринятых международных стандартов тактики ведения пациентов с различными формами АФС, а предлагаемые рекомендации основаны главным образом на результатах «открытых» испытаний или ретроспективного анализа исходов заболевания . Недостаточно изучены подходы к профилактике и лечению атеросклеротического поражения сосудов, нередко развивающегося у пациентов с АФС . Поскольку «специфические» методы лечения иммунопатологических нарушений, лежащих в основе АФС, не разработаны, ведение пациентов с АФС (как и с другими тромбофилиями) основано на применении антикоагулянтных (антагонисты витамина К, гепарин) и антиагрегантных препаратов - ацетилсалициловая кислота (АСК). Характерная особенность АФС - высокий риск повторных тромбозов . Поэтому большинство пациентов вынуждены принимать антиагрегантные и/или антикоагулянтные препараты в течение длительного времени, а иногда и пожизненно.
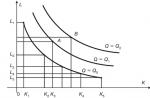
Полагают, что риск развития (и рецидивирования) тромбозов при АФС можно снизить путем исключения потенциально контролируемых «факторов риска», но истинная эффективность этих рекомендаций не известна. Факторы риска, которые необходимо учитывать при разработке тактики ведения пациентов, представлены в таблице 1.
Профилактика тромбозовАцетилсалициловая кислота
Учитывая определенную связь между увеличением титров аФЛ и риском развития тромбозов в общей популяции, полагают, что стойкое увеличение уровня аФЛ (даже в отсутствие клинических признаков АФС) является основанием для профилактического назначения низких доз АСК . Недавно были опубликованы данные двух ретроспективных исследований, посвященных оценке эффективности АСК . В одном исследовании изучалось 65 женщин с акушерской патологией, связанной с АФС. В течение 8 лет наблюдения тромботические нарушения развились только у 3 (10%) из 31 женщин, получавших АСК, и у 20 (59%) из 34 женщин, не получавших АСК . В другом исследовании, включавшем 77 пациентов с АФС или без тромбозов, но с положительными результатами определения аФЛ, было показано, что прием АСК четко ассоциируется с более низкой частотой развития тромбозов .
Учитывая определенную связь между увеличением титров аФЛ и риском развития тромбозов в общей популяции, полагают, что стойкое увеличение уровня аФЛ (даже в отсутствие клинических признаков АФС) является основанием для профилактического назначения низких доз АСК . Недавно были опубликованы данные двух ретроспективных исследований, посвященных оценке эффективности АСК . В одном исследовании изучалось 65 женщин с акушерской патологией, связанной с АФС. В течение 8 лет наблюдения тромботические нарушения развились только у 3 (10%) из 31 женщин, получавших АСК, и у 20 (59%) из 34 женщин, не получавших АСК . В другом исследовании, включавшем 77 пациентов с АФС или без тромбозов, но с положительными результатами определения аФЛ, было показано, что прием АСК четко ассоциируется с более низкой частотой развития тромбозов .Гидроксихлорохин
Существенный профилактический эффект, по крайней мере, при вторичном АФС, связанный с системной красной волчанкой (СКВ), могут оказать аминохинолиновые (антималярийные) препараты (гидроксихлорохин) . Наряду с противовоспалительным гидроксихлорохин обладает определенными антитромботическим (подавляют аггрегацию и адгезию тромбоцитов, уменьшают размер тромба) и гиполипидемическим эффектами. Применение гидроксихлорохина, несомненно, показано всем аФЛ-позитивным пациентам с СКВ .
Варфарин
Лечение антагонистами витамина К (варфарин) безусловно, более эффективный, но менее безопасный (по сравнению с АСК) метод профилактики венозных и артериальных тромбозов при АФС . Напомним, что применение антагонистов витамина К-антикоагулянтов требует тщательного клинического (геморрагические осложнения) и лабораторного (определение протромбинового времени) контроля. Для стандартизации результатов этого теста следует оценивать параметр «международное нормализованное отношение» (МНО), который учитывает влияние используемого в тесте тромбопластина на величину протромбинового времени.
Схема лечения варфарином при АФС такая же, как и при других тромбофилиях, и заключается в назначении «насыщающей» дозы (5 мг/день) в течение первых 2-х дней, а затем в подборе оптимальной дозы препарата, ориентируясь на «целевое» МНО. Следует помнить, что у лиц пожилого возраста для достижения того же уровня антикоагуляции следует использовать более низкие дозы варфарина, чем у молодых .
Особое значение имеет вопрос об интенсивности и длительности антикоагуляции. Известно, что увеличение МНО с 2-3 до 3,1-4,0 ассоциируется с возрастанием частоты тяжелых геморррагических осложнений (интракраниальные геморрагии или геморрагии, приводящие к летальному исходу, требующие переливания крови или госпитализации) . Напомним, что к факторам риска геморрагических осложнений на фоне лечения варфарином относятся:
- пожилой возраст (увеличение на 32% частоты любых кровотечений и увеличение частоты «больших» кровотечений на 46% каждые 10 лет после 40 лет)
- неконтролируемая артериальная гипертензия (систолическое АД >180 мм Hg, диастолическое АД > 100 мм Hg)
- язвенная болезнь желудка
- прием алкоголя
- прием НПВП (включая низкие дозы АСК) и парацетамола
- наличие инсульта в анамнезе
- прием нескольких лекарственных препаратов
- прием азатиоприна
- прием высоких доз метилпреднизолона
- полиморфизм цитохрома Р450СY2C2, отвечающего за метаболизм гепарина
- диффузное снижение плотности белого вещества головного мозга (выявляемой при МРТ или КТ).
В общей популяции пациентов с венозными тромбозами отмена варфарина ассоциируется с одинаковой (5-10%) частотой рецидивирования тромбозов независимо от длительности предшествующего лечения варфарином (6, 12 и 24 мес.) . Однако, как уже отмечалось, для АФС характерен высокий риск рецидивирования тромбозов. Поэтому пациентам с АФС и венозными тромбозами лечение варфарином должно проводиться более длительно (>12 мес), чем пациентам без АФС (3-6 мес).
Одна группа авторов при риске рецидивирования тромбозов (включая ишемический инсульт) у пациентов АФС рекомендует интенсивную антикоагуляцию варфарином, позволяющую поддерживать МНО на уровне >3,1 . В то же время другие авторы указывают на эффективность (особенно при венозных тромбозах) среднего уровня антикоагуляции, позволяющего поддерживать МНО на уровне 2,0-3,0 . M.A. Cronwther и соавт. провели рандомизированное двойное слепое контролируемое исследование, в котором сравнивалась эффективность и безопасность умеренной интенсивной (МНО 2-3) и высокоинтенсивной (МНО 3.1-4) антикоагуляции варфарином при АФС. В исследование было включено 114 пациентов с высоким/умеренным уровнем аФЛ и по крайней мере одним эпизодом тромбоза (венозного и артериального) в анамнезе; длительность лечения составила 2,7 года. За период наблюдения рецидивы тромбозов имели место у 6 из 56 (10,7%) пациентов, получавших высокоинтенсивную терапию, и у 2 из 58 (3,4%) получавших умеренно интенсивную терапию варфарином. Интересно, что частота тяжелых кровотечений в сравниваемых группах была примерно одинаковой (у 3 пациентов, которым проводили интенсивную антикоагуляцию, и у 4 - умеренную).
Таким образом, в настоящее время наиболее аргументировано использование варфарина в средних дозах (МНО 2,0-3,0) у пациентов с первым эпизодом венозного тромбоза в отсутствие других факторов риска рецидивирования тромбоэмболических осложнений, в то время как у пациентов с рецидивами тромбозов в анамнезе, вероятно, более оправдана интенсивная антикоагуляция (МНО >3,0).
Специального обсуждения заслуживает вопрос о применении варфарина у пациентов с АФС и ишемическим инсультом . Это связано с тем, что по данным многочисленных контролируемых исследований варфарин не имеет преимуществ перед АСК в отношении профилактики рецидивов инсульта в общей популяции пациентов с мозговыми инсультами и часто вызывает тяжелые интракраниальные кровотечения . Однако, по мнению многих авторов, при АФС риск повторных мозговых тромбозов выше, чем риск кровотечений . При этом риск кровотечений на фоне интенсивной антикоагуляции при АФС может быть в определенной степени компенсирован тем, что пациенты с этим синдромом, как правило, молодого возраста . По данным G. Ruiz-Irastorza и соавт. , у пациентов с АФС на фоне лечения варфарином частота «больших» кровотечений составила 6 случаев на 100 пациентов-год, ни в одном случае не было фатальных кровотечений, а интракраниальные геморрагии имели место только у 1 пациента. При этом рецидивы тромбозов развивались главным образом у пациентов, у которых наблюдалась недостаточная антикоагуляция (МНО< 3,0). Таким образом, вопрос об оптимальном уровне антикоагуляции у пациентов с АФС и с ишемическими инсультами остается открытым и должен решаться индивидуально как с учетом тяжести и факторов риска рецидивов тромбоза, так и риска кровотечений .
Следует подчеркнуть, что у многих пациентов с АФС наблюдаются спонтанные колебания МНО, затрудняющие подбор эффективной и безопасной дозы варфарина . При этом колебания МНО связаны с приемом лекарственных препаратов, влияющих на метаболизм варфарина, многие из которых широко используются в ревматологии (например, цитостатики, ГК, аллопуринол, НПВП, цефалоспорины и др.). Кроме того, колебания МНО могут быть связаны с различными свойствами тромбопластина, использующегося для определения протромбинового времени. Дозу непрямых антикоагулянтов сложно подбирать при наличии в крови ВА, присутствие которого иногда приводит к «ложно-положительным» результатам - к увеличению протромбинового времени и МНО in vitro , при отсутствии эффективной антикоагуляции in vivo . У пациентов с АФС нередко наблюдается резистентность к варфарину, которая имеет генетическую природу (мутация V и II факторов свертывания крови).
Т.М. Решетняк и соавт. изучалась эффективность варфарина у 20 больных (5 - мужчин и 15 - женщин) с АФС, среди которых у 8 был первичный АФС и 12 - АФС с СКВ. 18 пациентов получали варфарин в течение года, а двое - в течение 4 лет. Больные с артериальными тромбозами в анамнезе получали пентоксифиллин или низкие дозы АСК (50-100 мг/сутки).
Больные с АФС были разделены на три группы. В первую группу вошли 8 пациентов с целевым МНОЈ2,0, во вторую - 7 - с МНОЈ3,0 и в третью - 7 больных с МНОЈ2,0, получавших АСК (100 мг/сут) и пентоксифиллин (600 до 1200 мг/сут.). Рецидив венозного тромбоза имел место у двух больных с МНО<2,0. В других группах рецидивов не отмечено. Однако у 2-х пациентов 2 и 3 групп имели место «большие» кровотечения. Частота «малых» геморрагий в сравниваемых группах не различалась.
При недостаточной эффективности монотерапии варфарином возможно проведение комбинированной терапии непрямыми антикоагулянтами и низкими дозами АСК (и/или дипиридомола), которая наиболее оправдана у лиц молодого возраста без факторов риска кровотечений (вторичный АФС, тромбоцитопения, нарушения функции тромбоцитов, связанные с присутствием ВА, дефекты протромбина) .
В случае избыточной антикоагуляции (МНО>4,0) в отсутствие кровотечений рекомендуется временно отменить варфарин до того момента, когда значение МНО вернется к желаемому уровню . Более быстро нормализации МНО можно достигнуть путем введения небольших доз витамина К: 1 мг перорально (позволяет снизить риск по крайней мере «малых» кровотечений) или 0,5 мг внутривенно. Следует избегать назначения высоких доз витамина К, так как это может привести к длительной (в течение нескольких дней) резистентности к антагонистам витамина К. Подкожные инъекции витамина К не рекомендуются из-за выраженной вариабильности абсорбции. В случае гиперкоагуляции, сопровождающейся «большими» кровотечениями, введения только витамина К недостаточно, так как полный эффект развивается только через 12-24 часа после введения. В этом случае рекомендуется введение свежезамороженной плазмы или, что более предпочтительно, концентрата протромбинового комплекса.

Центральное место в лечении острых тромботических осложнений при АФС занимают прямые антикогулянты - гепарин и особенно препараты низкомолекулярного гепарина . Тактика применения прямых антикоагулянтов у пациентов с АФС не отличается от общепринятой:
Центральное место в лечении острых тромботических осложнений при АФС занимают прямые антикогулянты - гепарин и особенно препараты низкомолекулярного гепарина . Тактика применения прямых антикоагулянтов у пациентов с АФС не отличается от общепринятой:1. Определить базальный уровень АЧТВ, протромбиновое время и общий анализ крови.
2. Подтвердить отсутствие противопоказаний для гепаринотерапии.
3. Ввести внутривенно 5000 МЕ гепарина.
4. Решить вопрос о тактике гепаринотерапии.
Начать непрерывную внутривенную инфузию нефракционированного гепарина - 18 МЕ/кг/час (в среднем 30000/24 часа мужчине 70 кг веса):
Определять АЧТВ каждые 6 часов в течение первых 24 часов, затем ежедневно;
Поддерживать АЧТВ на уровне 1.5-2.5;
Продолжать инфузии в течение 5-7 дней.
Подкожное введение гепарина: начать с дозы 17500 МЕ каждые 12 часов (или 250 МЕ/кг каждые 12 часов).
5. Каждый день определять уровень тромбоцитов из-за возможности развития тромбоцитопении.
6. Если больные до этого не получали варфарин, то его следует назначить в течение первых 24-48 часов от начала гепаринотерапии.
7. Продолжить лечение гепарином по крайней мере в течение 4-5 дней после назначения варфарина. У пациентов с массивным илеофеморальным тромбозом или легочной тромбоэмболией лечение гепарином проводится в течение не менее 10 дней.
8. Прекратить введение гепарина при достижении МНО > 2 в течение 48 часов.
У пациентов с факторами риска рецидивирования тромбозов в течение длительного времени должна проводиться интенсивная профилактика с использованием низкомолекулярного гепарина.
Катастрофический антифосфолипидный синдром
Прогноз катастрофического АФС во многом зависит от того, насколько рано поставлен диагноз и начата «агрессивная» терапия. Для лечения «катастрофического» АФС
используется весь арсенал методов интенсивной и противовоспалительной терапии, применяемый для лечения критических состояний при ревматических болезнях (рис. 1) .

Рис. 1. Алгоритм лечения <катастрофического> АФС
Эффективность терапии в определенной степени зависит от возможности устранить факторы, провоцирующие его развитие (например, подавление инфекции и/или активности основного заболевания). При подозрении на наличие инфекции следует незамедлительно назначать антибактериальную терапию, а при развитии гангрены конечностей проводить ампутацию. Важное значение имеет «неспецифическая» интенсивная терапия, например, гемодиализ у пациентов с быстро развивающейся почечной недостаточностью, вентиляция легких, введение инотропных препаратов и др.
Проведение интенсивной терапии глюкокортикоидами направлено не на лечение самих «тромботических» нарушений, а определяется необходимостью курирования синдрома «системного воспалительного ответа». Напомним, что синдром системного воспалительного ответа характеризуется диффузным воспалением сосудистого эндотелия, связанным с гиперпродукцией ФНО-a и ИЛ-1. Целый ряд клинических проявлений АФС, связанных как с тромбозом мелких сосудов, так и распространенным некрозом (например, дыхательный дистресс-синдром у взрослых и др.), являются показаниями для назначения высоких доз глюкокортикоидов. Обычно рекомендуется проведение пульс-терапии по стандартной схеме (1000 мг метилпреднизолона в день в течение 3-5 дней) с последующим назначением высоких доз глюкокортикоидов (1-2 мг/кг/день) перорально. Следует еще раз подчеркнуть, что сами по себе глюкокортикоиды не влияют на риск развития повторных тромбозов.
Внутривенный иммуноглобулин вводится в дозе 0,4 г/кг в течение 4-5 дней и особенно эффективен при наличии тромбоцитопении. Следует, однако, помнить, что внутривенный иммуноглобулин может вызывать нарушение функции почек, особенно у лиц пожилого возраста, получавших нефротоксические препараты.
«Катастрофический» АФС является единственным абсолютным показанием для проведения сеансов плазмафереза (рекомендуется удаление 2-3 литров плазмы в течение 3-5 дней) у пациентов АФС, которые следует сочетать с максимально интенсивной антикоагулянтной терапией, использованием для замещения свежезамороженной плазмы, а при наличии показаний - с проведением пульс-терапии ГК и циклофосфамидом. Плазмаферез - метод выбора при тромботической тромбоцитопенической пурпуре и тромботической микроангиопатической гемолитической анемии, нередко осложняющей КАФС.
Циклофосфамид (0,5-1,0 г в сутки) в определенной степени показан при развитии катастрофического АФС на фоне обострения СКВ и для предотвращения синдрома «рикошета» после проведения сеансов плазмафереза.
Данные, касающиеся возможности применения антицитокинов (например, ингибитора ФНО-a ), отсутствуют. Теоретическим основанием для их применения являются данные о существенном повышении уровня ФНО-a при АФС, в том числе катастрофическом АФС. Вероятно, введение инфликсимаба может быть потенциально показано пациентом с синдромом системного воспалительного ответа на фоне АФС.
Патология беременности
Стандартом профилактики рецидивирующих потерь плода (а также венозных и артериальных тромбозов в послеродовом периоде) при АФС является применение низких доз АСК (81 мг/сут) в сочетании с нефракционированным гепарином или низкомолекулярным гепарином в течение всего периода беременности и по крайней мере в течение 6 мес. после родов (табл. 3).

Основными недостатками гепарина являются различная биодоступность при подкожном введении и его неспецифическое связывание с белками плазмы (АТ III и факторы коагуляции), тромбоцитарными белками (например, тромбоцитарный фактор 4) и ЭК. При этом некоторые гепарин-связывающие белки относятся к белкам острой фазы воспаления, концентрация которых существенно увеличивается на фоне воспаления. Наконец, еще одно ограничение гепаринотерапии - снижение способности гепарина инактивировать тромбин, находящийся в комплексе с фибрином и фактор Xa, связанный с активированными тромбоцитами в образующемся тромбе. Поэтому гепарин не оказывает влияния на рост тромба, а после прекращения гепаринотерапии может наблюдаться «рикошетное» усиление коагуляции.
Препараты низкомолекулярного гепарина обладают преимуществами перед нефракционированным гепарином при лечении венозных тромбозов и акушерской патологии у пациентов АФС и почти полностью вытеснили последний (табл. 4).

Недавно было проведено рандомизированное исследование, в котором сравнивалась эффективность низкомолекулярного гепарина в сочетании с АСК и внутривенным иммуноглобулином . В исследование было включено 30 женщин с 3 и более спонтанными абортами в анамнезе. У женщин, получавших гепарин и АСК, число успешных родов (84%) было выше, чем у женщин, получавших внутривенный иммуноглобулин (57%).
При родоразрешении кесаревым сечением введение низкомолекулярных гепаринов отменяется за 2-3 дня и возобновляется в послеродовом периоде с последующим переходом на прием непрямых антикоагулянтов. Лечение АСК и гепарином позволяет снизить риск венозных и артериальных тромбозов, которые нередко развиваются у пациентов с АФС на фоне и после беременности .
Необходимо иметь в виду, что длительная терапия гепарином беременных женщин может приводить к развитию остеопороза, осложняющегося переломами костей скелета. Для уменьшения потери костной массы необходимо рекомендовать прием карбоната кальция (1500 мг) в сочетании с витамином D. Лечение низкомолекулярным гепарином реже приводит к остеопорозу, чем лечение нефракционированным гепарином. Одним из ограничений для применения низкомолекулярного гепарина является опасность развития эпидуральной гематомы при проведении регионарной анестезии. Поэтому, если предполагаются преждевременные роды, лечение низкомолекулярным гепарином следует прекратить не позже, чем на 36-й неделе беременности.
Использование непрямых антикоагулянтов при беременности в принципе противопоказано, так как приводит к варфариновой эмбриопатии, характеризующейся нарушением роста эпифизов и гипоплазией носовой перегородки, а также неврологическими нарушениями. Однако по данным недавно проведенного исследования назначение варфарина между 15 и 34 неделями беременности пациенткам с АФС (n=14) не ассоциировалось с тератогенным эффектом , а частота успешных родов (86%) была такая же, как и у женщин, принимавших низкие дозы АСК и низкомолекулярный гепарин (87%). Эти данные позволяют предположить, что в некоторых случаях у пациенток, нуждающихся в активной антикоагулянтной терапии (но не переносящих лечение гепарином) или имеющих тяжелые системные тромбозы (инсульт и др.), возможно назначение варфарина в сроки от 14 до 34 недели беременности. У пациенток, которым проводится искусственное зачатие или индукция овуляции, необходимо заменить варфарин на гепарин. Гепарин следует отменить за 12-24 часа до проведения операции, а через 6-8 часов возобновить терапию.
Лечение средними/высокими дозами глюкокортикоидов (ГК), популярное в 80-х годах, в настоящее время практически не применяется из-за побочных эффектов как у матери, так и у плода и отсутствия доказательств их эффективности. Более того, глюкокортикоидная терапия приводит к развитию тяжелых побочных эффектов, включая преждевременный разрыв мембраны, преждевременные роды, задержку роста плода, инфекции, преэклампсию, диабет, остеопению и остеонекроз. Однако перед родами отменять ГК у женщин, получавших их во время беременности, не следует, а во время родов им необходимо дополнительно вводить внутривенно ГК, для того чтобы избежать надпочечниковой недостаточности. Применение ГК оправдано при вторичном АФС (в сочетании с СКВ) и направлено на лечение основного заболевания. Лишь в некоторых случаях у пациенток, у которых невынашивание беременности не удается преодолеть на фоне стандартной терапии низкими дозами АСК и гепарином (а также внутривенным иммуноглобулином), возможно назначение преднизолона (20-40 мг/сут).
Применение внутривенного иммуноглобулина (0,4 г/кг в течение 5 дней каждый мес.) не имеет преимуществ перед стандартным лечением АСК и гепарином и показано только при неэффективности «стандартной» терапии АСК и гепарином . Имеется несколько предварительных сообщений об определенной эффективности плазмафереза, однако в настоящее время этот метод используется крайне редко.
Следует подчеркнуть, что выявление аФЛ не влияет на исходы беременности у женщин, которым проводилось искусственное оплодотворение.

При соблюдении представленных рекомендаций удается увеличить частоту успешных родов у женщин с двумя и более эпизодами потери плода в анамнезе до 70-80%. Следует, однако, подчеркнуть, что даже в случае успешных родов у пациенток с АФС отмечается увеличение частоты преэкслампсии, задержки роста плода, преждевременных родов и других форм акушерской патологии. Дети у женщин с АФС, как правило, рождаются здоровыми, без признаков нарушения физического и нейропсихического развития, тромбозов и др., по крайней мере, в течение 5 лет наблюдения.
Гематологические нарушения
Умеренная тромбоцитопения, нередко наблюдающаяся у пациентов с АФС, не требует специального лечения. При вторичном АФС в рамках СКВ, тромбоцитопения обычно хорошо контролируется ГК, аминохинолиновыми препаратами, а в резистентных случаях - низкими дозами АСК.
Тактика лечения резистентной тяжелой тромбоцитопении (<50000/ мм 3), создающей угрозу кровотечений, до конца не разработана. Этим пациентам, наряду с применением ГК в высоких дозах, целесообразно назначение внутривенного иммуноглобулина. Имеются данные об определенной эффективности препарата даназол (слабый андроген) или дапсон.
В случае неэффективности высоких доз ГК методом «выбора» является спленэктомия , причем у подавляющего большинства пациентов отмечена стойкая нормализация уровня тромбоцитов.
Периоперационное ведение пациентов с АФС
У пациентов с АФС имеет место существенное увеличение риска тромбозов (особенно после операций на сосудах и клапанах сердца) и нередко развитие катастрофического АФС. В целом пациенты АФС составляют группу очень высокого риска развития венозных тромбоэмболических осложнений в послеоперационном периоде .
Развитие тромбозов в до- и послеоперационном периоде может быть связано со следующими факторами: <
- >
- Отменой непрямых антикоагулянтов
- Спонтанным увеличением свертываемости, несмотря на лечение варфарином или гепарином
- Развитием катастрофического АФС.
Кроме того, у некоторых пациентов имеет место очень высокая угроза некотролируемых кровотечений, развитие которых может быть связано со следующими причинами: <
- >
- Неадекватной антикоагулятной терапией
- Тромбоцитопенией
- Наличием дефицита факторов свертывания (например, синтезом высокоаффинных антител к протромбину).
Разработаны стандарты антикоагулянтной терапии для группы «высокого риска» , к которой относятся пациенты АФС (табл. 6). Следует, однако, подчеркнуть, что эти рекомендации специально не апробировались при АФС.

По мнению D. Erkan и соавт. , пациентам с АФС необходимо проводить более интенсивную антикоагулянтную терапию и свести к минимуму время, в течение которого антикоагулянтная терапия приостанавливается. У пациентов, которые в течение длительного времени применяли варфарин, препарат следует назначить сразу после операции при отсутствии хирургических противопоказаний. Лечение гепарином следует продолжить до стабилизации МНО на терапевтическом уровне.
В случае необходимости ургентных операций у пациентов с АФС, получающих варфарин, следует перелить свежезамороженную плазму (содержит все факторы свертывания, в том числе витамин К, дефицит которого развивается на фоне приема варфарина). Пациентам с тромбоцитопений (<50х10 9 /Л) или кровоточивостью следует назначать ГК и/или внутривенный иммуноглобулин. Переливание тромбоцитарной массы, как правило, не эффективно и может увеличивать риск развития тромбозов.
1. До операции
- Удлинение АЧТВ (или умеренно удлинение протромбинового времени) не является противопоказанием для хирургических операций
- При уровне тромбоцитов >10х10 9 /л специфической терапии не требуется
- Тромбоцитопения не снижает риск развития тромбозов
2 . Во время операции
- Минимизировать внутрисосудистые манипуляции
- Бинтовать конечности
- Помнить, что любое необъяснимое изменение состояния пациентов может быть связано с тромбозом
3 . Назначение антикоагулянтов
- Следует свести к минимуму промежуток времени без антикоагулянтной терапии
- Необходимо иметь в виду, что у пациентов с АФС могут развиться тромботические осложнения, несмотря на антикоагулянтную терапию
- Необходимо иметь в виду, что «стандартная» антикоагулянтная терапия может быть недостаточно эффективна при АФС
- Больные с АФС часто нуждаются в более агрессивной антикоагулянтной терапии
- Следует вести больных с АФС, имеющих акушерскую патологию, так, как если бы у них был сосудистый тромбоз
4 . Больные с трансплантированной почкой
- Следует проводить агрессивную антикоагулянтную терапию во время операции у всех пациентов с АФС (имеющих тромбоз в анамнезе)
- Тщательно взвесить необходимость антикоагулянтной терапии у «бессимптомных» пациентов с положительными результатами определения аФЛ.
- Назначение АСК позволяет снизить риск тромбозов, индуцированных циклоспорином А, по крайней мере у пациентов после пересадки почки.
Атеросклероз и артериальная гипертензия
Учитывая высокий риск атеросклеротического поражения сосудов при СКВ, и особенно при АФС, профилактика атеротромботических нарушений (как и при сахарном диабете) показана практически всем пациентам (табл. 7).

Для лечения сопутствующей артериальной гипертензии и сердечной недостаточности при АФС, вероятно, наиболее оправдано использование ингибиторов АПФ. Доказано, что терапия данными препаратами улучшает исход у пациентов с гипертонией, застойной сердечной недостаточностью и ИБС.
Перспективы фармакотерапии АФС
Очевидно, что высокий риск развития коронарной болезни сердца при АФС уже сам по себе является веским основанием для широкого применения статинов
у пациентов с этими заболеваниями. Однако учитывая данные об иммунных механизмах патогенеза атеротромбоза при СКВ и АФС, применение статинов при этих патологических состояниях имеет очень важные дополнительные патогенетические и клинические обоснования . Известно также, что статины оказывают профилактические действие не только в отношении ИМ, но и других сосудистых осложнений - инсульта и даже тромбоза глубоких вен голени, которые являются наиболее характерными клиническими проявлениями АФС.
Хотя эффективность антикоагулянтов и ингибиторов аггрегации тромбоцитов при АФС не вызывает сомнения, практическое использование этих препаратов имеет свои ограничения из-за недостаточно высокой эффективности, токсичности (или того и другого). Для «стандартных» антикоагулянтов характерно узкое «терапевтическое окно» (трудность достигнуть адекватной антикоагуляции без риска развития кровотечений), а также выраженная вариабельность терапевтического ответа у отдельных пациентов, что диктует необходимость тщательного лабораторного мониторинга. Все это вместе взятое послужило мощным стимулом для разработки новых антитромботических агентов . К ним относятся как уже широко применяющиеся в клинической практике тиоперидиновые ингибиторы АФД рецепторов (тиклопедин и клопидогрел) и ингибиторы тромбоцитарных (GPIIb/IIIa) рецепторов , так и новые антикоагулянты - прямые ингибиторы тромбина, ингибиторы фактора X, ингибиторы тканевого фактора (ТФ), рекомбинантный активированный белок С и др. (табл. 8 и рис. 2).


Рис. 2. Механизмы действия новых антикоагулянтов
В последние годы благодаря расшифровке структуры антигенов, которые являются мишенями для аФЛ, созданы реальные предпосылки для разработки «патогенетической» терапии этого заболевания. Одно из таких принципиально новых направлений фармакотерапии АФС, как аутоиммунной тромбофилии, связано с возможностью индукции специфической В-клеточной толерантности к потенциальным аутоантигенам, индуцирующим синтез «патогенных» аФЛ. Таким «патогенным» типом аутоантител при АФС могут быть антитела к b 2 -гликопротеину (ГП)-I.
Свойствами b 2 -ГП-I «толерагена» обладает препарат LJP 1082 . Он представляет собой рекомбинантную тетравалентную молекулу, состоящую из 4-х копий домена 1 b 2 -ГП-I человека (соединены полиэтиленгликольными мостиками), в котором присутствует, как полагают, основной В-клеточный «аутоэпитоп» этого антигена . Полагают, что LJP 1082 обладает способностью связываться с b 2 -ГПI-специфическими В-лимфоцитами и в отсутствие Т-клеточного сигнала индуцировать анергию или апоптоз В-клеток, синтезирующих антитела к b 2 -ГПI. Недавно было проведено несколько клинических испытаний (в рамках I/II фаз) , в которых продемонстрирована высокая безопасность и переносимость лечения этим препаратом.
Литература:1. Levine J, Branch DW, Rauch J. The antiphospholipid syndrome. N Engl J Med 2002; 346: 752-763
2. Алекберова ЗС, Насонов ЕЛ., Решетняк ТМ., Раденска-Лоповок СГ. Антифосфолипидный синдром: 15 лет изучения в России В кн: Избранные лекции по клинической ревматологии. Москва, Медицина. Под редакцией В.А.Насоновой, Н.В.Бунчука 2001, 132-148.
3. Cuadrado, MJ. Treatment and monitoring of patients with antiphospholipid antibodies and thrombotic history (Hughes syndrome). Curr Rheumatol Rep 2002; 4:392
4. Roubeu RAS. Treatment of the antiphospholipid syndrome. Curr Opin Rheumatol 2002; 14: 238-242
5. Ruiz-Irastorza G, Khamashta MA, Hughes GRV. Antiagregant and anticoagulant therapy in systemic lupus erythematosus and Hughes dyndrome. Lupus 2001;10: 241-245.
6. Derksen R.H,M., de Groot Ph G., Nieuwenhuis H,K,M Christiaens G,C.M.L. How to treat women with antiphospholipid antibodies in pregnancy. Ann. Rheum. Dis., 2001; 60: 1-3
7. Lockwood C.J., Schur P.H. Monitoring and treatment of pregnant women with the antiphospholipid antibody syndrome. UpToDate 2002; 10, No,2
8. Berman BL, Schur PH, Kaplan AA. Prognosis and therapy of the antiphospholipid antibody syndrome. UpToDate 2004; 11.3
9. Roubey RAS. New approaches to prevention of thrombosis in the antiphospholipid syndrome: hopes, trials, and tribulations. Arthritis Rheum 2003; 48: 3004-3008.
10. Насонов Е.Л. Современные подходы к профилактике и лечению антифосфолипидного синдрома. Терапевт архив 2003;5:83-88.
11. Petri M. Evidence-based management of thrombosis in the antiphospholipid antibody syndrome. Curr Rheumatol Report 2003; 5: 370-373.
12. Salmon JE, Roman MJ. Accelerated atherosclerosis in systemic lupus erythematosus: implication for patients management. Curr Opin Rheumatol 2001; 13: 341-344
13. Wajed J, Ahmad Y, Durrington PN, Bruce IN. Prevention of cardiovascular disease in systemic lupus erythematosus - proposed guidelines for risk factor management. Rheumatology 2004; 43: 7-12
14. Alarcon-Segovia D, Boffa MC, Branch W, et al. Prophylaxis of the antiphospholipid syndrome: a consensus report. Lupus 2003; 12: 499-503.
15. Erkan D, Merrill JT, Yazici Y et al. High Thrombosis rate after fetal loss in antiphospholipid syndrome: effective prophylaxis with aspirin. Arthr Rheum 2001; 44: 1466-1469.
16. Erkan D, Yazici Y, Peterson MG et al. A cross-sectional study of clinical thrombotic risk factors and preventive treatment in antiphospholipid syndrome. Rheumatology (Oxford) 2002; 41: 924-929.
17. Насонов Е.Л., Иванова М.М. Антималярийные (аминохинолиновые) препараты: новые фармакологические свойства и перспективы клинического применения Клин. фармакол. терапия 1998, 3:65-68.
18. Yoon KH. Sufficient evidence to consider hydroxychloroquine as an adjunct therapy in antiphospholipid antibody (Hughes`) syndrome. J. Rheumatol., 2002; 29; 1574-1575.
19. Meroni PL, Moia M, Derksen RHWM, et al. Venous thromboembolism in the antiphospholipid syndrome: management guidelines for second prophylaxis. Lupus 2003; 12: 504-507.
20. Brey RL, Chapman J, Levine SR et al. Stroke and the antiphospholipid syndrome: consensus meeting Taormina 2002. Lupus 2003; 12: 508-513.
21. Valentini KA, Hull RD. Clinical use of warfarin. UpToDate 2003; 12.1
22. Hirsh J, Fuster V, Ansell J, Halperin JL. American Heart Association/American College of Cardiology Foundation Guide to warfarin therapy. Circulation 2003; 107; 1692-1711.
23. van Dongen CJJ, Vink R, Hutten BA Buller HR, Prins MH. The incidence of recurrent venous thromboembolism after treatment with vitamin K antagonists in relation to time since first events. A meta-analysis. Arch Intern Med 2003; 163: 1285-1293.
24. Ruiz-Irastorza G, Khamashta MA, Caetellino G, Hughes GRV. Systemic lupus erythematosus. Lancet 2001; 357: 1027-1032.
25. Crowther MA, Ginsberg JS, Julian J, et al. A comparison of two intensities of warfarin for the prevention of recurrent thrombosis in patients with the antiphospholipid antibody syndrome. New Engl J Med 2003; 349: 1133-1138.
26. Adam HP. Emergent use of anticoagulantion for treatment of patients with ischemic stroke. Stroke 2002; 33: 856-861.
27. Sandercock P, Gubitz G, Foley P, Counsell C. antiplatelet therapy for acute ischemic stroke. Cochrane Database Syst Rev 2003; CD00029
28. Ruiz-Irastorza G, Khamashta M, Hunt B et al. Bleeding and recurrent thrombosis in definite antiphospholipid syndrome. Analysis of a series of 66 patients with oral anticoagulation to a target international normalization ratio of 3.5. Arch Untern Med, 2002; 162: 1164-1169.
29. Moll, S, Ortel, TL. Monitoring warfarin therapy in patients with lupus anticoagulants. Ann Intern Med 1997; 127:177.
30. Robert, A, Le Querrec, A, Delahousse, B, et al. Control of oral anticoagulation in patients with the antiphospholipid syndrome - Influence of the lupus anticoagulant on international normalized ratio. Thromb Haemost 1998; 80:99.
31. Tripodi, A, Chantarangkul, V, Clerici, M, et al. Laboratory control of oral anticoagulant treatment by the INR system in patients with the antiphospholipid syndrome and lupus anticoagulant. Results of a collaborative study involving nine commercial thromboplastins. Br J Haematol 2001; 115: 672.
32. Решетняк ТМ, Широкова ИЕ, Кондратьева ДВЮ и соавт. Варфарин в комплексной терапии антифосфолипидного синдрома: предварительные результаты. Науно-практическая ревматология 2003; 3: 37-41.
33. Shulman S. Care of patients receiving long-term anticoagulant therapy. New Engl J Med 2003; 349: 675-683.
34. Weitz J.I. Low-molecular-weight heparins. New Engl J Med 1997; 337: 688-698.
35. Aherson RA, Cervera R, de Groot P, Erkan D, et al. Catastrophic antiphospholipid syndrome (CAPS): International consensus statement on classifacation criteria and treatment guidelanes. Lupus 2003; 12: 530-544.
36. Erkan D, Cervra R, Asherson RA. Catastrophic antiphospholipid syndrome; where do we stand. Arthritis Rheum 2003; 48: 3320-327.
37. Lockwood CJ, Schur PH. Monitoring and treatment of
© Использование материалов сайта только по согласованию с администрацией.
Антифосфолипидный синдром (АФС) или синдром антифосфолипидных антител (САФА) четыре десятилетия назад не был известен даже врачам, не занимающихся данной проблемой, не говоря уже о пациентах. О нем заговорили только с начала 80-х прошлого века, когда симптомокомплекс во всех подробностях представил лондонский врач Грэм Хьюз, поэтому АФС можно встретить и под таким названием – синдром Хьюза (некоторые авторы именуют его синдромом Хьюджа, что, наверное, тоже правильно).
Чем же страшит эта болезнь медиков, пациентов и, особенно, женщин, мечтающих о материнстве? Все дело в действии антифосфолипидных антител (АФЛА), которые вызывают повышенное тромбообразование в венозных и артериальных сосудах кровеносной системы, чем осложняют течение беременности, провоцируют выкидыши и преждевременные роды, где плод нередко гибнет. К тому же, следует отметить, что сам синдром антифосфолипидных антител чаще выявляется у женской половины человечества, находящейся в репродуктивном возрасте (20 – 40 лет). Мужчинам в этом плане везет больше.
Основа развития синдрома фосфолипидных антител
Причиной формирования данного симптомокомплекса является появление антител (АТ), действие которых направлено на фосфолипиды, населяющие мембраны различных клеток многих тканей живого организма (кровяные пластинки – тромбоциты, нервные клетки, клетки эндотелия).
 Присутствующие на клеточных мембранах и выступающие в качестве антигена фосфолипиды, различаются по своему строению и способности давать иммунный ответ, поэтому подразделяются на виды, например, нейтральные и анионные (отрицательно заряженные) фосфолипиды – эти два класса встречаются наиболее часто.
Присутствующие на клеточных мембранах и выступающие в качестве антигена фосфолипиды, различаются по своему строению и способности давать иммунный ответ, поэтому подразделяются на виды, например, нейтральные и анионные (отрицательно заряженные) фосфолипиды – эти два класса встречаются наиболее часто.
Таким образом, если существуют различные классы фосфолипидов, то и антитела к ним будут представлять собой довольно разнообразное сообщество. Антифосфолипидные антитела (АФЛА) должны быть разной направленности, обладать способностью реагировать с теми или иными детерминантами (либо с анионными, либо с нейтральными). Наиболее известными, широко распространенными, имеющими важное клиническое значение считаются иммуноглобулины, по которым осуществляется диагностика АФС:
- Волчаночный антикоагулянт (иммуноглобулины классов G либо М – IgG, IgM) – эта популяция впервые была обнаружена у пациентов, страдающих СКВ (системная красная волчанка) и весьма склонных к тромбозам;
- Антитела к кардиолипиновому антигену , который является главным компонентом теста на сифилис, так называемой реакции Вассермана. Как правило, эти АТ представляют собой иммуноглобулины классов A, G, M;
- АТ, проявляющие себя в смеси холестерина, кардиолипина, фосфатидилхолина (ложноположительный результат реакции Вассермана);
- Бета-2-гликопротеин-1-кофакторзависимые АТ к фосфолипидам (суммарные иммуноглобулины классов A , G, M). Сам β-2-ГП-1 относится к естественным антикоагулянтам, то есть, к веществам, препятствующим ненужному образованию тромбов. Естественно, что появление иммуноглобулинов к бета-2-ГП-1 приводит к возникновению тромбозов.
Исследование антител к фосфолипидам очень важно в диагностике синдрома, ведь сама по себе она сопряжена с определенными трудностями.
Диагностика антифосфолипидного синдрома
Безусловно, антифосфолипидный синдром может быть заподозрен и по ряду клинических симптомов, однако окончательный диагноз должен быть установлен на основании сочетания симптомов и иммунологического обследования пациента, что подразумевает проведение определенного (и довольно широкого) перечня лабораторных анализов. Это и традиционные методы: общий (с подсчетом тромбоцитов) и биохимический анализ крови, включающий коагулограмму, и специфические тесты, направленные на выявление антител к фосфолипидам.

Недостаточное обследование (имеется в виду определение какого-то одного, чаще наиболее стандартизированного и доступного метода, которым, например, нередко считают антикардиолипиновый тест), скорее всего, приведет к гипердиагностике, ведь данный анализ дает позитивный результат и при других патологических состояниях.
Очень важными методами лабораторной диагностики на сегодняшний день является определение:
При антифосфолипидном синдроме могут поражаться различные сосуды: от капилляров до крупных артериальных стволов, расположенных в любых частях человеческого организма, поэтому спектр симптомов данной патологии чрезвычайно широк. Он затрагивает разнообразные сферы медицины, привлекая тем самым многих специалистов: ревматологов, неврологов, кардиологов, акушеров, дерматологов и др.
Тромбозы в венах и артериях
Чаще всего врачи сталкиваются с тромбозом, который носит рецидивирующий характер и поражает . Тромбы, там образованные, отрываясь, направляются в сосуды легких, закупоривают их, а это влечет возникновение такого опасного, а нередко и смертельного, состояния, как . Здесь все зависимо от размера пришедшего тромба и калибра сосуда, в котором этот тромб застрял. Если закрылся основной ствол легочной артерии (ЛА), то рассчитывать на благоприятный исход не приходится – рефлекторная остановка сердца приводит к мгновенной смерти человека. Случаи закупорки мелких ветвей ЛА дают шансы на выживание, однако не исключают геморрагии, легочную гипертензию, инфаркт легкого и развитие сердечной недостаточности, что также не «рисует» особо радужных перспектив.

На втором месте по частоте встречаемости можно поставить тромбозы в сосудах почек и печени с формированием соответствующих синдромов (нефротический, ).
Хотя и реже, но встречаются тромбозы подключичных вен или сосудов сетчатки, а также тромбоз, локализованный в центральной вене надпочечников, который вслед за геморрагиями и некрозом формирует у пациента хроническую надпочечниковую недостаточность.
В иных ситуациях (в зависимости от места расположения) тромбоз стоит в ряду пусковых механизмов возникновения .
Артериальные тромбозы дают явления ишемии с развитием некрозов. Словом, инфаркты, синдром дуги аорты, гангрена, асептический некроз бедренной головки – все это следствие артериального тромбоза.
АФС при беременности – сложная задача в акушерской практике
Синдром антифосфолипидных антител при беременности находится в списке особо трудных задач, поставленных перед акушерством, ведь треть женщин, пребывающих в предвкушении счастья материнства, вместо этого получают слезы и разочарования. Вообще, можно сказать, что акушерская патология вобрала в себя самые характерные, но довольно опасные черты синдрома антифосфолипидных антител:

- Невынашивание беременности, которое становится привычным;
- Рецидивирующие самопроизвольные выкидыши (1 триместр), риск которых возрастает пропорционально повышению иммуноглобулинов класса G к кардиолипиновому антигену;
- ФПН (фетоплацентарная недостаточность), создающая непригодные для нормального формирования нового организма условия, в результате чего – , задержка его развития, а нередко и гибель в утробе матери;
- с риском наступления преэклампсии, эклампсии;
- Хорея;
- Тромбозы (и в венах и в артериях), повторяющиеся вновь и вновь;
- Гипертензия беременных;
- Раннее начало и тяжелое течение заболевания;
- hellp-синдром – опасная патология 3 триместра (35 недель и дальше), неотложное состояние в акушерской практике (стремительное нарастание симптомов: рвота, боль в эпигастрии, головная боль, отеки);
- Раннее, несвоевременное отделение плаценты;
- Роды на сроках до 34 недель;
- Неудачные попытки ЭКО.
Старт развитию патологических изменений при беременности, конечно, дают тромбозы сосудов, ишемия плаценты, плацентарная недостаточность.
Важно – не пропустить!
Женщины с подобной патологией в период гестации требуют особого внимания и динамического наблюдения. Врач, который ведет ее, знает, что может грозить беременной и чем она рискует, поэтому назначает дополнительные обследования:
- с определенной периодичностью, чтобы всегда видеть, как ведет себя система свертывания крови;
- Ультразвуковое исследование плода с ;
- Ультразвуковую диагностику сосудов головы и шеи, глаз, почек, нижних конечностей;
- , чтобы избежать нежелательных изменений со стороны клапанов сердца.
Эти мероприятия производятся с целью не допустить развития тромбоцитопенической пурпуры, гемолитико-уремического синдрома и, конечно, такого грозного осложнения, как . Или исключить их, если у врача есть хоть малейшие сомнения.
Разумеется, наблюдением за развитием беременности у женщин с антифосфолипидным синдромом занимается не только врач акушерско-гинекологического профиля. С учетом того, что АФС заставляет страдать многие органы, к работе могут быть привлечены разные специалисты: ревматолог – в первую очередь, кардиолог, невролог и др.
Женщинам с АФС в течение гестационного периода показан прием глюкокортикостероидов и антиагрегантов (в небольших, назначенных врачом, дозировках!). Показаны также иммуноглобулины и гепарин, однако они применяются только под контролем коагулогаммы.
А вот девушкам и женщинам, которые уже знают о «своем АФС» и в дальнейшем планируют беременность, а сейчас думают пока «пожить для себя», хочется напомнить, что пероральные противозачаточные препараты им не подойдут, поскольку могут сослужить плохую службу, поэтому лучше попытаться найти другой способ контрацепции.
Влияние АФЛА на органы и системы
Что можно ожидать от синдрома АФЛА – предсказать довольно сложно, он способен создать опасную ситуацию в любом органе. Например, не остается в стороне от неприятных событий в организме головной мозг (ГМ). Тромбоз его артериальных сосудов является причиной таких заболеваний, как и рецидивирующий , которые могут иметь не только характерные для себя симптомы (парезы и параличи), но и сопровождаться:

- Судорожным синдромом;
- Деменцией, неуклонно прогрессирующей и загоняющей мозг пациента в «растительное» состояние;
- Различными (и часто весьма неприятными) расстройствами психики.
Кроме этого, при синдроме антифосфолипидных антител можно встретить и другую неврологическую симптоматику:
- Головные боли, напоминающие таковые при мигрени;
- Беспорядочные непроизвольные движения конечностей, характерные для хореи;
- Патологические процессы в спинном мозге, влекущие двигательные, чувствительные и тазовые расстройства, совпадающие по клинике с поперечным миелитом.
Патология сердца , обусловленная влиянием антифосфолипидных антител, может иметь не только выраженную симптоматику, но и серьезный прогноз в отношении сохранения здоровья и жизни, ведь неотложное состояние – инфаркт миокарда , является результатом тромбоза коронарных артерий, правда, если затрагиваются только самые мелкие ветви, то поначалу можно обойтись нарушением сократительной способности сердечной мышцы . АФС «принимает активное участие» в формировании клапанных пороков, в более редких случаях – способствует образованию внутрипредсердных тромбов и ведет диагностику по ложному пути, поскольку врачи начинают подозревать миксому сердца .
Немало неприятностей АФС может доставить и другим органам:

Многообразие симптомов, указывающих на поражение того или иного органа, часто позволяет антифосфолипидному синдрому протекать в разных формах, в виде псевдосиндромов , имитирующих другую патологию. Нередко он ведет себя, как васкулит, иногда проявляется как дебют рассеянного склероза, в одних случаях врачи начинают подозревать опухоль сердца, в других – нефрит или гепатит…
И немного о лечении…
Главной целью лечебных мероприятий является профилактика тромбоэмболических осложнений. Прежде всего, пациента предупреждают о важности соблюдения режима :
- Тяжести не поднимать, физическая нагрузка – посильная, умеренная;
- Длительное пребывание в неподвижной позе – недопустимо;
- Спортивные занятия даже с минимальным риском травмирования – крайне нежелательны;
- Авиаперелеты в течение длительного времени – настоятельно не рекомендованы, короткие путешествия – согласованы с врачом.
Лечение фармацевтическими средствами включает:

Лечение антиагрегантами и/или антикоагулянтами сопровождает пациента длительное время, а часть больных вынуждена «сидеть» на них вообще до конца жизни.
Прогноз при АФС не так уж плох, если соблюдать все рекомендации врачей. Ранняя диагностика, постоянная профилактика рецидивов, своевременное лечение (с должной ответственностью со стороны пациента) дают положительные результаты и вселяют надежду на долгую качественную жизнь без обострений, а также на благоприятное течение беременности и благополучные роды.
Сложности в прогностическом плане представляют такие неблагоприятные факторы, как сочетание АСФ + СКВ, тромбоцитопения, стойкая артериальная гипертензия, быстрое увеличение титров антител к кардиолипиновому антигену. Тут можно только тяжело вздохнуть: «Неисповедимы пути Господни…». Но это совсем не значит, что у больного так уж мало шансов…
Всех пациентов, имеющих уточненный диагноз «Антифосфолипидный синдром» ставят на учет у ревматолога, который наблюдает за течением процесса, периодически назначает анализы ( , серологические маркеры), проводит профилактику и при необходимости – лечение.
Обнаружили антифосфолипидные тела в анализе? Серьезно, но без паники…
В крови здоровых людей концентрация АФЛА обычно не показывает высокие результаты. Вместе с тем, нельзя также сказать, что у данной категории граждан они вовсе не выявляются. До 12% обследуемых людей могут иметь в своей крови АТ к фосфолипидам, но при этом ничем не болеть. Кстати, с возрастом частота обнаружения данных иммуноглобулинов, скорее всего, будет повышаться, что считается вполне естественным явлением.
А еще, иной раз бывают случаи, заставляющие некоторых особо впечатлительных людей изрядно поволноваться или вообще пережить шок. Например, пошел человек на какое-то обследование, предусматривающее проведение многих лабораторных тестов, в том числе, и анализ на сифилис. А проба оказывается положительной… Потом, конечно, все перепроверят и объяснят, что реакция была ложноположительной и, возможно, из-за присутствия в сыворотке крови антифосфолипидных антител. Однако, если подобное случается, то можно посоветовать не впадать в панику преждевременно, но и не успокаиваться окончательно, ведь антифосфолипидные антитела когда-нибудь могут и напомнить о себе.
Видео: лекции по АФС
Общая информация
О диагностике АФС
АФС и другие тромбофилии в акушерстве
Спасибо
Сайт предоставляет справочную информацию исключительно для ознакомления. Диагностику и лечение заболеваний нужно проходить под наблюдением специалиста. У всех препаратов имеются противопоказания. Консультация специалиста обязательна!
Антифосфолипидный синдром (АФС) , или синдром антифосфолипидных антител (САФА) , представляет собой клинико-лабораторный синдром, основными проявлениями которого являются образование тромбов (тромбозы) в венах и артериях различных органов и тканей, а также патология беременности. Конкретные клинические проявления антифосфолипидного синдрома зависят от того, сосуды какого именно органа оказались закупорены тромбами. В пораженном тромбозами органе могут развиваться инфаркты, инсульты , некрозы тканей, гангрена и т.д. К сожалению, на сегодняшний день отсутствуют единые стандарты профилактики и лечения антифосфолипидного синдрома вследствие того, что нет четкого понимания причин заболевания, а также нет каких-либо лабораторных и клинических признаков, позволяющих с высокой степенью достоверности судить о риске рецидива. Именно поэтому в настоящее время лечение антифосфолипидного синдрома направлено на уменьшение активности свертывающей системы крови, чтобы снизить риск повторных тромбозов органов и тканей. Такое лечение базируется на применении препаратов групп антикоагулянтов (Гепарины, Варфарин) и антиагрегантов (Аспирин и др.), которые позволяют профилактировать повторные тромбозы различных органов и тканей на фоне заболевания. Прием антикоагулянтов и антиагрегантов обычно производится пожизненно, поскольку такая терапия только предотвращает тромбозы, но не излечивает заболевание, позволяя, таким образом, продлить жизнь и поддерживать ее качество на приемлемом уровне.
Антифосфолипидный синдром – что это такое?
 Антифосфолипидный синдром (АФС) также называется синдромом Хьюджа
или синдромом антикардиолипиновых антител
. Данное заболевание было впервые выявлено и описано в 1986 году у пациентов, страдающих системной красной волчанкой . В настоящее время антифосфолипидный синдром относят к тромбофилиям
– группе заболеваний, характеризующихся усиленным образованием тромбов.
Антифосфолипидный синдром (АФС) также называется синдромом Хьюджа
или синдромом антикардиолипиновых антител
. Данное заболевание было впервые выявлено и описано в 1986 году у пациентов, страдающих системной красной волчанкой . В настоящее время антифосфолипидный синдром относят к тромбофилиям
– группе заболеваний, характеризующихся усиленным образованием тромбов.Антифосфолипидный синдром представляет собой аутоиммунное заболевание невоспалительного характера со своеобразным комплексом клинических и лабораторных признаков, в основе которого лежит образование антител к некоторым видам фосфолипидов, являющихся структурными компонентами мембран тромбоцитов , клеток кровеносных сосудов и нервных клеток. Такие антитела называются антифосфолипидными, и вырабатываются собственной иммунной системой, которая ошибочно принимает собственные структуры организма за чужеродные, и стремится уничтожить их. Именно из-за того, что в основе патогенеза антифосфолипидного синдрома лежит выработка антител иммунной системой против структур собственных клеток организма, заболевание относится к группе аутоиммунных.
Иммунная система может вырабатывать антитела на различные фосфолипиды, такие, как фосфатидилэтаноламин (ФЭ), фосфатидилхолин (ФХ), фосфатидилсерин (ФС), фосфатидилинозитол (ФИ), кардиолипин (дифосфатидилглицерол), фосфатидилглицерин, бета-2-гликопротеин 1, которые входят в состав мембран тромбоцитов, клеток нервной системы и кровеносных сосудов. Антифосфолипидные антитела "распознают" фосфолипиды, против которых они были выработаны, прикрепляются к ним, образуя на мембранах клеток крупные комплексы, активирующие работу свертывающей системы крови. Прикрепившиеся к мембранам клеток антитела выступают в качестве своего рода раздражителей для системы свертывания, поскольку имитируют неблагополучие в сосудистой стенке или на поверхности тромбоцитов, что вызывает активацию процесса свертывания крови или тромбоцитов, так как организм стремится устранить дефект в сосуде, "заделать" его. Такая активизация свертывающей системы или тромбоцитов приводит к образованию многочисленных тромбов в сосудах различных органов и систем. Дальнейшие клинические проявления антифосфолипидного синдрома зависят от того, сосуды какого именно органа оказались закупорены тромбами.
Антифосфолипидные антитела при антифосфолипидном синдроме являются лабораторным признаком заболевания и определяются, соответственно, лабораторными методами в сыворотке крови. Некоторые антитела определяют качественно (то есть устанавливают только тот факт, имеются они в крови, или нет), другие – количественно (определяют их концентрацию в крови).
 К антифосфолипидным антителам, которые выявляют при помощи лабораторных анализов в сыворотке крови, относят следующие:
К антифосфолипидным антителам, которые выявляют при помощи лабораторных анализов в сыворотке крови, относят следующие:
- Волчаночный антикоагулянт. Данный лабораторный показатель является количественным, то есть определяется концентрация волчаночного антикоагулянта в крови. В норме у здоровых людей волчаночный антикоагулянт может присутствовать в крови в концентрации 0,8 – 1,2 у.е. Повышение показателя выше 2,0 у.е. является признаком антифосфолипидного синдрома. Сам волчаночный антикоагулянт является не отдельным веществом, а представляет собой совокупность антифосфолипидных антител классов IgG и IgM к различным фосфолипидам клеток сосудов.
- Антитела к кардиолипину (IgA, IgM, IgG). Данный показатель является количественным. При антифосфолипидном синдроме уровень антител к кардиолипину в сыворотке крови более 12 Ед/мл, а в норме у здорового человека данные антитела могут присутствовать в концентрации менее 12 Ед/мл.
- Антитела к бета-2-гликопротеину (IgA, IgM, IgG). Данный показатель является количественным. При антифосфолипидном синдроме уровень антител к бета-2-гликопротеину повышается более 10 Ед/мл, а в норме у здорового человека данные антитела могут присутствовать в концентрации менее 10 Ед/мл.
- Антитела к различным фосфолипидам (кардиолипину, холестерину , фосфатидилхолину). Данный показатель является качественным, и определяется с помощью реакции Вассермана. Если реакция Вассермана дает положительный результат при отсутствии заболевания сифилисом , то это является диагностическим признаком антифосфолипидного синдрома.
Тем не менее, несмотря на широкий спектр клинических признаков антифосфолипидного синдрома, врачи выделяют ведущие симптомы заболевания, которые присутствуют всегда у любого человека, страдающего данной патологией. К ведущим симптомам антифосфолипидного синдрома относят венозные или артериальные тромбозы , патологию беременности (невынашивание беременности, привычные выкидыши , отслойка плаценты , внутриутробная гибель плода и др.) и тромбоцитопению (низкий уровень тромбоцитов в крови). Все остальные проявления антифосфолипидного синдрома комбинируются в топические синдромы (неврологический, гематологический, кожный, сердечно-сосудистый и др.) в зависимости от пораженного органа.
 Наиболее часто развиваются тромбозы глубоких вен голени, тромбоэмболия легочной артерии , инсульт (тромбоз сосудов мозга) и инфаркт миокарда (тромбоз сосудов сердечной мышцы). Тромбозы вен конечностей проявляются болью, отечностью, покраснением кожи , язвами на коже, а также гангреной в области закупоренных сосудов. Тромбоэмболия легочной артерии, инфаркт и инсульт являются жизнеугрожающими состояниями, которые проявляются резким ухудшением состояния.
Наиболее часто развиваются тромбозы глубоких вен голени, тромбоэмболия легочной артерии , инсульт (тромбоз сосудов мозга) и инфаркт миокарда (тромбоз сосудов сердечной мышцы). Тромбозы вен конечностей проявляются болью, отечностью, покраснением кожи , язвами на коже, а также гангреной в области закупоренных сосудов. Тромбоэмболия легочной артерии, инфаркт и инсульт являются жизнеугрожающими состояниями, которые проявляются резким ухудшением состояния.
Помимо этого, тромбозы могут развиваться в любых венах и артериях, вследствие чего у людей, страдающих антифосфолипидным синдромом, часто поражена кожа (трофические язвы , высыпания , похожие на сыпь, а также сине-фиолетовая неровная окраска кожи) и нарушено мозговое кровообращение (ухудшается память, появляются головные боли , развивается слабоумие). Если у женщины, страдающей антифосфолипидным синдромом, наступила беременность, то в 90% случаев она прерывается из-за тромбозов сосудов плаценты. При антифосфолипидном синдроме наблюдаются следующие осложнения беременности: самопроизвольные аборты , внутриутробная гибель плода, преждевременная отслойка плаценты, преждевременные роды, HELLP-синдром, преэклампсия и эклампсия .
Выделяют две основные разновидности антифосфолипидного синдрома – первичный и вторичный. Вторичный антифосфолипидный синдром всегда развивается на фоне какого-либо другого аутоиммунного (например, системная красная волчанка, склеродермия), ревматического (ревматоидный артрит и др.), онкологического (злокачественные опухоли любой локализации) или инфекционного заболевания (СПИД , сифилис, гепатит С и т.д.), или после приема лекарственных препаратов (оральные контрацептивы, психотропные средства, Изониазид и др.). Первичный антифосфолипидный синдром развивается на фоне отсутствия иных заболеваний, и его точные причины в настоящее время не установлены. Однако предполагается, что в развитии первичного антифосфолипидного синдрома играет роль наследственная предрасположенность, тяжелые хронические длительно текущие инфекции (СПИД, гепатиты и др.) и прием некоторых лекарств (Фенитоин , Гидралазин и др.).
Соответственно, причиной вторичного антифосфолипидного синдрома является имеющееся у человека заболевание, которое и спровоцировало увеличение концентрации антифосфолипидных антител в крови с последующим развитием патологии. А причины первичного антифосфолипидного синдрома неизвестны.
Несмотря на отсутствие знаний о точных причинах антифосфолипидного синдрома, врачи и ученые выявили ряд факторов, которые можно отнести к предрасполагающим для развития АФС. То есть условно данные предрасполагающие факторы можно считать причинами антифосфолипидного синдрома.
В настоящее время к предрасполагающим факторам антифосфолипидного синдрома относят следующие:
- Генетическая предрасположенность;
- Бактериальные или вирусные инфекции (стафилококковые и стрептококковые инфекции , туберкулез, СПИД, цитомегаловирусная инфекция , вирусы Эпштейна-Барр , гепатиты В и С, инфекционный мононуклеоз и т.д.);
- Аутоиммунные заболевания (системная красная волчанка, системная склеродермия, узелковый периартериит, аутоиммунная тромбоцитопеническая пурпура и др.);
- Ревматические заболевания (ревматоидный артрит и др.);
- Онкологические заболевания (злокачественные опухоли любой локализации);
- Некоторые заболевания ЦНС;
- Длительный прием некоторых лекарственных препаратов (оральные контрацептивы, психотропные средства, интерфероны , Гидралазин, Изониазид).
Антифосфолипидный синдром – признаки (симптомы, клиника)
Рассмотрим признаки катастрофического АФС и других форм заболевания по-отдельности. Такой подход представляется рациональным, поскольку по клиническим проявлениям различные виды антифосфолипидного синдрома одинаковы, а отличия имеются только у катастрофического АФС.Если тромбозы поражают мелкие сосуды, то это приводит к легким нарушениям функционирования органа, в котором находятся закупоренные вены и артерии. Например, при закупорке мелких сосудов миокарда отдельные небольшие участки сердечной мышцы теряют способность сокращаться, что вызывает их дистрофию , но не провоцирует инфаркт или иные тяжелые повреждения. Но если тромбоз захватывает просвет основных стволов коронарных сосудов, то произойдет инфаркт.
При тромбозах мелких сосудов симптоматика проявляется медленно, но степень расстройства функций пораженного органа неуклонно прогрессирует. При этом симптоматика обычно напоминает какое-либо хроническое заболевание, например, цирроз печени , болезнь Альцгеймера и т.д. Таково течение обычных типов антифосфолипидного синдрома. Но при тромбозе крупных сосудов происходит резкое нарушение работы органа, что вызывает катастрофическое течение антифосфолипидного синдрома с полиорганной недостаточностью, ДВС-синдромом и другими тяжелыми состояниями, опасными для жизни.
Поскольку тромбоз может затрагивать сосуды любого органа и ткани, в настоящее время описаны проявления антифосфолипидного синдрома со стороны центральной нервной системы, сердечно-сосудистой системы, печени, почек, желудочно-кишечного тракта, кожи и др. Тромбоз сосудов плаценты при беременности провоцирует акушерскую патологию (выкидыши, преждевременные роды, отслойку плаценты и др.). Рассмотрим симптоматику антифосфолипидного синдрома со стороны различных органов.
 Во-первых, необходимо знать, что тромбозы при АФС могут быть венозными и артериальными
. При венозном тромбозе тромбы локализуются в венах, а при артериальном, соответственно, в артериях. Характерной особенностью антифосфолипидного синдрома являются рецидивы тромбозов. То есть если не проводить лечение, то эпизоды тромбозов различных органов будут повторяться вновь и вновь, до тех пор, пока не наступит недостаточность какого-либо органа, несовместимая с жизнью. Также у АФС имеется еще одна особенность – если первый тромбоз был венозным, то и все последующие эпизоды тромбозов также бывают, как правило, венозными. Соответственно, если первый тромбоз был артериальным, то все последующие также будут захватывать артерии.
Во-первых, необходимо знать, что тромбозы при АФС могут быть венозными и артериальными
. При венозном тромбозе тромбы локализуются в венах, а при артериальном, соответственно, в артериях. Характерной особенностью антифосфолипидного синдрома являются рецидивы тромбозов. То есть если не проводить лечение, то эпизоды тромбозов различных органов будут повторяться вновь и вновь, до тех пор, пока не наступит недостаточность какого-либо органа, несовместимая с жизнью. Также у АФС имеется еще одна особенность – если первый тромбоз был венозным, то и все последующие эпизоды тромбозов также бывают, как правило, венозными. Соответственно, если первый тромбоз был артериальным, то все последующие также будут захватывать артерии.
Наиболее часто при АФС развиваются венозные тромбозы различных органов. При этом чаще всего тромбы локализуются в глубоких венах нижних конечностей, и несколько реже – в венах почек и печени. Тромбозы глубоких вен ног проявляются болями , отечностью, покраснением, гангреной или язвами на пораженной конечности. Тромбы из вен нижних конечностей могут отрываться от стенок сосудов и с током крови доходить до легочной артерии, провоцируя опасные для жизни осложнения – тромбоэмболию легочной артерии, легочную гипертензию , кровоизлияния в легкие . При тромбозе нижней или верхней полой вены развивается синдром соответствующей вены. Тромбоз вены надпочечников приводит к кровоизлияниям и некрозу тканей надпочечников и развитием их последующей недостаточности.
Тромбоз вен почек и печени приводит к развитию нефротического синдрома и синдрома Бадда-Киари. Нефротический синдром проявляется наличием белка в моче, отеками и нарушением обмена липидов и белков. Синдром Бадда-Киари проявляется облитерирующим флебитом и тромбофлебитом вен печени, а также выраженным увеличением размеров печени и селезенки, асцитом , усиливающейся с течением времени гепатоцеллюлярной недостаточностью и иногда гипокалиемией (низкий уровень калия в крови) и гипохолестеринемией (низкий уровень холестерина в крови).
При АФС тромбоз поражает не только вены, но и артерии. Причем артериальные тромбозы развиваются примерно в два раза чаще венозных. Такие артериальные тромбозы тяжелее по течению по сравнению с венозными, поскольку проявляются инфарктами или гипоксией мозга или сердца, а также расстройствами периферического кровотока (кровообращение в коже, конечностях). Наиболее часто встречается тромбоз внутримозговых артерий, вследствие которого развиваются инсульты, инфаркты, гипоксия и другие повреждения ЦНС. Тромбоз артерий конечностей приводит к гангрене, асептическому некрозу головки бедренной кости. Относительно редко развивается тромбоз больших артерий – брюшной аорты, восходящего отдела аорты и др.
Поражение нервной системы является одним из наиболее тяжелых проявлений антифосфолипидного синдрома. Вызывается тромбозом мозговых артерий. Проявляется транзиторными ишемическими атаками, ишемическими инсультами, ишемической энцефалопатией , судорогами , мигренью, хореей, поперечным миелитом , нейросенсорной тугоухостью и рядом других неврологических или психиатрических симптомов. Иногда неврологическая симптоматика при тромбозах сосудов мозга при АФС напоминает клиническую картину рассеянного склероза . В некоторых случаях тромбозы сосудов мозга вызывают временную слепоту или нейропатию зрительного нерва.
Транзиторные ишемические атаки проявляются потерей зрения , парестезией (ощущение бегания "мурашек", онемение), двигательной слабостью, головокружениями и общей амнезией . Нередко транзиторные ишемические атаки предшествуют инсульту, появляясь за несколько недель или месяцев до него. Частые ишемические атаки приводят к развитию слабоумия, потере памяти, ухудшению внимания и другим умственным нарушениям, которые похожи на болезнь Альцгеймера или токсическое поражение мозга.
Рецидивирующие микроинсульты при АФС часто протекают без четкой и заметной симптоматики, и могут проявляться через некоторое время судорогами и развитием слабоумия.
Головные боли также являются одним из наиболее частых проявлений антифосфолипидного синдрома при локализации тромбоза во внутримозговых артериях. При этом головные боли могут иметь различный характер – от мигренозных до постоянных.
Кроме того, вариантом поражения ЦНС при АФС является синдром Снеддона, который проявляется сочетанием артериальной гипертензии, сетчатого ливедо (сине-фиолетовая сетка на коже) и тромбоза сосудов мозга.
Поражение сердца при антифосфолипидном синдроме проявляется широким спектром различных нозологий, включая инфаркт, поражение клапанов, хроническую ишемическую кардиомиопатию , внутрисердечный тромбоз, повышенное артериальное давление и легочную гипертензию. В редких случаях тромбозы при АФС вызывают проявления, похожие на миксому (опухоль сердца). Инфаркт миокарда развивается примерно у 5% больных антифосфолипидным синдромом, причем, как правило, у мужчин младше 50-летнего возраста. Наиболее часто при АФС происходит поражение клапанов сердца, степень выраженности которого варьирует от минимальных нарушений (утолщение створок клапанов, заброс части крови обратно) до пороков (стеноз , недостаточность клапанов сердца).
Несмотря на то, что поражение сердечно-сосудистой системы при АФС развивается часто, оно редко приводит к сердечной недостаточности и тяжелым последствиям, требующим хирургической операции.
 Тромбоз сосудов почек
приводит к различным расстройствам функционирования данного органа. Так, наиболее часто при АФС отмечается протеинурия (белок в моче), которая не сопровождается какими-либо другими симптомами. Также при АФС возможно развитие почечной недостаточности с артериальной гипертензией. Любые нарушения работы почек при АФС обусловлены микротромбозом сосудов клубочков, который вызывает гломерулосклероз (замещение тканей почек рубцом). Микротромбозы клубочковых сосудов почек обозначаются термином "почечная тромботическая микроангиопатия".
Тромбоз сосудов почек
приводит к различным расстройствам функционирования данного органа. Так, наиболее часто при АФС отмечается протеинурия (белок в моче), которая не сопровождается какими-либо другими симптомами. Также при АФС возможно развитие почечной недостаточности с артериальной гипертензией. Любые нарушения работы почек при АФС обусловлены микротромбозом сосудов клубочков, который вызывает гломерулосклероз (замещение тканей почек рубцом). Микротромбозы клубочковых сосудов почек обозначаются термином "почечная тромботическая микроангиопатия".
Тромбоз сосудов печени при АФС приводит к развитию синдрома Бадда-Киари, инфаркту печени, асциту (выпот жидкости в брюшную полость), повышению активности АсАТ и АлАТ в крови, а также к увеличению размеров печени за счет ее гиперплазии и портальной гипертензии (повышенное давление в системе воротной вены печени).
При АФС примерно в 20% случаев отмечается специфическое поражение кожи из-за тромбозов мелких сосудов и нарушения периферического кровообращения. На коже появляется сетчатое ливедо (сосудистая сетка сине-фиолетового цвета, локализующаяся на голенях, ступнях, кистях, бедрах, и хорошо видимая при охлаждении), язвы, развивается гангрена пальцев рук и ног, а также множественные кровоизлияния в ногтевое ложе, которые по внешнему виду напоминают "занозу". Также иногда на коже появляется сыпь в виде точечных кровоизлияний, по внешнему виду напоминающая васкулит .
Также частым проявлением антифосфолипидного синдрома является акушерская патология , которая встречается у 80% беременных женщин, страдающих АФС. Как правило, АФС вызывает потерю беременности (выкидыш, замершая беременность , преждевременные роды), задержку внутриутробного развития плода, а также гестоз , преэклампсию и эклампсию.
Относительно редкими проявлениями АФС являются осложнения со стороны легких , такие, как тромботическая легочная гипертензия (повышенное кровяное давление в легких), кровоизлияния в легкие и капиллярит. Тромбозы легочных вен и артерий могут приводить к "шоковому" легкому – критическому для жизни состоянию, которое требует немедленного медицинского вмешательства.
Также редко при АФС развиваются желудочно-кишечные кровотечения , инфаркты селезенки, тромбозы мезентериальных сосудов кишки и асептические некрозы головки бедренной кости.
При АФС практически всегда имеется тромбоцитопения (количество тромбоцитов в крови ниже нормы), при которой количество тромбоцитов колеблется от 70 до 100 Г/л. Такая тромбоцитопения не требует лечения. Примерно в 10% случаев при АФС развивается Кумбс-положительная гемолитическая анемия или синдром Эванса (сочетание гемолитической анемии и тромбоцитопении).
Симптомы катастрофического антифосфолипидного синдрома
 Катастрофический антифосфолипидный синдром является видом заболевания, при котором происходит быстрое фатальное усиление нарушения функционирования различных органов из-за повторяющихся частых эпизодов массивных тромбозов. При этом в течение нескольких дней или недель развивается респираторный дистресс-синдром, нарушения мозгового и сердечного кровообращения, ступор, дезориентация во времени и пространстве, почечная, сердечная, гипофизарная или надпочечниковая недостаточность, которые при отсутствии лечения в 60% случаев приводят к гибели. Обычно катастрофический антифосфолипидный синдром развивается в ответ на заражение инфекционным заболеванием или перенесенную операцию.
Катастрофический антифосфолипидный синдром является видом заболевания, при котором происходит быстрое фатальное усиление нарушения функционирования различных органов из-за повторяющихся частых эпизодов массивных тромбозов. При этом в течение нескольких дней или недель развивается респираторный дистресс-синдром, нарушения мозгового и сердечного кровообращения, ступор, дезориентация во времени и пространстве, почечная, сердечная, гипофизарная или надпочечниковая недостаточность, которые при отсутствии лечения в 60% случаев приводят к гибели. Обычно катастрофический антифосфолипидный синдром развивается в ответ на заражение инфекционным заболеванием или перенесенную операцию.Антифосфолипидный синдром у мужчин, женщин и детей
Антифосфолипидный синдром может развиваться и у детей, и у взрослых. При этом детей данное заболевание встречается реже, чем у взрослых, но протекает тяжелее. У женщин антифосфолипидный синдром встречается в 5 раз чаще, чем у мужчин. Клинические проявления и принципы терапии заболевания одинаковы у мужчин, женщин и детей.Антифосфолипидный синдром и беременность
Что вызывает АФС при беременности?
 Антифосфолипидный синдром негативно сказывается на течении беременности и родов , поскольку приводит к тромбозам сосудов плаценты . Вследствие тромбоза сосудов плаценты возникают различные акушерские осложнения, такие, как внутриутробная гибель плода, фетоплацентарная недостаточность, задержка развития плода и т.д. Кроме того, АФС при беременности, помимо акушерских осложнений, может провоцировать тромбозы и других органов – то есть проявляться теми симптомами, которые характерны для данного заболевания и вне периода гестации. Тромбозы других органов также негативно сказываются на течении беременности, поскольку нарушается их функционирование.
Антифосфолипидный синдром негативно сказывается на течении беременности и родов , поскольку приводит к тромбозам сосудов плаценты . Вследствие тромбоза сосудов плаценты возникают различные акушерские осложнения, такие, как внутриутробная гибель плода, фетоплацентарная недостаточность, задержка развития плода и т.д. Кроме того, АФС при беременности, помимо акушерских осложнений, может провоцировать тромбозы и других органов – то есть проявляться теми симптомами, которые характерны для данного заболевания и вне периода гестации. Тромбозы других органов также негативно сказываются на течении беременности, поскольку нарушается их функционирование.В настоящее время доказано, что антифосфолипидный синдром может вызывать следующие акушерские осложнения:
- Бесплодие неясного происхождения;
- Неудачи ЭКО ;
- Выкидыши на ранних и поздних сроках беременности;
- Замершая беременность;
- Внутриутробная гибель плода;
- Преждевременные роды;
- Мертворождение;
- Пороки развития плода;
- Задержка развития плода;
- Гестозы;
- Эклампсия и преэклампсия;
- Преждевременная отслойка плаценты;
- Тромбозы и тромбоэмболии.
После наступления беременности врач выбирает одну из рекомендованных тактик , основанных на концентрации антифосфолипидных антител в крови и наличия тромбозов или осложнений беременности в прошлом. В целом золотым стандартом ведения беременности у женщин с АФС считается применение низкомолекулярных гепаринов (Клексан, Фраксипарин, Фрагмин), а также Аспирина в низких дозировках. Глюкокортикоидные гормоны (Дексаметазон , Метипред) в настоящее время не рекомендуется применять для ведения беременности при АФС, поскольку они оказывают незначительный лечебный эффект, но зато существенно повышают риск осложнений как для женщины, так и для плода. Единственные ситуации, когда применение глюкокортикоидных гормонов оправдано – это наличие иного аутоиммунного заболевания (например, системной красной волчанки), активность течения которого необходимо постоянно подавлять.
- Антифосфолипидный синдром, при котором у женщины в крови повышены уровни антифосфолипидных антител и волчаночного антикоагулянта, но в прошлом не было тромбозов и эпизодов потери беременности на ранних сроках (например, выкидыши, замершие беременности до 10 – 12 недель). В этом случае в течение всей беременности (до родов) рекомендуется принимать только Аспирин по 75 мг в сутки.
- Антифосфолипидный синдром, при котором у женщины в крови повышены уровни антифосфолипидных антител и волчаночного антикоагулянта, в прошлом не было тромбозов, но были эпизоды потери беременности на ранних сроках (выкидыши до 10 – 12 недель). В этом случае в течение всей беременности вплоть до родов рекомендуется принимать Аспирин по 75 мг в сутки, или комбинацию Аспирина 75 мг в сутки + препараты низкомолекулярного гепарина (Клексан, Фраксипарин, Фрагмин). Клексан вводят под кожу по 5000 – 7000 МЕ через каждые 12 часов, а Фраксипарин и Фрагмин – по 0,4 мг по одному разу в сутки.
- Антифосфолипидный синдром, при котором у женщины в крови повышены уровни антифосфолипидных антител и волчаночного антикоагулянта, в прошлом не было тромбозов, но были эпизоды замершей беременности на ранних сроках (выкидыши до 10 – 12 недель) или внутриутробной гибели плода, либо преждевременных родов вследствие гестоза или плацентарной недостаточности. В этом случае в течение всей беременности, вплоть до родов, следует применять низкие дозы Аспирина (по 75 мг в сутки) + препараты низкомолекулярного гепарина (Клексан, Фраксипарин, Фрагмин). Клексан вводят под кожу по 5000 – 7000 МЕ через каждые 12 часов, а Фраксипарин и Фрагмин – по 7500 – 10000 МЕ каждые 12 часов в первом триместре (до 12-ой недели включительно), и далее по 10000 МЕ каждые 8 – 12 часов во втором и третьем триместрах.
- Антифосфолипидный синдром, при котором у женщины в крови повышены уровни антифосфолипидных антител и волчаночного антикоагулянта, в прошлом были и тромбозы, и эпизоды потери беременности на любых сроках. В этом случае в течение всей беременности вплоть до родов следует применять низкие дозы Аспирина (по 75 мг в сутки) + препараты низкомолекулярного гепарина (Клексан, Фраксипарин, Фрагмин). Клексан вводят под кожу по 5000 – 7000 МЕ через каждые 12 часов, а Фраксипарин и Фрагмин – по 7500 – 10000 МЕ каждые 8 – 12 часов.
 Ведение беременности осуществляется врачом, который контролирует состояние плода, маточно-плацентарного кровотока и самой женщины. При необходимости врач корректирует дозировки препаратов в зависимости от значения показателей свертываемости крови. Указанная терапия обязательна для женщин с АФС во время беременности. Однако помимо данных препаратов, врач может назначать дополнительно и другие лекарственные средства, которые необходимы каждой конкретной женщине в текущий момент времени (например, препараты железа , Курантил и др.).
Ведение беременности осуществляется врачом, который контролирует состояние плода, маточно-плацентарного кровотока и самой женщины. При необходимости врач корректирует дозировки препаратов в зависимости от значения показателей свертываемости крови. Указанная терапия обязательна для женщин с АФС во время беременности. Однако помимо данных препаратов, врач может назначать дополнительно и другие лекарственные средства, которые необходимы каждой конкретной женщине в текущий момент времени (например, препараты железа , Курантил и др.).Так, всем женщинам с АФС, получающим во время беременности гепарины и Аспирин, рекомендуется вводить профилактически иммуноглобулин внутривенно по 0,4 г на 1 кг веса тела в течение пяти суток в начале каждого месяца, вплоть до родов. Иммуноглобулин профилактирует активизацию хронических и присоединения новых инфекций. Также рекомендуется женщинам, получающим гепарин, в течение всей беременности принимать препараты кальция и витамина D, чтобы предотвратить развитие остеопороза .
Применение Аспирина прекращают на 37-ой неделе беременности, а гепарины вводят вплоть до начала регулярной родовой деятельности, если роды ведут через естественные пути. Если назначено плановое кесарево сечение , то Аспирин отменяют за 10 дней, а гепарины за сутки до даты операции. Если гепарины применялись до начала родов, то таким женщинам нельзя давать эпидуральную анестезию .
После родоразрешения лечение, проводившееся во время беременности, продолжают еще 1 – 1,5 месяца. Причем возобновляют применением Аспирина и гепаринов через 6 – 12 часов после родов. Дополнительно после родов проводят мероприятия по профилактике тромбозов, для чего рекомендуется как можно раньше вставать с постели и активно двигаться, а также бинтовать ноги эластичными бинтами или надевать на них компрессионные чулки.
После 6-недельного применения гепаринов и Аспирина после родов дальнейшее лечение антифосфолипидного синдрома проводит врач-ревматолог , в компетенции которого и находится выявление и терапия данного заболевания. Через 6 недель после родов ревматолог отменяет гепарины и Аспирин, и назначает уже необходимое для дальнейшей жизни лечение.
В России в некоторых регионах распространена практика назначения беременным женщинам с АФС Вобэнзима
Несмотря на то что клинические рекомендации по диагностике, лечению антифосфолипидного синдрома разработаны ревматологами, к акушерству он имеет прямое отношение. Антифосфолипидный синдром при беременности приводит к привычному невынашиванию, что влечет за собой бездетность пары.
Антифосфолипидный синдром, или АФС – это патология, которая характеризуется повторяющимися тромбозами венозного, артериального, микроциркуляторного русла, патологией беременности с потерей плода и синтезом антифосфолипидных антител (афла): кардиолипиновых антител (аКЛ) и/или волчаночного антикоагулянта (ВА), и/или антител к бета2-гликопротеин Ⅰ. АФС – вариант часто приобретенной тромбофилии.
Код по МКБ 10 пересмотра – Д68.8.
Основой патогенеза антифосфолипидного синдрома является атака антителами мембран клеток. Чаще всего антифосфолипидный синдром развивается у женщин – в 5 раз чаще, чем у мужчин.
Манифестация синдрома происходит возникновением тромбозов, невынашиванием беременности. Часто до развития гестации женщины не подозревали о наличии этой патологии и присутствии антител в крови.
Классификация
Существует несколько вариантов антифосфолипидного синдрома. Основная классификация их такова:
- Первичный – связан с наследственными дефектами гемостаза.
- Вторичный АФС возник на фоне аутоиммунных болезней (ревматоидный артрит, системная красная волчанка), васкулитов, органоспецифичных патологий (сахарный диабет, болезни Крона), онкологических процессов, лекарственного воздействия, инфекций (ВИЧ, сифилис, малярия), при конечной стадии почечной недостаточности.
- Другие варианты АФС:
- серонегативный
- катастрофический
- другие микроангиопатические синдромы (ДВС-синдром, HELLP).
Причины невынашивания беременности

Патогенез развития акушерской патологии при АФС.
Доказано влияние АФС в развитии таких осложнений беременности:
- бесплодие неясного генеза;
- ранние преэмбриональные потери;
- неудачные ЭКО;
- выкидыши на разных сроках;
- внутриутробная гибель плода;
- послеродовая гибель плода;
- синдром задержки развития плода;
- преэклампсия и эклампсия;
- тромбозы во время беременности и после родов;
- пороки развития плода.
В послеродовом периоде у ребенка также возникают последствия антифосфолипидного синдрома: тромбозы, нейроциркуляторные расстройства с формированием аутизма в будущем. 20% детей, рожденных от матерей с АФС, в крови присутствуют антифосфолипидные антитела без симптомов, что говорит о внутриутробной передаче аФЛ.
Патогенетической основой развития всех проявлений АФС при беременности является плацентарная децидуальная васкулопатия, что вызывается недостатком продукции простагландина, тромбозами плаценты и нарушением механизма имплантации. Все эти механизмы препятствуют беременности.
Критерии диагноза

Выделяют критерии, по которым устанавливается диагноз «Антифосфолипидный синдром». Среди клинических критериев выделены следующие:
- Сосудистый тромбоз любой локализации: как венозный, так и артериальный, подтвержденный визуальными методами исследования. При использовании гистологического исследования в биоптатах должны отсутствовать признаки воспаления сосудистой стенки.
- Осложнения беременности:
- один или более эпизод гибели нормально развивающегося плода после 10 недель гестации или
- один или больше эпизодов преждевременных родов до 34 нед из-за значительной преэклампсии, эклампсии, плацентарной недостаточности или
- три или больше случаев подряд спонтанных абортов в сроке менее 10 недель, при отсутствии патологий анатомии матки, генетических мутаций, половых инфекций.
Лабораторные критерии таковы:
- В крови выявлены антитела к кардиолипину иммуноглобулины классов G и M в средних и высоких титрах, по крайней мере, 2 раза за 12 месяцев.
- Антитела к b2-гликопротеину I классов G и/или M в средних или высоких титрах, по крайней мере, 2 раза за год.
- Определен волчаночный антикоагулянт ВА в плазме в 2 более лабораторных исследованиях в промежутке хотя бы 12 месяцев. Заподозрить наличие ВА в крови можно при увеличении АЧТВ в коагулограмме в 2 и более раза.
Высокопозитивным считается анализ на антитела – 60 МЕ/мл, среднепозитивный ответ – 20-60 МЕ/мл, низкопозитивный – менее 20 МЕ/мл.
Для постановки диагноза «Антифосфолипидный синдром» необходимо присутствие одного клинического и одного лабораторного критерия.
Симптомы

Основным симптомом антифосфолипидного синдрома является тромбоз. У женщин эта патология проявляется невынашиванием беременности. Кроме таких очевидных признаков, у женщин могут проявляться дополнительные клинические критерии:
- сетчатое ливедо;
- наличие в анамнезе мигреней, хореи;
- трофические язвенные дефекты нижних конечностей;
- эндокардит и прочее.
Очень тяжело протекает катастрофическая форма антифосфолипидного синдрома. Она сопровождается клиникой острой почечной недостаточности, респираторным дистресс-синдромом, печеночной недостаточностью, нарушением мозгового кровотока, тромбозом крупных сосудов, в том числе и легочной артерии. Без срочной помощь прожить с этой формой длительно невозможно.
Лечение
Лечением АФС занимаются многие специалисты: ревматологи, гематологи, акушеры и гинекологи, кардиологи, кардиохирурги и прочие.
Первая группа пациентов
Пациенты, которые не имеют лабораторно выраженных признаков или клинических симптомов, не нуждаются в постоянном лабораторном контроле и непрерывной антикоагулянтной терапии. В этой группе пациентов проводят стандартную профилактику венозных тромбозов.
Вторая группа
У пациентов с высоким титром волчаночного антикоагулянта и/или антифосфолипидных антител более 10 МЕ/мл без тромбоза требуется назначение специфической профилактики – Аспирин в дозировке 75-100 мг один раз в день.
Третья группа
У этих людей результаты анализов на антитела отрицательны, но имеется подтвержденные случаи тромбоза и высокий риск их образования. У этих больных проводится лечение антикоагулянтами низкомолекулярного гепарина в терапевтических дозах. Сразу после постановки диагноза используют:
- Дальтепарин 100 МЕ/кг 2 раза в сутки;
- Надропарин 86 МЕ/кг или 0,1 мл на 10 кг 2 раза в день подкожно;
- Эноксапарин 1 мг/кг 2 раза в день подкожно;
- Со второго дня назначают Варфарин с 5 мг в сутки.
У пациентов этой группы проводят гепаринотерапию не менее 3 месяцев. В начале терапии выполняют контроль МНО каждые 4-5 дня для поддержания целевого значения в 2,0-3,0.
Четвертая группа
В эту группу входят люди, у которых тромбозы происходят на фоне повышенных титров волчаночного антикоагулянта и антифосфолипидного антитела. У этой категории больных назначается Варфарин и низкие доза (75-100 мг) Ацетилсалициловой кислоты. Пациенты с высоким уровнем риска должны получать пожизненно антикоагулянтную терапию.

Прегравидарная подготовка
Подготовка к беременности при АФС проводится в 2 последовательных этапа. На первом проводят оценку коагулограммы, определяют антигенный компоненты крови, удаляют и санируют инфекционные очаги.
Второй этап – это непосредственная подготовка к беременности и ее ведение. Для этого необходима антикоагулянтная терапия. Она проводится индивидуально в течение 1-2 менструальных циклов. Для этого нужно отнести женщину в одну из следующих групп:
- Серонегативный вариант АФС с наличием в анамнезе акушерских проявления синдрома. В сыворотке могут быть обнаружены только антитела к бета2-гликопротеину I. В этой группе проводят подготовку с помощью таких препаратов:
- один из препаратов низкомолекулярного гепарина 1 раз/сутки подкожно (дальтепарин (Фрагмин)120 антиХа МЕ/кг или эноксапарин (Клексан) 100 антиХа МЕ/кг;
- рыбий жир по 1-2 капсулы 3 раза/сутки;
- фолиевая кислота 4 мг/сутки;
- Если отсутствует волчаночный антикоагулянт, но присутствует АФЛА без тромбозов и акушерских клинических проявлений:
- при умеренном титре АФЛА назначается Аспирин 75-100 мг/сутки, а при развитии беременности он отменяется с заменой на дипиридомол 50-75 мг/сутки;
- при высоком и умеренном титре антифосфолипидного антигена комбинируют Ацетилсалициловую кислоту 75 мг/сутки и низкомолекулярный гепарин один раз в сутки подкожно;
- рыбий жир по 1-2 капсуле 3 раза в день;
- фолиевая кислота 4 мг/сутки.
- Если нет в крови волчаночного антикоагулянта, но есть в высоком или умеренном количестве антифосфолипидный антиген и имеется клиника тромбозов и акушерские осложнения:
- один из НМГ (Клексан, Фрагмин, Фраксипарин) 1 раз в сутки подкожно;
- Аспирин 75 мг/сутки с отменой его при развитии беременности и назначением Дипиридамола 50-75 мг/сутки;
- рыбий жир 1-2 капсулы 3 раза в день;
- фолиевая кислота 4 мг/сутки.
- В плазме женщины обнаружены АФЛА и определяется волчаночный антикоагулянт ВА от 1,5 до 2 усл.ед. До нормализации ВА следует воздержаться от беременности. Для нормализации ВА менее 1,2 усл.ед применяют:
- Клексан 100 антиХа МЕ/кг или Фрагмин 120 антиХа МЕ/кг один раз в сутки подкожно;
- рекомендован иммуноглобулин человеческий внутривенно 25 мл через день 3 дозы, повторяют введение препарата в 7-12 недель беременности, в 24 недели и последнее введение перед родами;
- после установления ВА в пределах нормы назначают Ацетилсалициловую кислоту 75 мг/сутки до наступления беременности;
- Клексан или Фрагмин один раз в день подкожно в прежних дозировках;
- рыбий жир 1-2 кап. 3 раза в день;
- фолиевая кислота 4 мг/кг.
- Если ВА в крови более 2 усл.ед, то зачатие откладывается минимум на 6-12 месяцев. Риск развития тромбоза у таких женщин очень велик. Целевое значение ВА – 1,2 усл.ед. Терапия проводится не менее 6 месяцев.
Лабораторная диагностика и обследование при планировании беременности обязательно включает такие показатели свертывания крови:
- тромбоциты – 150-400*10 9 /л;
- фибриноген – 2-4 г/л;
- МНО – 0,7-1,1;
- продукты деградации фибриногена и фибрина – менее 5 мкг/мл;
- д-димеры – менее 0,5 мкг/мл;
- растворимые фибринмономерные комплексы должны отсутствовать;
- протеин С – 69,1-134,1%;
- антитромбин Ⅲ – 80-120%;
- агрегационная активность тромбоцитов с солью аденозиндифосфата – 50-80%, с гидрохлоридом адреналина – 50-80%;
- антикардиолипиновые антитела – все классы иммуноглобулинов менее 10 МЕ/мл;
- ВА – отрицательный или менее 0,8-1,2 усл.ед;
- гипергомоцистеинемия – отрицательная;
- мутация FV (Leiden) гена, ответственного за синтез фактора V, или мутация G20210A гена, ответственного за синтез фактора II – отсутствует;
- общий анализ мочи для определения гематурии;
- контроль за развитием инфекционных болезней: лимфоциты, СОЭ.
Ведение беременности при АФС
Чтобы во время беременности не возникало тромбозов и потери плода, необходима профилактика – немедикаментозная и медикаментозная.
Немедикаментозная:
- физическая активность стимулирует собственный тканевой плазминоген;
- эластичный медицинский трикотаж 1-2 класс компрессии;
- диета с большим количеством растительных масел, свеклы, чернослива, инжира, бананов, поскольку эти продукты обладают слабительным эффектом – это важно, чтобы при дефекации не создавать повышенное давление на стенки вен.
Медикаментозная профилактика тромбозов при беременности
Существует несколько вариантов профилактики в зависимости от течения антифосфолипидного синдрома.
- Отсутствуют серологические маркеры ВА и антикардиолипиновый антиген, тромботические осложнения, могут определяться антитела к бета2-гликопротеину I.
- В первом триместре назначают Клексан или Фрагмин в дозировке для оптимального поддержания д-димеров и фолиевая кислота 4 мг/кг.
- Второй и третий триместры – Фригмин или Клексан до нормальных цифр д-димеров, рыбий жир, Аспирин 75-100 мг/кг при повышенной агрегации тромбоцитов, СЗП 10 мл/кг или концентрат антитромбина при снижени антитромбина 3 менее 80%.
- Перед родами Аспирин отменяют за 3-5 суток, вечернюю дозу НМГ меняют на СЗП 10мг/кг с гепарином 1-2 Ед на каждый мл СЗП.
- При родоразрешении – нормальный уровень д-димеров СЗП 10 мг/кг, при высоком уровне перед операцией – СЗП 5 мл/кг плюс гепарин 1 Ед на 1 мл СЗП или концентрат антитромбина 3, во время операции СЗП 5 мл/кг.
- При наличии в крови АФЛА и тромбозами или без них, отсутствует волчаночный антикоагулянт.
- 1 триместр – Клесан или Фрагмин для поддержания нормального уровня д-димеров+фолиевая кислота 4 мг/сутки.
- 2 и 3 триместры – Клексан или Фрагмин в индивидуальных дозировках+Аспирин 75 мг/сутки+рыбий жир 1-2 кап 3 раза в день, при снижении антитромбина 3 менее 80% активности – СЗП 10 мл/кг или концентрат антитромбина Ⅲ – 10-50 МЕ/кг, при повышении д-димеров более 0,5 мкг/мл – повышении дозировки НМГ.
- Перед родами – отмена Аспирина за 3-5 дней, НМГ заменяют на СЗП 10 мл/кг+НФГ 1-2 ЕД на каждый мл СЗП, при повышении антифосфолипидных антител назначается Преднизолон (Метилпред) 1-1,5 мг/кг внутривенно.
- При родоразрешении если нормальные D-димеры – СЗП 10 мл/кг; если повышены д-димеры, то до операции СЗП 5 мл/кг+НФГ 1 ед на каждый мл CPG или концентрат антитромбина 3, во время операции – СЗП 5 мл/кг, при значительном повышении антител – Преднизолон 1,5-2 мл/кг внутривенно.
- При повышении ВА от 1,5 до 2 усл.ед.
- 1 триместр – базовый прием Фрагмин или Клексана в дозе, как в прошлом варианте+фолиевая кислота+иммуноглобулин человеческий 25 мл через день 3 дозы в 7-12 нед. Если имеется повышение ВА более 1,5 усл.ед в первом триместре, то беременность стоить прервать.
- 2 и 3 триместр – Фрагмин и Клексан в дозировке для нормального поддержания д-димеров+Аспирин 75 мг+рыбий жир 1-2 кап 3 раза в день, при сниженном антитромбине – СЗП 10 мл/кг или концентрат антитромбина Ⅲ 10-50 МЕ/кг в/в, при повышении Д-димеров – повысить дозировку НМГ, иммуноглобулин 25 мл через 1 день 3 раза в 24 недели, если повышен ВА от 1,2 до 2 усл.ед – Преднизолон 30-60 мг/сут в/в, с 13 до 34 недели возможен перевод на Варфарин под контролем МНО.
- Перед родами если был Варфарин, то его отменяют за 2-3 нед, переводят на НМГ, Аспирин отменяется за 3-5 дней до родов, СЗП 10 мл/кг+НФГ 2 ед на каждый мл плазмы, Преднизолон – 1,5-2 мл/кг в/в, при сниженном антитромбине Ⅲ – концентрат антитромбина Ⅲ 10-30 МЕ/кг.
- При родах – до операции СЗП 500 мл+НФГ 1000 ЕД, во время операции – СЗП 10 мл/кг, Преднизолон 1,5-2 мг/кг в/в.
- При повышении ВА более 2 усл.ед беременность следует прерывать.
Если у женщины развился катастрофический антифосфолипидный или HELLP-синдром, то может быть назначен плазмоферез или плазмофильтрация.
Послеродовый период
После родоразрешения возобновить профилактику тромбоэмболии следует уже спустя 8-12 часов Фраксипарином (Надропарином) – 0,1 мл/10 кг, Клексан (Эноксапарин) 100 МЕ/кг, Фрагмин (Дальтепарин) 120 МЕ/кг, если нет кровотечения.
Если у женщины были отмечены тромбозы в анамнезе, то назначаются терапевтические дозы этих средств Фраксипарин – 0,1 мл/10 кг 2 раза в день, Клексан – 100 МЕ/кг 2 раза в день, Фрагмин – 120 МЕ/кг 2 раза в день.
Применение НМГ необходимо продолжать не меньше 10 дней. А если был эпизод доказанной тромбоэмболии, то антикоагулянты используются не менее 3-6 месяцев.
Повышение концентрации антигенов в крови требует консультации гематолога или ревматолога для решения вопроса о гормональной терапии.
Цена на анализы
Чтобы выявить АФС, можно пройти диагностику на платной основе. Многие частные лаборатории предлагают панель для определения антифосфолипидных антител. В лаборатории Инвитро в Москве цены на конец 2018 года таковы:
- обнаружение иммуноглобулинов G и M к кардиолипину стоит 1990 руб;
- диагностика вторичного АФС – цена 3170 руб;
- развернутое серологическое исследование на АФС – 4200 руб;
- лабораторные критерии АФС – 3950 руб.
В лаборатории Синэво в Москве цены на анализы этой панели несколько разняться:
- иммуноглобулинов G и M к кардиолипину – 960 руб;
- антитела к бета2-гликопротеиду I – 720 руб;
- антитела класса G к фосфолипидам – 720 руб;
- антитела класса M к фосфолипидам – 720 руб.
Примерно такие цены могут предложить и другие частные лаборатории в городах России.