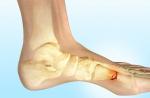
(ОП) и хронического панкреатита (ХП) одним из ведущих механизмов являются активация панкреатических ферментов, в первую очередь трипсина, и «самопереваривание» ткани поджелудочной железы. Трипсин вызывает коагуляционный некроз ацинарной ткани с лейкоцитарной инфильтрацией. В свою очередь А- и В-фосфолипазы разрушают фосфолипидный слой мембран и клеток, эластаза - на эластический «каркас» стенок сосудов. Кроме того, активация калликреина и других вазоактивных веществ способствует повышению сосудистой проницаемости, что приводит к геморрагическому пропитыванию ткани поджелудочной железы.
Преждевременная активация трипсина из трипсиногена в протоках поджелудочной железы осуществляется комплексом компонентов дуоденального содержимого, попадающего из двенадцатиперстной кишки при ее дискинезии и являющегося смесью активированных панкреатических ферментов, желчных солей, лизолецитина, эмульгированного жира и бактериальной флоры (H.Schmidt, 1976). При наличии воспалительного процесса в поджелудочной железе и препятствия для оттока панкреатического сока активация трипсина, химотрипсина и эластазы может происходить уже в самой железе.
По происхождению различают первичный и вторичный ХП
- При первичном ХП воспалительно-деструктивный процесс локализуется изначально в поджелудочной железе. Первичный ХП развивается на фоне ОП, травм, аллергии, сужения главного протока поджелудочной железы, хронического алкоголизма, нарушения кровообращения.
- Вторичный ХП обусловлен патологией соседних органов, нарушающей функционирование поджелудочной железы (желчнокаменная болезнь, язвенная болезнь, дивертикулы двенадцатиперстной кишки и т.д.).
ХП, по мнению многих исследователей, чаще является следствием перенесенного ОП. У большинства больных ХП (60 % - по P.Mallet-Guy) острая фаза панкреатита остается нераспознанной, так как у них ошибочно вместо ОП устанавливают диагноз пищевой токсикоинфекции, желчнокаменной болезни, холецистита, аппендицита и др. Иногда, например в условиях хронической пищевой, прежде всего белковой, недостаточности, возникает первичный ХП без приступов ОП в анамнезе.
В.М.Данилов и В.Д.Федоров, (1995) считают, что у большинства больных ХП и ОП являются заболеваниями с единым патогенезом и что, как правило, при этих заболеваниях речь идет о едином воспалительно-дегенеративном процессе в поджелудочной железе. Концепция, рассматривающая ОП и ХП как два самостоятельных заболевания, которые характеризуются различным патогенезом, отвергнута тщательно проведенными исследованиями Y.Kloppel, B.Maillet (1991), Д.С.Саркисова и соавторов, 1985, в которых определены этапы перехода ОП в ХП и описаны ряд общих для них морфологических признаков.
Y.Kloppel и B.Mailet (1986, 1992) на основании ретроспективных анатомо-морфологических и гистологических исследований предположили, что ХП является следствием повторных эпизодов ОП. По данным их исследований, макро- и микроскопические изменения поджелудочной железы у больных с ОП и ХП, вызванным алкоголем очень сходны. Одним из основных изменений в тканях поджелудочной железы авторы считают некроз пери- и интрапанкреатической жировой основы, что ведет к развитию фиброзной ткани, формированию псевдокист, стенозу протоков поджелудочной железы. Обструкция в протоковой системе поджелудочной железы вызывает сгущение и преципитацию белков в соке поджелудочной железы и в дальнейшем - образование камней. Эти данные подтверждены исследованиями, проведенными в Цюрихе (R.W.Amman и соавт., 1994). Очаги стеатонекроза в поджелудочной железе даже при отечной форме панкреатита могут приводить к развитию рубцовой ткани и обструктивным явлениям в ее протоковой системе. Отличительной особенностью предложенной гипотезы является тот факт, что первичные в развитии ХП - патоморфологические изменения в тканях поджелудочной железы, ведущие к сужению и обструкции протоковой системы, вторичные - образование преципитатов и камней.
В патоморфологической основе ХП лежит сочетание деструкции ацинарного аппарата с прогрессирующим хроническим воспалительным процессом, приводящим к атрофии и нарушениям в протоковой системе поджелудочной железы, преимущественно за счет развития стриктур, микро- и макролитиаза. Отмечаются также затруднения лимфооттока (вначале - вследствие отека, а затем - и склеротических изменений ацинарной ткани), нарушения микроциркуляции за счет образования в капиллярах фибринных нитей и микротромбирования. Одновременно происходит уплотнение поджелудочной железы вследствие разрастания соединительной ткани, фиброза железы.
По мере прогрессирования воспалительно-дегенеративных изменений, склероза паренхимы поджелудочной железы, облитерации протоковой системы вначале нарушается ее экзокринная, затем эндокринная функция. Этот процесс, как правило, протекает фазово, с чередованием периодов обострения, сопровождающихся деструкцией ткани поджелудочной железы, и периодов относительного благополучия, когда поврежденная паренхима органа замещается соединительной тканью.
При ХП периодически возникают обострения, напоминающие по морфологической и патофизиологической картине острого панкреатита, которые сменяются ремиссиями. Каждое такое обострение является причиной быстрого прогрессирования заболевания. Во время обострений хронического панкреатита преимущественно повреждается дольчатая ткань поджелудочной железы, осуществляющая экзокринную функцию. При фиброзе поражаются и дольки, и панкреатические островки, что обусловливает прогрессирующие нарушения как экзо-, так и эндокринной функции. Все вышеперечисленные изменения постепенно нарастают, параллельно этому снижаются функциональные резервы поджелудочной железы, которые затем проявляются клинически в виде ее экзо- и эндокринной недостаточности.
По некоторым данным (Stephen Holt, 1993), экзокринная недостаточность проявляется клинически при деструкции 90% паренхимы железы. Для поздних стадий ХП характерна триада:
- кальцификация железы,
- сахарный диабет,
- стеаторея.
Стеаторея появляется, когда продукция липазы поджелудочной железой падает ниже 16% ее нормального уровня.
Таким образом, ХП в настоящее время рассматривается чаще не как самостоятельное заболевание, а как продолжение и исход ОП, что соответствует так называемой фиброзно-некротической теории развития ХП. У 10 % больных ОП переходит в ХП непосредственно после первого приступа ОП, у 20 % - между приступом ОП и развитием ХП имеется длительный латентный период (от 1 года до 20 лет), у 70 % больных ХП выявляют после нескольких приступов ОП. Его развитию в первую очередь способствуют хронический алкоголизм, холедохолитиаз, хронические заболевания желудка и кишок (язвенная болезнь, папиллит, папиллостеноз, дуоденостаз), атеросклеротическое поражение сосудов поджелудочной железы и некоторые другие факторы в меньшей степени.
Ранние стадии хронического панкреатита
При патологоанатомическом исследовании в относительно ранней стадии ХП выявляют в разной степени выраженное увеличение поджелудочной железы, относительно небольшое неравномерное уплотнение ее ткани, отек, некроз, кровоизлияния, псевдокисты, свидетельствующие о бывших ранее острых приступах. Одновременно обнаруживают как признаки острого воспаления, обычно свойственные ОП, так и хронического, в частности, фиброз долек или межуточной ткани, выраженную клеточную инфильтрацию с отложением гемосидерина и микролитов. Эти изменения распространяются и на протоки поджелудочной железы, эпителий которых метаплазирован, слущен, закупоривает их просветы. В начальный период заболевания патологический процесс может носить ограниченный (очаговый) характер и не распространяться на всю железу: левосторонний, правосторонний, парамедианный ХП (P.Mallet-Guy, 1960).
Поздние стадии хронического панкреатита
В поздних стадиях ХП поджелудочная железа, как правило, неравномерно увеличена, плотная, нередко с псевдокистами, наполненными бесцветной или желтовато-коричневатой окраски жидкостью, спаяна с соседними органами за счет фиброзных изменений в парапанкреатической клетчатке, прилегающие вены нередко тромбированы. Строма органа представлена разрастаниями широких пластов соединительной ткани разной степени зрелости, в части случаев имеются отложения извести как в просвете протоков в виде зернистых камней белесовато-желтого цвета, так и среди разрастаний фиброзной ткани в местах бывшего некроза паренхимы. Объем экзокринной паренхимы резко уменьшен.
Облитерация и отложение внутри протоков извести обусловливают образование ретенционных кист. При вскрытии главного протока поджелудочной железы обращает на себя внимание наличие неравномерных сужений и расширений его просвета. L.Leger (1961) выделяет следующие разновидности расширения протоков железы по их преимущественной локализации: дилятацию на всем протяжении, эктазию в области головки, корпокаудальное образование псевдокист.
Конечная стадия хронического панкреатита
В конечной стадии ХП поджелудочная железа атрофична, уменьшена в объеме, деревянистой плотности. Часто выявляются диффузные внутридольковые и внутрипротоковые кальцинаты.
Таким образом, патоморфологические изменения при ХП характеризуются сочетанием склеротических, атрофических и регенеративных процессов, которые нередко сопровождаются обызвествлениями паренхимы органа и образованием истинных и ложных кист. Поэтому выделяют несколько патоморфологических вариантов ХП:
- индуративный,
- кистозный,
- псевдотуморозный.
Индуратаивный хронический панкреатит
Индуративный ХП у большинства больных развивается вскоре после перенесенного ОП и проявляется диффузным разрастанием соединительной ткани с одновременной атрофией паренхимы железы и расширением ее протоков. Возникающие при остром воспалительном процессе кровоизлияния и очаговые жировые некрозы в дальнейшем организуются в большинстве случаев с отложением кальциевых солей и гидроокиси апатитов в очаги разнообразных по форме и размерам обызвествлений.
Кистозный хронический панкреатит
Кистозный ХП характеризуется как рубцовыми сужениями протоков поджелудочной железы с нарушением оттока панкреатического сока и дилятацией дистальных отделов главного протока поджелудочной железы, так и развитием псевдокист в зоне некроза железы.
Псевдотуморозный хронический панкреатит
Псевдотуморозный ХП обусловлен преобладанием гиперпластического воспалительного процесса и сопровождается увеличением объема всей железы или ее части. Гиперпластический процесс чаще захватывает головку поджелудочной железы и сочетается с развитием в ней фиброзных уплотнений, мелких очагов обызвествлений и небольших кист.
В начальной стадии ХП доминирует абдоминальный болевой синдром, который развивается прежде всего вследствие внутрипротоковой гипертензии в поджелудочной железе и панкреатит-ассоциированного неврита. Характерны и такие осложнения, как псевдокисты, желтуха, компрессия двенадцатиперстной кишки с ее непроходимостью, панкреатический асцит, плевральный выпот.
Клинически выраженная желтуха может выявляться у 8% больных (А.А.Шалимов и соавт., 1997). Причинами возникновения желтухи у больных ХП могут быть: компрессия дистального отдела общего желчного протока, холелитиаз, стенозирующий папиллит, токсический гепатит. У некоторых больных вследствие сдавления и тромбоза селезеночной и воротной вен возникает портальная гипертензия. На фоне длительнотекущего ХП возможно образование карциномы поджелудочной железы.
Таким образом, основными патогенетическими факторами при ХП являются:
- хронический воспалительный процесс, сопровождающийся в первую очередь деструкцией экзокринного аппарта железы и облигатной деструкцией ее эндокринного аппарата на поздних стадиях заболевания;
- необратимая прогрессирующая атрофия и фиброз ацинусов и эндокринного аппарата поджелудочной железы (P.Banks, 1988; J.Valenzuela, 1988; H.Sarles, 1989; J.Grendell, 1993; H.Spiro, 1994).
При рассмотрении этиопатогенеза ХП должны быть выделены две основные формы заболевания:
- хронический кальцифицирующий панкреатит и
- хронический обструктивный панкреатит.
Это наиболее частые заболевания поджелудочной железы в странах Западной Европы (G.Cavallini, 1993). Реже наблюдается хронический воспалительный фиброзный панкреатит. В то же время ряд специалистов (проф. Henri Sarles из Марселя) считают, что по морфологическим изменениям эти две формы мало чем отличаются. Патогенез первичного и вторичного ХП, возникающего вследствие обтурации протоковой системы, может быть очень сходным.
Панкреатический сок содержит значительное количество кальция в сочетании с высоким уровнем бикарбонатов. Патогенез ХП во многих случаях связан с нарушением формирования растворимых белково-кальциевых ассоциатов и образованием кальцификатов. Различают 3 разновидности камней поджелудочной железы:
- кальций-карбонатно-протеиновые,
- кальций-карбонатные и
- белковые (органические) - мелкие нерастворимые протеиновые пробки с отсутствием или слабой степенью кальцификации.
Согласно теории, предложенной Sarles (1991), в патогенезе первичного ХП главную роль играет преципитация белков в протоках поджелудочной железы. В 1979 г. обнаружен гликопротеид - литостатин (PSP - pancreatic stone protein), который непосредственно связан с образованием конкрементов в поджелудочной железе. В состав белковых внутрипротоковых агрегатов входят фибриллярные нерастворимые пептиды (LS-H 2), которые являются ферментами белка литостатина (LS-S). Литостатин продуцируется ацинарными клетками. Основная роль литостатина связана с ингибированием нуклеации, агрегации и образованием кристаллов солей кальция в панкреатическом соке. Литостатин рассматривается как наиболее важный стабилизатор кальция в растворимом виде. Он обнаружен в зимогенных гранулах ацинарных клеток поджелудочной железы, присутствует в панкреатическом соке у здоровых людей, слюне (D.Hay, 1979) и моче (Y.Nakagawa, 1983). Преципитацию кальция и образование конкрементов в просвете протоков поджелудочной железы связывают с дефицитом синтеза белка литостатина (Horovitz, 1996). Уже на самых ранних этапах формирования ХП в мелких протоках поджелудочной железы обнаруживают белковые преципитаты, представляющие собой нерастворимый фибриллярный белок с отложениями кальция в виде карбонатов. Согласно этой теории, определенные врожденные факторы, а также приобретенные (злоупотребление алкоголем, курение) влияют на секрецию и стабильность литостатина. Белковые преципитаты и камни в протоках железы вызывают повреждение их покровного эпителия и способствуют перидуктальным воспалительным процессам, приводящим к развитию фиброзной ткани. Образование белковых преципитатов и камней ведет к обструкции протоковой системы, вызывает ее стенозы, что в дальнейшем приводит к возникновению новых конкрементов в протоковой системе. Алкоголь и никотин влияют на биохимический состав панкреатического сока и тем самым способствуют литогенезу в протоковой системе поджелудочной железы. В исследованиях установлено, что алкоголь способствует увеличению секреции белков ацинарными клетками поджелудочной железы, при этом увеличивается секреция белка лактоферрина и уменьшается секреция бикарбонатов и цитратов, что приводит к изменению рН панкреатического сока. Это вызывает уменьшение концентрации ингибитора трипсина, повышая нестабильность трипсиногена (L.A.Scurro, 1990). В некоторых случаях дефицит синтеза литостатина обусловлен врожденными генетическими факторами, что приводит к развитию врожденного, семейного ХП. Данная гипотеза практически исключает образование кальцифицирующих конкрементов на ранних стадиях заболевания.
При радиоиммунологическом анализе с моноклональными антителами не выявлено существенных различий в содержании литостатина в панкреатическом соке больных ХП по сравнению с контролем (W.Schimigel,1990). Концентрация литостатина в панкреатическом соке не имеет существенного значения для формирования преципитатов, более существенным является уменьшение возможностей синтеза, то есть общего пула литостатина (D.Giorgi, 1989). С этих позиций патогенез преципитации протеиново-кальциевых агрегатов рассматривается как результат снижения секреции литостатина в условиях повышенной потребности. Такие состояния возникают при усилении гидролиза белка в панкреатическом соке, индукции полимеризации белковых компонентов, появлении большого количества плохо растворимых белков, увеличении секреции кальциевых солей (J.Bernard, 1994). Изучение состава органического матрикса камней поджелудочной железы показало, что в него входят модифицированный литостатин, альбумин, глобулины с высокой молекулярной массой.
Horovitz (1996) различает 2 основных патогенетических типа ХП - кальцифицирующий и обструктивный.
Кальцифицирующий хронический панкреатит
Кальцифицирующий ХП характеризуется наличием в железе камней с высокой степенью кальцификации и имеет четкую связь с употреблением алкоголя или недостаточным (неполноценным) питанием. В начальных стадиях ХП могут обнаруживаться мелкие нерастворимые протеиновые пробки с отсутствием кальцификации. Такие «микролиты» являются рентгенотрицательными. Основные вопросы патогенеза кальцифицирующего ХП рассматриваются в настоящее время с позиций возникновения механизма преципитации кальция и протеина.
Кальцифицирующий ХП считают наиболее частой формой ХП, встречающейся в странах Западной Европы, на долю которого приходится от 36 до 95% всех ХП (T.T.White, 1978; J.Bernard, 1994). В высокоразвитых странах кальцифицирующий ХП ассоциируется прежде всего со злоупотреблением алкоголем, поражает преимущественно мужчин из зажиточных слоев населения в возрасте 30-40 лет.
В азиатских и африканских странах кальцифицирующий ХП, как правило, не имеет связи с употреблением алкоголя, он поражает представителей наименее обеспеченных слоев населения, одинаково часто отмечается у мужчин и женщин, начиная с 10-20-летнего возраста.
Обструктивный хронический панкреатит
Второй по частоте формой ХП является обструктивный панкреатит, характеризующийся наличием стеноза протоков поджелудочной железы на любом уровне. В биоптатах поджелудочной железы обычно обнаруживают атрофию ацинозной ткани с очагами фиброза. Наиболее часто обструкция локализуется на уровне ампулярного отдела, при этом имеется дистальная внутрипротоковая гипертензия с развитием дилятации протоковой системы. В случае анатомического слияния терминальных отделов протоков желчной системы и протоков поджелудочной железы при обструктивном ХП может происходить дилятация желчных протоков.
Алкогольный панкреатит
Bordalo из Португалии (1984) предложил новую гипотезу развития ХП. По его данным, основанным на анатомо-морфологических исследованиях, ХП возникает при длительном приеме алкоголя, что ведет к накоплению липидов внутри клеток поджелудочной железы и к развитию периацинарных фиброзных процессов. Автор пришел к выводу, что аналогично развитию цирроза печени фиброз поджелудочной железы возникает вследствие некрозов ацинарных клеток железы и алкогольного хронического отравления. Эта гипотеза серьезно воспринята Марсельской школой, специалисты которой считают, что вследствие алкогольного отравления в тканях поджелудочной железы происходит накопление окислительных продуктов, пероксидаз, окислительных радикалов (J.M.Braganza и соавт., 1983). Доказано, что при длительном приеме алкоголя нарушаются функции печени и поджелудочной железы, что приводит к накоплению окислительных радикалов и снижению уровня таких антиоксидантов, как витамины С, Е, рибофлавин, бета-каротин, селен. Изменения функции клеток поджелудочной железы по этой теории приводит к снижению секреции литостатина и вследствие этого - к образованию конкрементов в ее протоках. Данная гипотеза важна тем, что впервые было доказано токсическое воздействие приема алкоголя в течение длительного времени на нарушение функции поджелудочной железы, дегенерацию ацинарных клеток, развитие интрапанкреатического склероза, стеатонекроза и фиброза.
В настоящее время наиболее изучены морфологические и патогенетические особенности ХП алкогольной этиологии (H.Sarles, 1981; Kloppel и Maillet, 1992; С.П.Лебедев, 1982), для которого характерны особенно тяжелые морфологические изменения паренхимы и протоков поджелудочной железы. Наиболее вероятным при злоупотреблении алкоголем является первично-хроническое течение заболевания. Прием этилового спирта в течение длительного времени вызывает холинэргический эффект, ведет к гиперсекреции белка ацинарными клетками.
Существенным фактором развития ХП является некроз интерстициальной жировой клетчатки, что ведет к возникновению перилобулярного фиброза. При разрастании соединительной ткани между дольками поджелудочной железы происходит сдавление мелких протоков и формируется гипертензия в ее протоковой системе, препятствующая нормальному оттоку панкреатического сока. В этих условиях белковый секрет, не сбалансированный гиперпродукцией воды и бикарбонатов, накапливается в мелких протоках в виде белковых преципитатов, в которые откладываются соли кальция и в дальнейшем формируются конкременты поджелудочной железы. Эти изменения способствуют развитию интра- и перидуктального склероза, локальных стенозов и обтурации протоков поджелудочной железы с одновременной дилятацией протоковой системы.
Патогномоничными признаками алкогольного панкреатита являются:
- расширение протоков поджелудочной железы, метаплазия и десквамация протокового эпителия;
- неравномерность патологических изменений в различных участках поджелудочной железы (W.Boecker и соавт., 1972; H.Sarles, 1974).
Рассмотренные ранее 3 теории развития ХП показывают пути повреждения ацинарной ткани поджелудочной железы, приводящие к нарушениям в протоковой системе. Boros и Singer (1984) предполагают, что длительный прием алкоголя, сочетаемый с нарушением питания вызывает развитие деструктивных изменений в эпителии протоков поджелудочной железы с последующим образованием в них преципитатов и конкрементов. На моделях ХП у животных авторами было показано (1991, 1992), что при длительном приеме алкоголя у животных возможно развитие обструктивных процессов в протоках поджелудочной железы вследствие образования в них преципитатов и конкрементов. Нарушение оттока секрета железы вызывает весь комплекс клинической картины ХП. Сходство морфологической картины перидуктального фиброза при различных видах ХП приводит к мысли об определенной роли аутоимунных процессов в развитии хронического воспаления поджелудочной железы (J.Cavallini,1997). Инфильтрация ткани поджелудочной железы лимфоцитами является триггерным процессом, вызывающим фибропластический процесс в перидуктальной области. С этой точки зрения патогенез ХП выглядит следующим образом: плохой отток панкреатического сока приводит к преципитации белков, образованию белковых сгустков и в дальнейшем - камней, что вызывает обструктивные процессы в протоковой системе, и к развитию клиники ХП. Такие экзогенные факторы, как алкоголь и никотин влияют на литогенетическую способность сока поджелудочной железы и вызывают повреждение эпителиального покрова протоковой системы поджелудочной железы. Все перечисленные теории требуют четкого подтверждения. Так, R.P.Jalleh и соавт. (1993), Cavallini (1997) указывают на наличие генетической предрасположенности в развитии ХП.
K.Hakamura (1982) в морфогенезе ХП выделяет 2 стадии:
- воспалительную - до начала образования камней; типичным является дольчатый и многодольчатый характер распространения воспалительных очагов; и
- кальцинозную - с момента возникновения обызвествленных участков и камней в железе; видимых даже на обычных рентгенограммах: для этой стадии характерна непроходимость протоков поджелудочной железы.
Нарушение переваривания и всасывания пищевых веществ при ХП приводит к потере с фекалиями потребляемых белков, жиров и витаминов. В результате могутразвиться истощение, астения, нарушения метаболизма костной ткани, свертывающей системы крови.
А.А.Шалимов, В.В.Грубник, Джоэл Горовиц, А.И.Зайчук, А.И.Ткаченко / Хронический панкреатит. Современные концепции патогенеза, диагностики и лечения. 2000г
Использованные источники:
- Данилов М.В., Федоров В.Д. Хирургия поджелудочной железы. - М.: Медицина, 1995. - 509 с.
- Опыт использования сандостатина у пациентов с хроническим панкреатитом / Логи-нов А.С., Садоков А.С. Садоков В.М. и соавт. // Тер.архив. - 1995. - Т.67. - С.60-62
- Радзиховский А.П. Свищи поджелудочной железы. - К.: Наук. думка, 1987. - 222 с.
- Шалимов А.А., Шалимов С.А., Ничитайло М.Е., Радзиховский А.П. Хирургия подже-лудочной железы. - Симферополь: Таврида, 1997. - 553 с.
- Beger H.G., Buchler M. Duodenum-preserving resection of the head of the pancreas in chronic pancreatitis with inflammatori mass in the head // World J. Surg. - 1990. - Vol. 14, No. 1. - P.83-87.
- Beger H.G., Buchler M., Bittner R.R. Duodenum-preserving resection of the head of the pancreas in severe chronic pancreatitis: early and late results // Ann. Surg. - 1989. - Vol. 209, No. 3. - P.273 - 278.
- Binmoeller K.F., Jue P., Seifert H. Endoscopic pancreatic stent drainage in chronic pancreatitis and a dominant stricture: long-term results // Endoscopy. - 1995. - Vol. 27. - P.638-644.
- Bornman P.C., Russell R.C.G. Endoscopic treatment for chronic pancreatitis // Br. J. Surg. - 1992. -Vol. 79, No. 12. - P.1260-1261.
- Buchler M.W., Friess H., Baer H. Surgical treatment of chronic pancreatitis: new standards // Dig. Surg. - 1996. - Vol. 13, No. 2.
- Carlin A., Fromm D. Pancreaticoduodenectomy for recurrent alcoholic pancreatitis associated with microabscesses // Surg. Gynec. Obst. - 1993. - Vol. 176, No. 4. - P.315-318.
- Coleman S.D., Eisen G.M., Troughton A.B. Endoscopic treatment in pancreas divisum // Am. J. Gastroenterol. - 1994. - Vol. 89, No. 8. - P.1152 - 1155.
- Cremer M., Deviere J., Delhaye M. Non-surgical management of severe chronic pancreatitis. // Scand. J. Gastroenterol. - 1990. - Vol. 175, suppl. - P.77-84.
- Cremer M., Deviere J., Delhaye M. Stenting in severe chronic pancreatitis: results of medium-term follow-up in sewenty-six patients // Endoscopy. - 1991. - Vol. 23.- P.171-176.
- Crombleholme T.M., deLorimier A.A., Way L.W. The modified Puestow procedure for chronic relapsing pancreatitis in children // J. Pediatric Surg. - 1990. - Vol. 25, No. 7. - P.749- 754.
- Greenlee H.B., Prinz R.A., Arancha G.V. Long-term results of side-to-side pancreaticojejunostomy // World J. Surg. - 1990. - Vol. 14, No. 1. - P.70-76.
- Holt S. Chronic pancreatitis // Sout. Med. J. - 1991. - Vol. 86, No. 2. - P.201-207.
Хронический панкреатит (ХП) – хроническое полиэтиологическое воспаление поджелудочной железы, продолжающееся более 6 месяцев, характеризующееся постепенным замещением паренхиматозной ткани соединительной и нарушением экзо- и эндокринной функции органа.
Эпидемиология : чаще страдают мужчины среднего и пожилого возраста; частота у взрослых 0,2-0,6%
Основные этиологические факторы:
1) алкоголь – основной этиологический фактор (особенно при сочетании с курением)
2) заболевания желчного пузыря и желчевыводящих путей (хронический калькулезный и бескаменный холецистит, дискинезии желчевыводящих путей)
3) злоупотребление жирной, острой, соленой, перченой, копченой пищей
4) лекарственная интоксикация (в первую очередь эстрогены и ГКС)
5) вирусы и бактерии, попадающие в проток поджелудочной железы из ДПК через фатеров сосочек
6) травмы поджелудочной железы (при этом возможно склерозирование протоков с повышением внутрипротокового давления)
7) генетическая предрасположенность (часто сочетание ХП с группой крови О(I)
8) беременность на поздних сроках (приводит к сдавления поджелудочной железы и повышению внутрипротокового давления)
Патогенез хронического панкреатита:
В развитии хронического панкреатита основную роль играют 2 механизма:
1) чрезмерная активация собственных ферментов поджелудочной железы (трипсиногена, химотрипсиногена, проэластазы, липазы)
2) повышение внутрипротокового давления и затруднение оттока поджелудочного сока с ферментами из железы
В результате наступает аутолиз (самопереваривание) ткани поджелудочной железы; участки некроза постепенно замещается фиброзной тканью.
Алкоголь является как хорошим стимулятором секреции соляной кислоты (а она уже активируют панкреатические ферменты), так и приводит к дуоденостазу, повышая внутрипротоковое давление.
Классификация хронического панкреатита:
I. По морфологическим признакам: интерстициально-отечный, паренхиматозный, фиброзно-склеротический (индуративный), гиперпластический (псевдотуморозный), кистозный
II. По клиническим проявлениям: болевой вариант, гипосекреторный, астеноневротический (ипохондрический), латентный, сочетанный, псевдотуморозный
III. По характеру клинического течения: редко рецидивирующий (одно обострение в 1-2 года), часто рецидивирующий (2-3 и более обострений в год), персистирующий
IV. По этиологии: билиарнозависимый, алкогольный, дисметаболический, инфекционный, лекарственный
Клиника хронического панкреатита:
1) боль – может быть внезапной, острой или постоянной, тупой, давящей, возникает через 40-60 мин после еды (особенно обильной, острой, жареной, жирной), усиливается в положении лежа на спине и ослабевает в положении сидя при небольшом наклоне вперед, локализована при поражении головки — справа от срединной линии, ближе к правому подреберью, при поражении тела — по срединной линии на 6-7 см выше пупка, при поражении хвоста — в левом подреберье, ближе к срединной линии; в 30% случаев боль носит опоясывающий характер, еще в 30% — не имеет определенной локализации; половина больных ограничивают себя в приеме пищи из-за боязни болей
2) диспепсический синдром (отрыжка, изжога, тошнота, рвота); рвота у части больных сопровождают болевой синдром, многократная, не приносит никакого облегчения
3) синдром экзокринной недостаточности поджелудочной железы: «панкреатогенная диарея» (связана с недостаточным содержанием в выделенном панкреатическом соке ферментов, при этом характерно большое количество каловых масс, содержащих много нейтрального жира, непереваренных мышечных волокон), синдром мальабсорбции, проявляющийся рядом трофических нарушений (снижение массы тела, анемия, гиповитаминоз: сухость кожи, ломкость ногтей и выпадение волос, разрушение эпидермиса кожи)
4) синдром эндокринной недостаточности (вторичный сахарный диабет).
Диагностика хронического панкреатита:
1. Сонография поджелудочной железы: определение ее размеров, эхогенности структуры
2. ФГДС (в норме ДПК, как «корона», огибает поджелудочную железу; при воспалении эта «корона» начинает расправляться – косвенный признак хронического панкреатита)
3. Рентгенография ЖКТ с пассажем бария: контуры ДПК изменены, симптом «кулис» (ДПК выпрямляется и раздвигается, как кулисы на сцене, при значительном увеличении pancreas)
4. КТ – в основном используется для дифференциальной диагностики ХП и рака поджелудочной железы, т.к. их симптомы схожи
5. Ретроградная эндоскопическая холангиодуоденопанкреатография — через эндоскоп специальной канюлей входят в фатеров сосочек и вводят контраст, а затем делают серию рентгенограмм (позволяет диагностировать причины внутрипротоковой гипертензии)
6. Лабораторные исследования:
а) ОАК: при обострении — лейкоцитоз, ускорение СОЭ
б) ОАМ: при обострении — увеличение диастазы
в) БАК: при обострении — повышение уровня амилазы, липазы, трипсина
в) копрограмма: нейтральный жир, жирные кислоты, непереваренные мышечные и коллагеновые волокна
Лечение хронического панкреатита.
1. При обострении — стол № 0 в течение 1-3 дней, затем стол № 5п (панкреатический: ограничение жирной, острой, жареной, пряной, перченой, соленой, копченой пищи); вся пища вареная; питание 4-5 раз/сутки малыми порциями; отказ от употребления алкоголя
2. Купирование боли: спазмолитики (миолитики: папаверин 2% – 2 мл 3 раза/сут в/м или 2% – 4 мл на физрастворе в/в, дротаверин / но-шпа 40 мг 3 раза/сут, М-холиноблокаторы: платифиллин, атропин), анальгетики (ненаркотические: анальгин 50% – 2 мл в/м, в тяжелых случаях – наркотические: трамадол внутрь 800 мг/сут).
3. Антисекреторные препараты: антациды, блокаторы протонной помпы (омепразол по 20 мг утром и вечером), блокаторы Н 2 -рецепторов (фамотидин по 20 мг 2 раза/сут, ранитидин) – снижают секрецию желудочного сока, который является естественным стимулятором секреции поджелудочной железы
4. Ингибиторы протеаз (особенно при интенсивном болевом синдроме): гордокс, контрикал, трасилол, аминокапроновая кислота в/в капельно, медленно, на физрастворе или 5% растворе глюкозы, октреотид / сандостатин 100 мкг 3 раза/сут п/к
5. Заместительная терапия (при недостаточности экзокринной функции): панкреатин 0,5 г 3 раза/сут во время или после еды, креон, панцитрат, мезим, мезим-форте.
6. Витаминотерапия – для предупреждения трофических нарушений как результата синдрома мальабсорбции
7. Физиотерапия: ультразвук, синусомоделированные токи различной частоты, лазер, магнитотерапия (при обострении), тепловые процедуры: озокерит, парафин, грязевые аппликации (в фазе ремиссии)
Диспансерное наблюдение : 2 раза/год на уровне поликлиники (осмотр, основные лабораторные тесты, УЗИ).
Операции: резекция и операционный внутренний дренаж холецистэктомия,панктрэктомия холедохостомия,папиллосфинктеропластика,вирсунгопластика,формирование панкреатоеюнальнного соустья
Панкреатит представляет собой тяжелое заболевание поджелудочной железы, в основе которого лежит внутриорганная активация продуцируемых железой пищеварительных ферментов и выраженное в различной степени ферментативное повреждение ткани (панкреонекроз), с последующим развитием фиброза, нередко распространяющееся на окружающие ткани (парапанкреофиброз), а также осложняемое вторичной инфекцией. Клинически панкреатит может протекать в острой и хронической формах, нередко тесно связанных между собой.
Этиология.
Этиологией возникновения хронического панкреатита являются:
1. Алкоголь, раздражая слизистую оболочку 12 п.к„ не только усиливает продукцию секретина, панкреозимина, гистамина, гастрина, а, следовательно, и внешнюю секрецию ПЖ, но и вызывает рефлекторный спазм сфинктера Одди, приводящий к внутрипротоковой гипертензии. Длительное употребление алкоголя сопровождается дуоденитом с нарастающей атонией сфинктера, что приводит к дуоденопанкреатическому и билиарнопанкреатическому рефлюксу, особенно во время рвоты. Имеет значение и белково-витаминная недостаточность свойственная хроническому алкоголизму. Некоторые авторы полагают, что алкоголь может оказывать и прямое токсическое воздействие на паренхиму ПЖ. Кроме того, имеются данные, что хроническая алкогольная интоксикация изменяет состав панкреатического сока за счет увеличения количества белка, лактоферрина и снижения бикарбонатов и ингибиторов протеаз, что способствует образованию конкрементов.
2. Заболевания желчного пузыря и желчевыводящих путей, при доминировании желчнокаменной болезни, включая и состояние после холецистэктомии. Сопровождающий эти заболевания воспалительно-склеротический процесс в дистальных отделах желчевыводящих путей приводит к стенозу, либо недостаточности сфинктера Одди. Спазм или стеноз сфинктера приводят к гипертензии в протоковой системе ПЖ и, как следствие, выходу компонентов панкреатического сока в паренхиму с развитием в ней воспалительных и склеротических изменений. Рефлюкс желчи при этом не имеет решающего значения, так как ХП развивается и при раздельном впадении холедоха и вирсунгиева протока в 12 п.к. Слизистая оболочка панкреатических протоков в норме резистентна к действию желчи, и только при длительной инкубации желчи в смеси с панкреатическим секретом или культурой бактерий желчь приобретает повреждающее действие на ПЖ. В случае недостаточности большого дуоденального соска происходит рефлюкс кишечного содержимого в протоки ПЖ с активацией протеолитических ферментов, что в сочетании с гипертензией и оказывает повреждающее воздействие на паренхиму органа.
3. Травма ПЖ, в том числе интраоперационная, В развитии послеоперационного панкреатита имеет значение не только прямое воздействие на ткань железы и ее протоки, но и деваскуляризация ПЖ,
4. Заболевания желудочно-кишечного тракта, особенно 12 п.к.: отек в области Фатерова соска, затрудняющий отток панкреатического секрета, дуоденостаз, сопровождающийся дуоденопанкреатическим рефлюксом; дивертикулы 12 п.к., которые могут приводить либо к сдавлению протоков с последующей гипертензией, либо, в случае открытия протока в дивертикул- к дуоденопанкреатическому рефлюксу. Дуоденит не только поддерживает воспаление Фатерова соска, но и вызывает секреторную дисфункцию ПЖ вследствие нарушения продукции полипептидных гормонов ЖКТ. Пенетрация язвы 12 п.к. или желудка в ПЖ чаще приводит к очаговому воспалительному процессу, а в ряде случаев - к типичному хроническому рецидивирующему панкреатиту.
5. Одностороннее питание углеводной и жирной пищей при недостатке белков ведет к резкой стимуляции внешней секреции с последующим срывом регенераторных процессов в ПЖ. Особенно большое значение имеет прием алкоголя с жирной пищей.
6. Эндокринопатии и нарушения обмена веществ:
Гиперпаратиреоз, который ведет к гиперкальцисмии и кальцификации ПЖ /кальций способствует переходу трипсиногена в трипсин в протоках ПЖ
Гиперлипидемия, которая ведет к жировой инфильтрации клеток ПЖ, повреждению сосудистой стенки, образованию тромбов, микроэмболии сосудов;
7. Аллергические факторы. В крови ряда больных обнаруживаются антитела к ПЖ; в некоторых случаях отмечается выраженная эозинофилия (до 30-40% и более). В литературе описаны случаи появления болевых кризов при употреблении клубники, и развития ХП на фоне бронхиальной астмы.
8. Наследственные факторы. Так известно, что у детей, родители которых страдают ХП, повышена вероятность его развития по аутосомно-доминантному типу. Подчеркивается более частая встречаемость ХП у лиц с 0(1) группой крови. В некоторых случаях это бывает причиной так называемых ювенильных панкреатитов.
9. Пороки развития панкреобилиодуоденапьной зоны: кольцевидная ПЖ, сопровождающаяся дуоденостазом; добавочная ПЖ с различными вариантами хода протоков, не обеспечивающими отток секрета; энтерогенные кисты ПЖ.
10. Лекарственные препараты: стероидные гормоны, эстрогены, сульфаниламиды, метилдофа, тетрациклин, сульфасалазин, метронидазол, ряд нестероидных противовоспалительных средств, иммунодепрессанты, антикоагулянты, ингибиторы холинэстеразы и другие.
11. Неспецифический язвенный колит, болезнь Крона, гемохроматоэ и ряд других заболеваний, сопровождающихся склеротическими изменениями в ПЖ без клинической манифестации, что можно рассматривать как неспецифическую тканевую реакцию на токсические или циркуляторные воздействия. В эту же группу, вероятно, следует отнести фиброз ПЖ при циррозах печени.
Патогенез. Можно считать общепризнанным, что в основе патогенеза панкреатита у подавляющего большинства больных лежит повреждение ткани железы ею же продуцируемыми пищеварительными ферментами. В норме эти ферменты выделяются в неактивном состоянии (кроме амилазы и некоторых фракций липазы) и становятся активными лишь после попадания в двенадцатиперстную кишку. Большинство современных авторов выделяют три главных патогенетических фактора, способствующих аутоагрессии ферментов в секретирующем их органе:
1) затруднение оттока секрета железы в двенадцатиперстную кишку и внутрипротоковая гипертензия;
2) ненормально высокие объем и ферментативная активность сока поджелудочной железы;
3) рефлюкс в протоковую систему поджелудочной железы содержимого двенадцатиперстной кишки и желчи.
Механизмы патологической внутриорганной активации ферментов и повреждения ткани железы различаются в зависимости от причины панкреатита. Так известно, что алкоголь, особенно в больших дозах, рефлекторным и гуморальным путем резко повышает объем и активность панкреатического сока. К этому дбавляется стимулирующее действие алиментарного фактора, поскольку алкоголики питаются нерегулярно, не столько едят, сколько закусывают, принимая много жирной и острой пищи. Кроме того, алкоголь способствует спазму сфинктера печеночно-панкреатической ампулы (сфинктера Одди), вызывает повышение вязкости панкреатического секрета, образование в нем белковых преципитатов, в дальнейшем трансформирующихся в конкременты, характерные для хронической формы заболевания. Все это затрудняет отток секрета и ведет к внутрипротоковой гипертензии, которая при уровне, превышающем 35-40 см вод. ст., способна обусловить повреждение клеток эпителия протоков и ацинусов и освобождение цитокиназ, запускающих механизм активации ферментов. Спазм сфинктера Одди, возможно, ведет к желчно-панкреатическому рефлюксу и внутрипротоковой активации ферментов за счет желчных кислот. Не исключают также и прямое повреждающее действие высоких концентраций алкоголя в крови на железистые клетки.
При панкреатите, связанном с заболеваниями желчных путей, главным патогенетическим фактором является нарушение оттока панкреатического сока в двенадцатиперстную кишку, что связано, прежде всего, с наличием упоминавшегося «общего канала», то есть печеночно-панкреатической (фатеровой) ампулы, через которую отходят желчные конкременты и куда обычно впадает главный панкреатический проток. Известно, что при раздельном впадении желчного и панкреатических протоков, а также при отдельном впадении в двенадцатиперстную кишку добавочного протока, сообщающегося с главным протоком поджелудочной железы, билиарный панкреатит не развивается.
Проходя через фатерову ампулу, желчные конкременты временно задерживаются в ней, вызывая спазм сфинктера Одди и преходящую протоковую гипертензию, обусловливающую ферментативное повреждение ткани железы и, возможно, приступ острого панкреатита, в ряде случаев протекающий малосимптомно или же маскирующийся приступом желчной колики. Повторное «проталкивание» желчных камней через ампулу за счет высокого панкреатического и билиарного давления может привести к травме слизистой дуоденального сосочка и стенозирующему панпиллиту, все более затрудняющему пассаж желчи и панкреатического сока, а также и повторное отхождение камней. Иногда наступает стойкое ущемление желчного конкремента в ампуле, ведущее к обтурациониой желтухе и тяжелому панкреонекрозу.
Самостоятельную роль в патогенезе панкреатита могут играть также заболевания двенадцатиперстной кишки, связанные с дуоденостазом и гипертензией в ее просвете и способствующие рефлюксу дуоденального содержимого в панкреатический проток (в том числе «синдром приводящей петли» после резекции желудка по типу Бильрот П). Некоторые авторы указывают и на значение дивертикулов двенадцатиперстной кишки, в особенности перипапиллярных, которые могут обусловливать как спазм, так и (редко) атонию сфинктера Одди.
Травматический панкреатит может быть связан как с прямым, так и с опосредованным воздействием на поджелудочную железу. При прямой травме к внутриорганной активации ферментов ведет механическое повреждение железы с выделением из омертвевающих клеток уже упоминавшихся активаторов (цитокиназ) и последующим развитием в дополнение к травматическому еще и ферментативного панкреонекроза. При эндоскопических вмешательствах на большом дуоденальном сосочке (РХПГ, ЭПСТ) часто травмируется слизистая оболочка фатеровой ампулы и терминального отдела главного панкреатического протока. В результате травмы кровоизлияний и реактивного отека может затрудняться отток панкреатического секрета и развиваться протоковая гипертензия.Стенки протока могут повреждаться и от избыточного давления при введении контрастного вещества при РХПГ.
При опосредованном воздействии случайных и операционных травм на поджелудочную железу (травматический шок, кровопотеря, кардиохирургические вмешательства с длительной перфузией) повреждение железистой ткани с высвобождением активирующих клеточных факторов связано в основном с микроциркуляторными расстройствами и соответствующей гипоксией.
Следует обратить внимание на еще один важный аспект патогенеза хронического панкреатита, недостаточно освещаемый в литературе. По представлениям большинства клиницистов панкреонекроз считается определяющей особенностью наиболее тяжелых форм острого деструктивного панкреатита. Однако повреждение и гибель (омертвение, некроз) ткани поджелудочной железы под воздействием внутриорганной активации и аутоагрессии пищеварительных ферментов определяет возникновение и течение любых, в том числе и хронических, форм рассматриваемого заболевания.
При хроническом панкреатите, не являющемся следствием острого, также имеет место ферментативное повреждение, некробиоз, некроз и аутолиз панкреатоцитов, происходящие как постепенно, под влиянием длительно действующего фактора, так и остро скачкообразно в период обострений хронического процесса.
Патологическая анатомия. В процессе развития панкреатита в ткани поджелудочной железы происходит разрастание соединительной ткани, в результате чего развивается фиброз и склероз. В дальнейшем развиваются обызвествление, нарушение проходимости панкреатических протоков..
Catad_tema Панкреатит - статьи
Хронический панкреатит: от патогенеза к терапии
К.м.н. О.И. Костюкевич
РГМУ
Поджелудочная железа (ПЖ) – один из самых загадочных органов желудочно–кишечного тракта. До сих пор остается много нерешенных вопросов, что объясняется особенностями расположения ПЖ и неспецифическими проявлениями многих ее заболеваний. Как слазал известный панкреатолог Г.Ф. Коротько, «поджелудочная железа медленно и неохотно раскрывает свои тайны» .
Во всем мире за последние 30 лет наблюдается увеличение за болеваемости острым и хроническим панкреатитом более чем в 2 раза . В России отмечен более интенсивный рост заболеваемости ХП. Так, распространенность заболеваний ПЖ среди взрослых за последние 10 лет увеличилась в 3 раза, а среди подростков – более чем в 4 раза. Считается, что данная тенденция связана с увеличением потребления алкоголя, в том числе низкого качества, снижением качества питания и общего уровня жизни . Обычно ХП развивается в возрасте 35-50 лет, среди заболевших на 30% увеличилась доля женщин.
Значения показателей заболеваемости постоянно растут и за счет улучшения методов диагностики, появления в последнее время новых методов визуализации ПЖ с высокой разрешающей способностью, позволяющих выявлять ХП на более ранних стадиях развития заболевания .
Хронический панкреатит (ХП) – медленно прогрессирующее воспалительное заболевание поджелудочной железы, характеризующееся фокальными некрозами в сочетании с фиброзом, и приводящее к прогрессирующему снижению экзо– и эндокринной функции органа (даже после прекращения воздействия этиологического фактора). Условно о ХП говорят, когда воспалительный процесс в ПЖ продолжается более 6 мес. ХП обычно протекает с эпизодами обострений и ремиссий.
Острый и хронический панкреатит. Практикующему врачу известно, насколько важно провести грань между острым и хроническим панкреатитом, поскольку имеются принципиальные отличия в тактике ведения таких пациентов. В то же время провести эту грань порой чрезвычайно сложно, поскольку обострение хронического панкреатита по своей клинической картине очень напоминает ОП, а ОП, в свою очередь, может остаться нераспознанным (в 60% случаев!), протекая под масками других болезней ЖКТ.
В диагностике ОП важнейшим маркером является повышение уровня сывороточной амилазы более чем в 4 раза.
Известно, что острый панкреатит в 10% случаев трансформируется в хронический (а учитывая нераспознанные эпизоды ОП – гораздо чаще).
Классификация ХП
I. Согласно Марсельско–Римской классификации (1988), принятой в европейских странах, выделяются следующие клинические формы ХП:
- обструктивный,
- кальцифицирующий,
- воспалительный (паренхиматозный).
Хронический обструктивный панкреатит развивается в результате обструкции главного протока ПЖ. Поражение ПЖ равномерное и не сопровождается образованием камней внутри протоков. В клинической картине при данной форме ХП ведущим является постоянный болевой синдром.
При кальцифицирующем ХП в протоках обнаруживаются белковые преципитаты или кальцификаты, камни, кисты и псевдокисты, стеноз и атрезия, а также атрофия ацинарной ткани. Для данной формы ХП характерно рецидивирующее течение с эпизодами обострения, на ранних этапах напоминающими острый панкреатит (хронический рецидивирующий панкреатит). Как правило, такой ХП имеет алкогольную этиологию.
Хронический паренхиматозный панкреатит характеризуется развитием очагов воспаления в паренхиме с преобладанием в инфильтратах мононуклеарных клеток и участков фиброза, которые замещают паренхиму ПЖ. При этой форме ХП отсутствуют поражение протоков и кальцификаты в ПЖ. В клинической картине ведущими являются медленно прогрессирующие признаки экзокринной и эндокринной недостаточности и отсутствие болевого синдрома (ХП, безболевая форма).
II. Общепринятой классификацией ХП в России является классификация, предложенная В.Т. Ивашкиным и соавт. , ХП подразделяют по нескольким признакам:
- По морфологическим признакам: 1) интерстициально–отечный; 2) паренхиматозный; 3) фиброзно–склеротический (индуративный); 4) гиперпластический (псевдотуморозный); 5) кистозный.
- По клиническим проявлениям:1) болевой; 2) гипосекреторный; 3) астеноневротический (ипохондрический); 4) латентный; 5) сочетанный.
- По характеру клинического течения: 1) редко рецидивирующий; 2) часто рецидивирующий; 3) персистирующий.
- По этиологии:1) алкогольный; 2) билиарнозависимый; 3) дисметаболический; 4) инфекционный; 5) лекарственный; 6) идиопатический.
- Осложнения:1) нарушения оттока желчи; 2) портальная гипертензия; 3) инфекционные (холангит, абсцессы); 4) воспалительные (абсцесс, киста, парапанкреатит, «ферментативный холецистит», эрозивный эзофагит); 5) гастро–дуоденальные кровотечения; 6) выпотной плеврит, пневмония, острый респираторный дистресс–синдром, паранефрит, острая почечная недостаточность; 7) экзокринные нарушения (сахарный диабет, гипогликемические состояния).
Этиология ХП
Основными причинами развития ХП являются следующие:
- употребление алкоголя – алкогольный панкреатит (чаще у мужчин) в дозе более 20–80 мг этанола/сут. на протяжении 8–12 лет (по данным разных источников) – 40–80% и курение табака;
- болезни ЖП и двенадцатиперстной кишки – билиарный панкреатит (чаще у женщин);
- желчно–каменная болезнь является причиной ХП в 35–56%;
- патология сфинктера Одди (стеноз, стриктуры, воспаление, опухоль);
- дуоденит и язвенная болезнь 12 ПК. Так, язвенная болезнь 12 ПК в 10,5–16,5% случаев является непосредственной причиной развития ХП .
- муковисцидоз (часто у детей);
- наследственный панкреатит. Наиболее распространен в Северной Европе, его частота составляет около 5% из всех случаев ХП. Заподозрить наследственную форму панкреатита позволяют отсутствие этиологических факторов и случаи панкреатита в семье у родственников больного;
- идиопатический панкреатит. Когда на момент исследования идентификация этиологического фактора не возможна – 10 до 30% от всех панкреатитов;
- другие причины:
- аутоиммунный панкреатит
- системные заболевания и васкулиты
- вирусные (Коксаки, ЦМВ) и бактериальные инфекции
- глистные инвазии (описторхоз)
- нарушения метаболизма (гиперлипидемия, сахарный диабет, ХПН и др.)
- дисциркуляторные расстройства (ишемический панкреатит)
- аномалии развития ПЖ
- травмы, острые отравления.
Патогенез ХП
В основе патогенеза ХП вне зависимости от причины лежит преждевременная активация собственных ферментов, что приводит к аутолизу («самоперевариванию») ПЖ. Главным фактором является превращение трипсиногена в трипсин непосредственно в протоках и в ткани ПЖ (в норме это происходит в 12 ПК), который является чрезвычайно агрессивным фактором, повреждающим ПЖ, в результате развивается воспалительная реакция. Механизмы, лежащие в основе преждевременной активации ферментов, будут различаться в зависимости от основного этиологического фактора.
Влияние алкоголя на ПЖ
В патогенезе алкогольного панкреатита участвуют несколько механизмов :
- Этанол вызывает спазм сфинктера Одди, что приводит к развитию внутрипротоковой гипертензии и стенки протоков становятся проницаемыми для ферментов. Последние активируются, «запуская» аутолиз ткани ПЖ.
- Под влиянием алкоголя изменяется качественный состав панкреатического сока, в котором содержится избыточное количество белка и имеется низкая концентрация бикарбонатов. В связи с этим создаются условия для выпадения белковых преципитатов в виде пробок, которые затем кальцифицируются и обтурируют панкреатические протоки (кальцифицирующий панкреатит).
- Этанол нарушает синтез фосфолипидов клеточных мембран, вызывая повышение их проницаемости для ферментов.
- Непосредственное токсическое действие этанола и его метаболитов на клетки ПЖ, снижение активности фермента оксидазы, что приводит к образованию свободных радикалов, ответственных за развитие некрозов и воспаления с последующим фиброзированием и жировым перерождением ткани ПЖ.
- Этанол способствует фиброзу мелких сосудов с нарушением микроциркуляции.
Механизмы развития билиарного панкреатита
- Анатомическая близость мест впадения общего желчного и панкреатического протоков в двенадцатиперстную кишку в силу разных причин может приводить к рефлюксу желчи, в результате чего активируется трипсиноген.
- Вследствие обструкции протока или ампулы дуоденального сосочка развивается гипертензия в протоке ПЖ с последующим разрывом мелких панкреатических протоков. Это приводит к выделению секрета в паренхиму железы и активации пищеварительных ферментов. Частые рецидивы билиарного панкреатита обычно возникают при миграции мелких и очень мелких камней (микролитов), наиболее опасными являются камни размером до 4 мм.
- Достаточно частой причиной, приводящей к развитию ХП, является дуоденопанкреатический рефлюкс, возникающий на фоне атонии сфинктера Одди, особенно при наличии дуоденальной гипертензии.
- Патогенетическими факторами развития ХП при язвенной болезни являются:
- отек фатерова сосочка (папиллит) с вторичным затруднением оттока панкреатического секрета.
- гиперацидность желудочного сока с чрезмерной стимуляцией ПЖ соляной кислотой, в условиях затруднения оттока это приводит к внутрипротоковой гипертензии.
- Часто в развитии билиарного ХП имеет место комбинация этиологических механизмов; например, у больных желчно–каменной болезнью выявляются опухоли БДС, язвенная болезнь и др.
Ишемия. Ишемический панкреатит достаточно часто возникает в пожилом и старческом возрасте. Выделяют несколько основных причин ишемии ПЖ:
- сдавление чревного ствола увеличенными забрюшинными лимфатическими узлами, кистами ПЖ;
- давление питающих сосудов увеличенной ПЖ при псевдотуморозном панкреатите.
- атеросклеротическое поражение чревного ствола;
- тромбоэмболия;
- диабетическая ангиопатия.
Гиперлипидемия. Высокий риск панкреатита наблюдается при повышении триглицеридов более 500 мг/дл. Механизм развития ХП связывают с токсическим воздействии на ткань ПЖ высоких концентраций свободных жирных кислот, которые не могут быть полностью связаны сывороточными альбуминами в плазме крови.
Клинические проявления ХП
Наиболее часто встречаемыми клиническими синдромами при ХП являются:
- болевой абдоминальный синдром,
- синдром внешнесекреторной недостаточности ПЖ,
- синдром эндокринных нарушений,
- диспепсический синдром,
- синдром билиарной гипертензии.
1. Болевой синдром
Боль может встречаться как при обострении, так и в фазу ремиссии ХП. Боль не имеет четкой локализации, возникая в верхнем или среднем отделе живота слева или посередине, иррадиирует в спину, иногда принимая опоясывающий характер. Более чем у половины больных боли крайне интенсивные.
Можно выделить следующие механизмы развития болей при ХП:
- острое воспаление ПЖ (повреждение паренхимы и капсулы);
- псевдокисты с перифокальным воспалением;
- обструкция и дилатация панкреатического и желчного протока;
- фиброз в области сенсорных нервов, приводящий к их сдавлению;
- давление на окружающие нервные сплетения увеличенной ПЖ;
- стеноз и дискинезия сфинктера Одди. а) Боли, связанные с псевдокистами и обструкцией протоков значительно усиливаются во время или сразу после еды. Боли, как правило, опоясывающие, приступообразные. Значительно уменьшают боль антисекреторные препараты и препараты панкреатина (Панзинорм), которые снижают секрецию ПЖ по механизму обратной связи. б) Воспалительные боли не зависят от приема пищи, локализуются, как правило, в эпигастрии, иррадиируют в спину. Купируются такие боли анальгетиками (НПВП, в тяжелых случаях – наркотические анальгетики) в) Внешнесекреторная недостаточность ПЖ приводит к избыточному бактериальному росту в тонкой кишке, что также является причиной болевого синдрома у значительной части больных ХП. Эти боли обусловлены повышением давления в двенадцатиперстной кишке.
На поздних стадиях ХП, с развитием фиброза, боли уменьшаются и через несколько лет могут исчезнуть. Тогда на первый план выходят проявления экзокринной недостаточности.
2. Синдром внешнесекреторной недостаточности
Внешнесекреторная недостаточность ПЖ проявляется нарушением процессов кишечного пищеварения и всасывания. Клинически она проявляется:
- поносами (стул от 3 до 6 раз в сутки),
- стеатореей (возникает при снижении панкреатической секреции на 10%, кал кашицеобразный, зловонный, с жирным блеском).
- снижением массы тела,
- тошнотой,
- эпизодической рвотой,
- потерей аппетита.
Довольно быстро развивается синдром избыточного бактериального роста в тонкой кишке, проявляющийся:
- метеоризмом,
- урчанием в животе,
- отрыжкой.
Позднее присоединяются симптомы, характерные для гиповитаминоза.
В основе внешнесекреторной недостаточности ПЖ лежат следующие механизмы:
- деструкция ацинарных клеток, в результате чего снижается синтез панкреатических ферментов;
- обструкция панкреатического протока, нарушающая поступление панкреатического сока в двенадцатиперстную кишку;
- снижение секреции бикарбонатов эпителием протоков ПЖ приводит к закислению содержимого двенадцатиперстной кишки до рН 4 и ниже, в результате чего происходит денатурация панкреатических ферментов и преципитация желчных кислот.
3. Синдром билиарной гипертензии
Синдром билиарной гипертензии проявляется механической желтухой и холангитом и не является редким. До 30% больных в стадии обострения ХП имеют преходящую или стойкую гипербилирубинемию. Причинами синдрома являются – увеличение головки ПЖ со сдавлением ею терминального отдела холедоха, холедохолитиаз и патология БДС (конкременты, стеноз).
4. Синдром эндокринных нарушений
Выявляется примерно у 1/3 больных. В основе развития данных нарушений лежит поражение всех клеток островкового аппарата ПЖ, вследствие чего возникает дефицит не только инсулина, но и глюкагона. Это объясняет особенности течения панкреатогенного сахарного диабета: склонность к гипогликемиям, потребность в низких дозах инсулина, редкое развитие кетоацидоза, сосудистых и других осложнений.
5. Симптомы, обусловленные ферментемией
- Интоксикационный синдром проявляется общей слабостью, снижением аппетита, гипотонией, тахикардией, лихорадкой, лейкоцитозом и повышением СОЭ.
- Симптом Тужилина (симптом «красных капелек») появление ярко–красных пятнышек на коже груди, спины, живота. Эти пятнышки представляют собой сосудистые аневризмы и не исчезают при надавливании.
Диагностика ХП
I. Данные объективного обследования
II. Инструментальные методы диагностики
- Ультразвуковая диагностика хронического панкреатита.
- Трансабдоминальное УЗИ позволяет определять изменения размеров поджелудочной железы, неровность контура, понижение и повышение ее эхогенности, псевдокисты, кальцинаты и т.д.
- Эндоскопическая ультрасонография (ЭУС) – метод диагностики, при котором исследование проводится не через брюшную стенку, а через стенку желудка и двенадцатиперстной кишки. Это позволяет детально изучить структуру ткани ПЖ, состояние протоковой системы, выявить конкременты, провести дифференциальную диагностику панкреатита с раком ПЖ.
- Компьютерная томография – высокоинформативный метод, особенно в условиях плохой визуализации ПЖ при УЗИ.
- ЭРХПГ позволяет выявить патологию общего желчного и главного панкреатического протока, определить локализацию обструкции, обнаружить внутрипротоковые кальцинаты.
- Магнитно–резонансная томография – новейшие МРТ–программы, позволяющие получать прямое изображение протоков ПЖ (как при ЭРХПГ) без инвазивного вмешательства и введения контрастных веществ.
- Обзорный рентгеновский снимок живота позволяет выявить наличие кальцификатов в зоне проекции ПЖ, которые определяются у 30% больных ХП.
III. Лабораторная диагностика хронического панкреатита
1. Клинический анализ крови (при обострении ХП может встречаться лейкоцитоз, ускорение СОЭ. при развитии белково–энергетической недостаточности – анемия).
2. Исследование содержания (активности) ферментов поджелудочной железы:
- амилаза в крови и моче. В периоде ремиссии ХП может быть в норме, при обострении умеренно повышается (на 30%) при повышении сывороточной амилазы более 4 норм следует думать об ОП. Амилаза мочи – менее чувствительный маркер ОП, чем амилаза крови;
- эластаза 1 в крови и кале – высокочувствительный маркер. Активность этого фермента в крови повышается при панкреатите раньше, чем уровень других ферментов, и удерживается дольше.
Иммуноферментный метод определения эластазы 1 в кале на сегодняшний день является «золотым стандартом» – самым информативным из неинвазивных методов диагностики экзокринной недостаточности ПЖ. Этот фермент абсолютно специфичен для ПЖ, не разрушается при прохождении через ЖКТ и, что немаловажно, на результаты теста не влияет заместительная фарментная терапия. Экзокринная недостаточность диагностируется при снижении эластазы 1 ниже 200 мкг/г кала.
3. Другие ферменты поджелудочной железы. Высокочувствительными и специфичными тестами, свидетельствующими об обострении заболевания, являются повышение активности сывороточной липазы, а также сывороточного трипсина и уменьшение концентрации ингибитора трипсина. Однако при выраженном фиброзе ПЖ уровень ферментов в сыворотке крови даже при обострении заболевания может быть нормальным или низким.
4. Оценка внешнесекреторной функции поджелудочной железы:
- стандартное копрологическое исследование. Критериями внешнесекреторной недостаточности являются повышенное содержание в кале нейтрального жира и мыл при малоизмененном содержании жирных кислот. Повышенное количество мышечных волокон в кале (креаторея) – является более поздним, чем стеаторея, признаком недостаточности ПЖ и свидетельствует о более тяжелой степени нарушений.
- количественное определение жира в кале – трудоемкий, но достаточно информативный тест (нормальное количество жира в кале менее 5 г/сут.).
- Зондовые методы – 1) секретин–панкреозиминовый (секретин–холецистокининовый) тест, 2) непрямой зондовый метод (тест Лунда). Тесты информативные, но трудоемкие, дорогостоящие и могут иметь осложнения. В настоящее время применяются редко.
- Беззондовые методы диагностики проще, дешевле и несут минимальный риск осложнений. Однако обладают меньшей чувствительностью и специфичностью, чем зондовые методы. Все они основаны на пероральном введении специфических субстратов для ферментов ПЖ. После взаимодействия последних с ферментами ПЖ в моче и/или в сыворотке крови определяются продукты расщепления, по количеству которых судят о степени внешнесекреторной недостаточности. 1) Бентирамидный тест (NBT–PABA тест). NBT – специфичный для химотрипсина трипептид, расщепляется до РАВА, которая определяется в моче; 2) йодо-липоловый тест: липаза расщепляет йодолипол до йодидов, которые определяются в моче; 3) флюоресцеин–дилауратный тест
5. Оценка инкреторной функции поджелудочной железы. Расстройства углеводного обмена при ХП выявляются примерно у 1/3 больных. Всем пациентам с ХП рекомендуется проводить глюкозотолерантный тест для выявления НТГ и СД.
Лечение ХП
Поскольку ведущим патогенетическим механизмом при ХП является активация собственных ферментов, основной мишенью патогенетической терапии будет являться именно внешнесекреторная функция ПЖ. Что важно, снижения собственной секреции ПЖ мы должны добиваться не только при обострении, но и в ремиссии ХП. Это необходимо и для лечения панкреатической боли, и для снижения степени воспаления в ПЖ.
Основными стимуляторами секреции ПЖ являются соляная кислота, желчные кислоты, жиры, особенно животного происхождения, алкоголь. Важно максимально уменьшить влияние этих факторов на ПЖ.
Диетотерапия
Алкоголь исключается на всех стадиях ХП вне зависимости от причины его развития. Также исключают соленую, жареную и жирную пищу. При обострении ХП в первые 2 дня рекомендован голод. Разрешается только прием жидкости в количестве 1,0-1,5 л в сутки (5-6 раз по 200 мл). Назначают щелочную минеральную воду без газа, отвар шиповника, некрепкий чай.
По мере улучшения состояния (обычно на 2–3–й день от начала обострения) можно медленно расширять диету. При этом важно соблюдать основные принципы диетотерапии больных ХП - диета должна быть механически и химически щадящей, малокалорийной и содержащей физиологическую норму белка (с включением 30% белка животного происхождения). Так как жидкая пища и углеводы в наименьшей степени стимулирую панкреатическую и желудочную секрецию, перорально питание начинают со слизистых супов, жидких протертых молочных каш, овощных пюре и киселей. При легких обострениях назначают овсяную или рисовую каши на воде, макаронные изделия, обезжиренную белковую пищу.
Фармакотерапия
Принципы лечения панкреатической боли
1. Диета и исключение алкоголя!
2. Анальгетики. Для быстрого купирования боли назначается поэтапная аналгезирующая терапия включающая спазмоанальгетики. При отсутствии эффекта в течение 3–4 часов назначаются нейролептик (дроперидол 2,5–5 мг + фентанил 0,05–0,1 мг в/в. Нередко дополнительно используется в/в капельно введение лидокаина по 400 мг/сут. (4 мл 10% раствора 100 мл изотонического раствора хлорида натрия или глюкозы). При выраженном болевом синдроме, не поддающемся лечению, назначаются наркотические средства (промедол).
3. Панкреатические ферменты. Для купирования панкреатической боли необходимо высокое содержание липазы и трипсина. Важным является исключение желчных кислот в ферментном препарате.
Таким требованиям удовлетворяет ПАНЗИНОРМ ФОРТЕ 20000. Препарат содержит в каждой таблетке свиной панкреатин с энзимной активностью: липазы 20000 ЕД Ph.Eur., амилазы 12000 ЕД Ph. Eur., протеазы 900 ЕД Ph. Eur. Препарат выпускается в виде таблеток, покрытых пленочной оболочкой. Входящие в его состав панкреатические ферменты (липаза, α–амилаза, трипсин, химотрипсин) способствуют расщеплению белков до аминокислот, жиров – до глицерина и жирных кислот, крахмала – до декстринов и моносахаридов, снижая таким образом стимулирующее влияние пищи на секрецию ПЖ. Трипсин также подавляет стимулированную секрецию поджелудочной железы, оказывая аналгезирующее действие. Панкреатические ферменты высвобождаются из лекарственной формы в щелочной среде тонкого кишечника, т.к. защищены от действия желудочного сока оболочкой, что также повышает эффективность данного препарата. Максимальная ферментативная активность препарата отмечается через 30–45 мин. после приема.
Очень важен правильный режим приема препарата. Так, для купирования болевого синдрома ПАНЗИНОРМ ФОРТЕ 20000 необходимо назначать в период голодания по 1 таблетке каждые 3 часа или по 2 таблетки каждые 6 часов (1–3 дня), а после возобновления приема пищи – по 1 таб. за 20–30 мин. до еды. А для заместительной терапии внешнесекреторной недостаточности ПАНЗИНОРМ ФОРТЕ 20000 назначается по 1–2 таблетке вместе с едой.
4. Соматостатин и октреотид назначаются в основном при тяжелых обострениях ХП и при ОП.
5. Антисекреторные препараты. С целью снижения секреции ПЖ назначают ингибиторы протонной помпы (омепразол), или Н2–блокаторы (ранитидин), алюминий содержащие антациды (рутацид), связывающие желчные кислоты.
Заместительная полиферментная терапия
Для компенсации внешнесекреторной недостаточности поджелудочной железы, как правило, применяют высокоактивные ферментные препараты, содержащие большие дозы энзимов (не менее 10 000 ЕД липазы). Заместительная терапия необходима при заболеваниях, сопровождающихся атрофией более чем 90% паренхимы органа . Доза ферментов зависит от степени внешнесекреторной недостаточности, а также от способности пациента соблюдать диету. При внешнесекреторной недостаточности поджелудочной железы однократная доза ферментов составляет от 10 000 до 20 000, а иногда – до 30 000 ед. липазы. Эффективность терапии оценивается клинически и лабораторно (копрологическое исследование, экскреция жира с калом, эластазный тест). Доказанной эффективностью в отношении коррекции экскреторной функции ПЖ обладает ПАНЗИНОРМ 10000. Препарат выпускается в форме капсулы, каждая содержит панкреатин в виде пеллет, с активностью липазы 10000 ЕД Ph. Eur, амилазы не менее 7200 ЕД Ph. Eur., протеазы не менее 400 ЕД Ph. Eur. Препарат обладает высокой ферментной активностью. ПАНЗИНОРМ 10000 принимают по 1–2 капсулы во время еды 3 р/сут.
При правильно подобранной дозе ферментов у больных стабилизируется или увеличивается вес, прекращаются диарея, метеоризм, боли в животе, исчезает стеаторея и креаторея. ПАНЗИНОРМ 10000 при ХП с внешнесекреторной недостаточностью назначается пожизненно. Дозы могут снижаться при соблюдении строгой диеты с ограничением жира и белка и увеличиваться при ее расширении.
Инфузионная и дезинтоксикационная терапия
При тяжелых обострениях в течение первых дней обострения показано в/в введение жидкости 3 и более л/сут.: реополиглюкин (400 мл/сут.), гемодез (300 мл/сут.), 10% раствор альбумина (100 мл/сут.), 5–10% раствор глюкозы (500 мл/сут.), что наряду с уменьшением болевого синдрома и интоксикации предупреждает развитие гиповолемического шока.
ЛИТЕРАТУРА
1. Коротько Г.Ф. Регуляция секреции поджелудочной железы // Росс. журн. гастроэн терол., гепатол. и колопроктол. – 1999. –№ 4. – С. 6–15.
2. Маев И.В., Казюлин А.Н., Кучерявый Ю.А. и др. Некоторые вопросы эпидемиологии хронического панкреатита // Клинико–эпидемиологические и этно–экологические проблемы заболеваний органов пищеварения: Материалы Третьей Восточно–Сибирской гастроэнтерологической конференции / Под ред. проф. В.В. Цукано ва. – Красноярск, 2003. – С. 9–52.
3. Тучина Л.М., Порошенко Г.Г. Распространенность заболеваний поджелудочной железы среди населения г. Москвы // Росс. гастроэнтерол. журн – 2001 –№ 2 – С. 154.
4. Минько А.Б., Пручанский В.С, Корытова Л.И. Комплексная лучевая диагностика заболеваний поджелудочной железы.– СПб: Гиппократ.– 2001.– 134 с.
5. Багненко С.Ф., Курыгин А.А., Рухляда Н.В., Смирнов А.Д. Хронический панкреатит: Руководство для врачей. – СПб.: Питер, 2000. – 416 с.
6. Кокуева О.В., Цымбалюк Ю.М., Новоселя Н.В. Особенности ультразвуковой картины при хроническом панкреатите в сочетании с язвенной болезнью двенадцатиперстной кишки // Клин, мед. 2001. № 7. С. 57–60.
7. И.В. Маев, А.Н. Казюлин, Ю.А. Кучерявый / Хронический панкреатит. – М.: Медицина, 2005. – 504 с.
8. Ивашкин В.Т., Хазанов А.И., Пискунов Г.Г. и др. О классификации хронического панкреатита // Клин, мед. – 1990. –№ 10. – С.96-99.
9. Яковенко, А.В. Практические подходы к лечению хронического панкреатита / А.В. Яковенко, Н.А. Агафонова, Э.П. Яковенко // Эксперимент. и клинич. гастроэнтерология. – 2007. – N 6. – C. 67–70.
10. Sarles H., Pastor J., Pauli A.M., Barthelemy M. Determination of pancreatic function. A statisti cal analysis conducted in normal subjects and in patients with proven chronic pancreatitis (duodenal intubation, glucose tolerance test, determination of fat content in the stools, sweat test) // Gastroenterol. 1963. Vol. 99. P. 279–300.
Версия: Справочник заболеваний MedElement
Хронический панкреатит алкогольной этиологии (K86.0)
Гастроэнтерология
Общая информация
Краткое описание
Термином "хронический панкреатит
" обозначают группу хронических заболеваний поджелудочной железы (ПЖ) различной этиологии, преимущественно воспалительной природы. Заболевание сопровождается фазово-прогрессирующими очаговыми, сегментарными или диффузными дегенеративными, деструктивными изменениями экзокринной части ПЖ, атрофией железистых элементов (панкреоцитов) и замещением их соединительной (фиброзной) тканью; изменениями в протоковой системе ПЖ с образованием кист и конкрементовКонкременты - камни, плотные образования, встречающиеся в полостных органах и выводных протоках желез человека.
, с различной степенью нарушения экзокринной и эндокринной функций.
Хронический алкогольный панкреатит
(ХАП) выделен в отдельную нозологическую единицу по рекомендации ВОЗ, исходя из следующих соображений:
- алкоголь и его суррогаты являются наиболее частой причиной возникновения хронического панкреатита;
- причину (злоупотребление алкоголем) возможно и необходимо модифицировать без существенных затрат со стороны системы здравоохранения.
Классификация
Общепризнанная классификация хронического алкогольного пакреатита (ХАП) отсутствует. При необходимости можно воспользоваться несколькими вариантами классификации клинических проявлений хронического панкреатита (ХП).
I. Степень тяжести ХП
1. Легкое течение:
Обострения редкие (1-2 раза в год), непродолжительные, быстро купирующиеся;
Умеренный болевой синдром;
Вне обострения самочувствие больного улучшается;
Отсутствует уменьшение массы тела;
Не нарушена функция поджелудочной железы;
Копрологические анализы в пределах нормы.
2. Течение средней степени тяжести:
Обострения 3-4 раза в год, протекают с типичным длительным болевым синдромом;
Выявляется панкреатическая гиперферментемия;
- наблюдаются умеренное снижение внешней секреторной функции поджелудочной железы и похудание;
- отмечается стеатореяСтеаторея - повышенное содержание в кале нейтрального жира, жирных кислот или мыл.
, креатореяКреаторея - повышенное содержание в кале непереваренных мышечных и соединительнотканных волокон
, амилореяАмилорея - выделение с испражнениями увеличенного количества непереваренного крахмала, чаще при усиленной перистальтике кишечника
.
3. Тяжелое течение:
Частые и длительные обострения с упорным болевым синдромом;
Панкреатогенные поносы;
Падение массы тела, вплоть до прогрессирующего истощения;
Резкое нарушение внешнесекреторной функции;
Осложнения (сахарный диабет, псевдокисты, сдавливание двенадцатиперстной кишки увеличенной головкой поджелудочной железы).
II.В течении ХП можно выделить следующие этапы заболевания:
1. Начальный этап -
протяженность в среднем 1-5 лет (до 10 лет). Наиболее частое проявление - боль различной интенсивности и локализации:
- в верхней части правой половины живота при поражении головки поджелудочной железы (ПЖ);
- в эпигастральной области при поражении тела ПЖ;
- в левом подреберье при поражении хвоста ПЖ;
- боли опоясывающего характера (встречаются нечасто, связаны с парезомПарез - уменьшение силы и/или амплитуды произвольных движений, обусловленное нарушением иннервации (обеспечения нервами и связи с центральной нервной системой) соответствующих мышц
поперечно-ободочной кишки).
При наличии диспепсического синдрома, он имеет явно сопутствующий характер и первым купируется при лечении.
2. Развернутая картина
болезни наблюдается позднее, в основном через 5-10 лет. Основные проявления: боль, признаки внешнесекреторной недостаточности, элементы инкреторной недостаточности (гипергликемия, гипогликемия). На первое место выходят признаки внешнесекреторной недостаточности.
3. Осложненный вариант
течения ХП (в любом периоде). Стихание активного патологического процесса или развитие осложнений чаще отмечаются через 7-15 лет от начала болезни. У 2/3 больных регистрируется стихание патологического процесса за счет адаптации больного к ХП (алкогольная абстиненцияАлкогольная абстиненция - симптомокомплекс соматических, неврологических и психопатологических расстройств у больного алкоголизмом, возникающих в результате внезапного прекращения запоя или снижения доз алкоголя
, соблюдение диеты), у 1/3 развиваются осложнения. Наблюдается изменение интенсивности болей или их иррадиации, динамики под влиянием лечения.
Этиология и патогенез
Главный этиологический фактор хронического алкогольного панкреатита - злоупотребление алкоголем.
В настоящее время отсутствует однозначное мнение о том, какая доза спирта способствует развитию заболевания. Разные авторы указывают, что хронический панкреатит развивается при употреблении от 20 до 100 грамм алкоголя в сутки
(в пересчете на чистый спирт)
в течение 2-20 лет.
В экономически развитых странах
у 60-70% больных хроническим панкреатитом отмечают длител
ьный прием (5-20 лет) спирта в дозе более 150 мг/сутки.
В то же время врачами наркологами и гастроэнтерологами установлено, что
к развитию изменений в поджелудочной железе (чаще всего кальцинозу и накоплению жира в ацинарных клетках) приводит
употребление алкоголя
даже в дозе 80-120 мл в сутки
на протяжении 8-12 лет.
В течении алкогольного панкреатита выделяют две стадии:
1. Воспалительная стадия
- возникают
повреждение эпителиальных клеток панкреатических протоков, воспалительная инфильтрация паренхимы различных участков ПЖ.
2. Кальцифицирующая стадия
- развиваются фиброз и обтурация просвета протоков, появляются очаги обызвествления в паренхиме ПЖ, на фоне неравномерного фиброза ПЖ формируются камни в ее протоках (кальцифицирующий хронический панкреатит).
Основные факторы патогенеза ХАП:
1. Токсико-метаболическое и повреждающее действие алкоголя на ПЖ. Д егенеративные и гипоксические изменения в ацинарных клетках развиваются д аже после разового приема большого количества алкоголя. При продолжительном употреблении алкоголя формируются очаги дегенерации в цитоплазме ацинарных клеток эпителия протоков, некроз, атрофия, фибрoз, кальциноз железы.
2. Нарушение функции сфинктера Одди - уменьшение амплитуды его сокращений и увеличение количества ретроградных перистальтических волн (дуоденопанкреатический рефлюкс).
3. Нарушение секреторной функции ПЖ и преципитация белков в ее протоках. В начальном периоде алкоголь стимулирует функцию ПЖ через усиление выделения секретина, гастрина, панкреозимина. При длительном воздействии алкоголя экзокринная функция ПЖ угнетается, наблюдается ее диссоциированное нарушение - преимущественное снижение секреции воды и бикарбонатов при менее выраженном уменьшении секреции пищеварительных ферментов. В результате происходит уменьшение объема жидкой части секрета, увеличение его вязкости, наступает преципитация белка. Увеличение белковых преципитатов в количестве и объеме постепенно вызывает сужение протоков с последующей полной их обструкцией. При продолжении секреторной деятельности поджелудочной железы это приводит к прогрессирующему увеличению давления в протоках ПЖ и ее отеку.
Таким образом, патогенез ХАП связан с нарушением формирования растворимых белково-кальциевых ассоциатов. Уже на самых ранних этапах формирования ХАП в протоках ПЖ выявляются белковые преципитаты, которые представляют собой нерастворимый фибриллярный белок (литостатин) с отложениями кальция в основном в виде кальцитов (карбонатов). Следует отметить, что существуют три разновидности панкреатических камней: кальций-карбонатно-протеиновые, преимущественно кальций-карбонатные и белковые (из органического материала). Последние , как правило, не связаны с приемом алкоголя и формируются вследствие недостаточности питания.
Эпидемиология
Алкоголь является ведущей причиной хронических панкреатитов - от 40 до 95% всех форм заболевания. Регистрируется в основном у мужчин. Распознать природу хронического панкреатита трудно, так как при сборе анамнеза больные зачастую заявляют, что пьют "как все". Тем не менее пациент с алкогольным хроническим панкреатитом потребляет алкоголь в значительно больших дозах, чем рекомендуется современными медицинскими постулатами. Поджелудочная железа более чувствительна к алкоголю по сравнению с печенью (токсические дозы для поджелудочной железы на 1/3 меньше, чем для печени). Тип алкогольных напитков и способ их употребления не имеют решающего значения в развитии заболевания.
Клинически выраженные проявления хронического алкогольного панкреатита развиваются у женщин через 10-12 лет, а у мужчин через 17-18 лет от начала систематического злоупотребления алкоголем.
Факторы и группы риска
Алкоголь является одним из основных этиологических факторов, ассоциирующихся с хроническим панкреатитом, в развитых странах. Доказаны наличие логарифмической зависимости риска хронического панкреатита от суточного потребления алкоголя и белка и U-образная зависимость от суточного потребления жира. Типичные характеристики больных: достаточно хорошие социально-экономические условия жизни (страны Европы, Япония, США), мужской пол, возраст старше 30-40 лет, высокий уровень суточного потребления белка и жира, употребление ежедневно более 20 г алкогольных напитков (в пересчете на чистый этанол).
Риск развития хронического панкреатита возрастает при наличии курения, как дополнительного патологического фактора. В данном случае характерно развитие панкреатита в более раннем возрасте. У курящих лиц хронический панкреатит регистрируется в 2 раза чаще по сравнению с некурящими, при этом риск развития панкреатита растет пропорционально количеству выкуриваемых сигарет.
Клиническая картина
Cимптомы, течение
При описании клинических проявлений хронического панкреатита (ХП) выделяют несколько синдромов.
Синдром экзокринной недостаточности. Проявляется потерей массы тела и диспептическими расстройствами. Вследствие липазной недостаточности наблюдаются учащение стула до 2-4 и более раз в сутки, полифекалия, избыточное газообразование, вздутие живота, стеаторея. При выраженном дефиците липазы у пациентов отмечается "панкреатический стул" (большого объема с сероватым оттенком, зловонный). Поверхность каловых масс может быть покрыта тонкой пленкой жира. Нарушено всасывание жирорастворимых витаминов. Трофические расстройства (сухость кожи, тусклость и ломкость ногтей и волос, трещины в углах губ, на языке) при синдроме нарушенного полостного пищеварения наблюдаются редко.
Воспалительно-деструктивный синдром.
Воспаление, склероз и кистообразование могут сопровождаются сдавливанием холедоха, развитием желтухи с ахолией, кожным зудом. Желтуха имеет рецидивирующий характер, возникает или увеличивается чаще после болевого приступа. У 1/3 больных отмечается гипербилирубинемия. При ХП может наблюдаться феномен "уклонения" ферментов: усиленное поступление ферментов в кровь, обусловленное нарушением целостности паренхимы железы или протоковой гипертензией.
Болевой синдром
в основном обусловлен нарушением оттока панкреатического сока и протоковой гипертeнзией, а также вовлечением в хронический воспалительный процесс париетальной брюшины, рубцовыми изменениями парапанкреатической клетчатки и смежных органов.
Обычно боли постоянные и зачастую мучительные. Боли локализуются в эпигастральной области, бывают опоясывающими; усиливаются при приеме жирной и острой пищи.
Иррадиация зависит от локализации воспалительно-дегенеративного процесса в поджелудочной железе. При поражении головки железы боли иррадиируют в правое подреберье, тела железы - в эпигастральную область, хвоста железы - в левое подреберье. Примерно в 10% случаев отмечается иррадиация болей в область сердца.
Болевой синдром зависит от характера пищи: при алкогольном панкреатите боли часто появляются после приема острой и кислой пищи; при холангиогенном панкреатите - после приема жирной пищи.
Синдром инкреторной недостаточности
характеризуется частым развитием гипогликемических состояний вследствие низкого уровня глюкагона в сыворотке крови или гипергликемии, в особенности на высоте воспалительно-деструктивного синдрома. Синдром проявляется приступами сильного голода и признаками сахарного диабета с меньшей потребностью в инсулине. Развивается "псевдопанкреатическая триада": гипергликемия, сухость во рту и жажда без кетоацидоза.
Диспептический синдром: изменение аппетита (вплоть до анорексии), отвращение к жирной пи-ще, тошнота, рвота, не приносящая облегчения, слюнотечение, метеоризм, вздутие кишечника, поносы, которые иногда чередуются с запорами.
Астено-вегетативный синдром
проявляется слабостью и снижением работоспособности, раздражительностью (особенно "на голодный желудок"), нарушением сна.
(Пальцев А.И., 2000)
| Основные клинические симптомы |
Количество больных (%) |
| Боли в левом подреберье слева от пупка | 71,3 |
| Боли в эпигастрии слева от срединной линии | 61,8 |
| Боли в эпигастрии справа от срединной линии | 56,7 |
| Опоясывающие боли в верхней половине живота | 24,2 |
| Боли в спине | 18,5 |
|
Определение болевых точек: - Дежардена - Губергрица - Мено-Робсона - Кача - Малле-Ги |
55,4 68,1 66,8 61,1 53,5 |
| Симптом Боткина | 17,2 |
| Симптом Кочаловского | 22,3 |
| Отрыжка | 92,3 |
| Изжога | 74,5 |
| Тошнота | 98,7 |
| Полифекалия | 20,4 |
| Стеаторея | 23,5 |
| Повышение активности амилазы | 54,1 |
Диагностика
Диагностика алкогольного панкреатита в принципе строится на диагностике хронического панкреатита (ХП) как такового и выявлении его алкогольной этиологии.
Анамнез
Хронический панкреатит клинически характеризуют два ведущих симптома: рецидивирующая или постоянная абдоминальная боль и экзокринная недостаточность поджелудочной железы (синдром мальабсорбции, стеаторея, трофологическая недостаточность). В связи с этим при сборе анамнеза необходимо выяснить время появления первых симптомов, проследить их динамику, оценить эффективность и адекватность проводимой ранее терапии.
Важнейший анамнестический аспект, на котором может базироваться клинический диагноз - прием алкоголя и перенесенный ранее рецидивирующий острый панкреатит, поскольку в настоящее время можно считать доказанной возможность трансформации острого панкреатита в хронический, особенно при продолжении приема алкоголя.
Необходимо оценить семейный анамнез, изучить спектр сопутствующих заболеваний, определить наличие, выраженность и длительность воздействия алкоголя, что может помочь в установлении этиологии заболевания.
Физикальное обследование
Общее состояние зависит от выраженности болевого синдрома и симптомов интоксикации, степени белково-энергетической недостаточности, нарушений центральной и периферической гемодинамики. В связи с этим оно варьируется от удовлетворительного до крайне тяжелого. Степень состояния питания также весьма вариабельна. Язык обложен, иногда суховат.
Крайне редко наблюдаются типичные для острого панкреатита симптомы, связанные с "уклонением" ферментов в кровь.
Часто отмечают симптомы, связанные со значительным отеком поджелудочной железы (ПЖ):
Субиктеричность или иктеричность слизистых оболочек ("ранняя" желтуха) и кожи, которые становятся менее выраженными и исчезают по мере уменьшения болевого синдрома;
Вынужденное коленно-локтевое положение (уменьшение давления на солнечное сплетение);
Симптом Фитца - "выбухание" эпигастрия вследствие дуоденостеноза;
Икота (раздражение диафрагмального нерва).
Симптомы белково-энергетической недостаточности:
Тотальная мышечная гипотрофия (маразм);
Мягкие, рыхлые отеки нижних конечностей, крестца, передней брюшной стенки, выпот в полостях (квашиоркор);
Симптом Грота - атрофия подкожной клетчатки в проекции ПЖ;
Синдром Бартельхеймера - пигментация кожи над областью ПЖ;
- синдром Эдельманна - кахексия, фолликулярный гиперкератоз, истончение и диффузная сероватая пигментация кожи, паралич глазных мышц, вестибулярные расстройства, полиневриты, изменения психики.
Пальпация.
При поверхностной пальпации определяется болезненность в эпигастрии, левом подреберье; при глубокой пальпации - болезненность в проекции ПЖ. Для определения проекции ПЖ на переднюю брюшную стенку, срединную линию от мечевидного отростка до пупка делят на трети. Между верхней и средней третями проводят горизонтальную линию - влево до левой реберной дуги, вправо - в два раза меньше, чем влево (2/3 горизонтальной линии находятся слева, а 1/3 - справа). Поскольку ПЖ расположена забрюшинно, в ее проекции обычно отсутствует резистентность.
Болезненность в зоне Шоффара и точке Дежардена условно свидетельствует о патологии головки ПЖ, а болезненность в зоне Губергрица-Скульского (симметрична зоне Шoффара) и в точке Губергрица (симметрична тoчке Дежардена) - о патологии тела ПЖ.
Дополнительное значение при пальпации придают следующим симптомам:
Боль при надавливании в левом реберно-позвоночном углу (точка Мейо-Робсона) свидетельствует о патологии хвоста ПЖ;
Симптом Ниднера - при пальпации всей ладонью хорошо определяется пульсация аорты в левом подреберье из-за давления на нее ПЖ;
- симптом Мюсси слева - боль при надавливании между ножками грудино-ключично-сосцевидной мышцы у прикрепления к медиальному краю ключицы;
Симптом Воскресенского - отсутствие пульсации брюшной аорты; свидетельствует о значительном увеличении ПЖ, которая "прикрывает" аорту.
Оценка экзокринной функции поджелудочной железы
Существует две группы тестов для оценки экзокринной функции ПЖ:
- зондовые методы, требующие введения кишечного зонда;
- неинвазивные беззондовые тесты.
Прямой зондовый метод
- секретин-панкреозиминовый (секретин-холецистокининовый) тест. Имеет высокую диагностическую точность, чувствительность и специфичность метода составляют более 90%. Признается большинством ученых в качестве "золотого стандарта" определения нарушений экзокринной функции ПЖ (определенное число специалистов считает проведение прямого зондового метода обязательным при диагностике ХП).
С помощью теста невозможно проводить дифференциальную диагностику с другими заболеваниями ПЖ, поскольку при раке ПЖ, муковисцидозе и других заболеваниях ПЖ регистрируют патологические результаты этого теста в 75-90% случаев.
Интерпретация результатов зондового исследования
(выделение патологических типов секреции ПЖ).
1. Гипосекреторный тип
: снижение продукции ферментов, бикарбонатов при нормальном объеме секрета. Характерен для диффузного фиброза ПЖ (поздние стадии ХП) и муковисцидоза (более редко определяют при раке ПЖ).
2. Гиперсекреторный тип
: нормальные или повышенные объемы секрета и дебит бикарбонатов, увеличение активности ферментов. Типичен для начальных воспалительных процессов в ПЖ без признаков атрофии ацинарных клеток и выраженного фиброза. Регистрируется в начальных стадиях ХП, когда задержка оттока секрета ПЖ недлительная и незначительная (при кратковременном спазме сфинктера Одди, язвенной болезни двенадцатиперстной кишки и пр.).
3. Обтурационный тип
делят на 2 подтипа:
3.1 Нижний блок: уменьшение объема секрета при нормальной концентрации бикарбонатов и ферментов, что приводит к снижению их дебита. Наблюдается при панкреатитах, развившихся в результате процессов, затрудняющих отток секрета ПЖ (стойкий спазм сфинктера Одди, папиллиты, обтурация главного панкреатического протока конкрементом, опухоли фатерова соска или головки ПЖ).
3.2 Верхний блок: снижение объема секрета и повышение концентрации ферментов (при их сниженном дебите), нормальное содержание бикарбонатов. Подобный вариант свидетельствует об отеке ПЖ и характерен для отечного панкреатита (обострение ХП).
4. Дуктулярный тип:
снижение объема секрета, нормальная продукция ферментов, резкое повышение концентрации бикарбонатов. Такие изменения могут быть связаны с воспалением протоков и нарушением реабсорбции бикарбонатов.
Недостатки прямого зондового метода заключаются в необходимости дуоденального зондирования (обременительно для пациента), большом объеме работы лаборанта, высокой стоимости и малой доступности стимуляторов ПЖ.
Непрямой зондовый метод -
тест Лунда. Чувствительность метода у больных с ХП составляет 90%. Отдельные ложноположительные результаты могут обнаруживать у больных с тонкокишечной мальабсорбцией, целиакией, сахарным диабетом. На ранних стадиях внешнесекреторной недостаточности ПЖ тест Лунда менее чувствителен.
Преимущества метода состоят в том, что он дешевле, проще в выполнении и удобнее для больного. Недостатки заключаются в необходимости дуоденального зондирования, отсутствии возможности определения объема секреции и концентрации бикарбонатов, а также в том, что на результаты теста оказывают влияние интрадуоденальная кислотность и эндогенная секреция гормонов из двенадцатиперстной кишки (ДПК).
Непрямые методы без дуоденального зондирования
Все беззондовые методы основаны на пероральном введении специфических субстратов для ферментов ПЖ. После взаимодействия субстратов с ферментами ПЖ в моче или сыворотке крови определяют продукты расщепления. Количество продуктов расщепления позволяет судить о внешнесекреторной недостаточности ПЖ. Принципиальный недостаток неинвазивных методов состоит в ослаблении их чувствительности при умеренно выраженной степени экзокринной панкреатической недостаточности.
1. Бентирамидный тест (NBT-PABA тест) - чувствительность - 83%, специфичность - 89%. В США этот метод не используется.
2. Определение степени потребления плазменных аминокислот
поджелудочной железой применяется для исследования функции ПЖ у больных с тяжелой внешнесекреторной недостаточностью. Основан на том, что при стимуляции секретином ПЖ поглощает большое количество аминокислот из плазмы крови, необходимых для синтеза панкреатических ферментов. Чувствительность метода - 69-96%, специфичность - 54-100%.
3. Качественное копрологическое исследование
осуществляют при следующих условиях: больные соблюдают стандартную диету (например, диету Шмидта), а также в этот период времени не применяются полиферментные препараты. Критерии внешнесекреторной недостаточности: повышенное содержание в кале нейтрального жира и мыл при малоизмененном содержании жирных кислот. Повышенное содержание мышечных волокон указывает на наличие креатореи.
4. Количественное определение жира в кале
. В норме после приема 100 г жира с пищей за сутки выделяется до 7 г нейтрального жира и жирных кислот. Увеличение количества жира свидетельствует о расстройствах переваривания и всасывания жира, чаще всего панкреатического происхождения. Определение тяжести стеатореи является простым и надежным показателем выраженной внешнесекреторной недостаточности ПЖ.
При неполном (неправильном) сборе кала и на фоне неадекватной диеты достоверность теста снижается. Тест неспецифичен для ряда заболеваний, поэтому не может быть использован для определения панкреатического характера стеатoреи. Данные теста почти всегда выходят за границы нормы при поражении подвздошной кишки и при бактериальной контаминации тонкой кишки.
5. Иммуноферментный метод определения эластазы 1 в кале
больных ХП получил широкое распространение в последнее время. Чувствительность эластазного теста у больных с экзокринной панкреатической недостаточностью тяжелой и средней степени приближаются к таковым при секретин-панкреозиминовом тесте. По данным большинства зарубежных исследователей, чувствительность составляют 90-100% (при легкой степени - 63%), специфичность - 96%. Это простой и быстрый метод, не имеющий ограничений в применении и позволяющий определять состояние внешнесекреторной функции ПЖ на более ранних стадиях.
О
бщий анализ крови
При обострении ХП может быть выражен лейкоцитоз, сдвиг формулы влево, нейтрофилез, увеличение СОЭ.
На фоне лечения наблюдается быстрая отчетливая редукция лейкоцитоза, несколько позднее нормализуется значение СОЭ (считается благоприятным клиническим признаком).
Неспецифическим маркером развития осложнений выступают длительно сохраняющийся лейкоцитоз со сдвигом влево и повышенные цифры СОЭ.
Достаточно редко определяют лейкоцитоз у больных ХП с внешнесекреторной недостаточностью. Более того, характерна умеренная лейкопения, которая свидетельствует о наличии трофологической недостаточности. В этом случае отмечают длительно сохраняющееся повышение СОЭ, наиболее часто обусловленное диспротеинемией.
У больных с тяжелыми формами синдрома мальабсорбции могут присутствовать признаки железодефицитной, В 6 -, В 12 - и фолиеводефицитной анемии (наиболее часто - смешанной анемии).
Биохимический анализ крови:
1. Сниженный уровень общего белка крови, альбумина, транстиретина, трансферрина, ферритина и других белков, которые характеризуют висцеральный пул белков и степень трофологической недостаточности.
2. Диспротеинемия: снижение альбумин-глобулинового коэффициента, относительное увеличение и а 1 и а 2 -глобулинов.
3. Нередко - повышенные показатели трансаминаз крови, ГГТ, лактат дегидрогеназы.
4. Для развившегося синдрома холестаза характерно повышение билирубина, преимущественно прямого, холестерина и щелочной фосфатазы. Это может быть обусловлено блоком холедоха, развитием реактивного гепатита.
5. У больных алкогольным ХП повышение в крови активности печеночных ферментов может быть обусловлено самостоятельной патологией печени (токсический гепатит, цирроз печени).
6. Нередко - гипокальциемия, степень которой может служить одним из критериев тяжести заболевания. При обнаружении гиперкальциемии возможено наличие гиперпаратиреоза как причинного фактора ХП.
Повышение уровня онкомаркеров (СА 19-9, карциноэмбриональный антиген - КЭА) выше значения, допустимого для воспаления, является косвенным признаком трансформации ХП в рак ПЖ. При ХП допустимо повышение СА 19-9 в три раза, КЭА - в два раза. Данные онкомаркеры не специфичны для рака ПЖ и могут быть выявлены при раке желудка, холангиогенном и колоректальном раке.
Инструментальные исследования
1. Классическое (трансабдоминальное) УЗИ считают первой линией диагностики. При использовании современного оборудования в большинстве случаев УЗИ достаточно для качественной визуализации всех отделов ПЖ, ее паренхимы и протоковой системы. Помимо этого УЗИ позволяет одновременно осмотреть печень, желчный пузырь, выявить явления гастро- и дуоденостаза.
Патогномоничные признаки:
- диффузное изменение размера ПЖ;
- неровность и нечеткость контуров;
- гиперэхогенность паренхимы (вне отечно-интерстициальных изменений);
- дилатация и утолщение стенок главного панкреатического протока;
- кальцификация паренхимы и вирсунголитиаз.
Совпадение гистологической картины при ХП (калькулезный, кистозный, индуративный, фиброзный и пр.) по результатам аутопсии с прижизненными данными УЗИ составляет 83,3%.
2. Эндоскопическая ультрасонография
(ЭУС) - высокоинформативный метод УЗ-диагностики заболеваний ПЖ. Сканирование осуществляется через стенку желудка и ДПК. Метод позволяет детально изучить структуру ткани ПЖ, состояние протоковой системы, оценить размеры парапанкреатических лимфоузлов и выявить конкременты протоковой системы, а также помогает в дифференциальной диагностике панкреатита с раком ПЖ.
У больных билиарнозависимыми формами панкреатитов ЭУС применяется для диагностики холедохолитиаза, поскольку обладает существенно большей чувствительностью, чем трансабдоминальное УЗИ.
ЭУС позволяет с большой точностью выявлять участки панкреонекроза и перипанкреатических жидкостных скоплений, что может играть большое прогностическое значение при тяжелых формах ХП.
ЭУС обладает равной или большей информативностью по сравнению с КТ, МРТ и ЭРХПГ, но менее инвазивна, чем ЭРХПГ.
Повышает диагностическую ценность ЭУС возможность проведения с большой точностью пункционной аспирационной биопсии ПЖ, особенно во всех случаях подозрения на опухоль. Чувствительность и специфичность метода превышают 90%.
Внутрипротоковое УЗИ ПЖ имеет еще большую информативность, а его диагностическое значение в отношении панкреатитов и опухолей ПЖ достигает 100%. Целесообразно проведение данного исследования для выяснения причины нарушения оттока секрета: при подозрении на аденому или рак большого дуоденального сосочка.
3.
Компьютерная томография
(КТ) помогает при постановке диагноза прежде всего на стадии осложнения панкреатита, когда наиболее часто выявляют кальцификацию, псевдокисты, поражение соседних органов, атрофию паренхимы ПЖ и малигнизацию.
Чувствительность и специфичность КТ составляют 80-90% и значительно колеблются в зависимости от стадии заболевания.
Спиральная КТ
с внутривенным болюсным усилением неионным контрастным веществом (йопромид, йогексол) используется в сложных диагностических случаях для уточнения патологии ПЖ. Данный метод позволяет точнее отличить участки деструкции от сохраненной паренхимы, оценить взаимоотношения ПЖ с сосудами, лимфатическими узлами, парапанкреатической клетчаткой, стенками желудка и ДПК.
Основное преимущество КТ, по сравнению с УЗИ, заключается в том, что обследование не затрудняется такими факторами, как тучность больных, наличие газа в толстой кишке и прочими. Тем не менее ложноотрицательные результаты отмечаются сравнительно часто.
При ХП достаточно эффективно сочетание УЗИ и КТ. При наличии сомнений применяется ЭРХПГ, как метод, обладающий более высокой диагностической информативностью.
4. Э ндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) считается "золотым стандартом" диагностики ХП в большинстве современных научных публикаций. Этот метод позволяет выявить стеноз главного панкреатического протока и определить локализацию обструкции, обнаружить структурные изменения мелких протоков, внутрипротоковые кальцинаты и белковые пробки, а также патологию общего желчного протока.
ЭРХПГ является важным методом при дифференциации ХП с раком ПЖ.
Чувствительность варьирует в пределах 71-93%, специфичность - 89-100%.
Ретроградное введение под давлением контраста в панкреатический проток при ЭРХПГ может стать причиной развития серьезных осложнений (острый панкреатит, холангит, сепсис, аллергические реакции на йодсодержащий контраст, кровотечение, перфорация ДПК и общего желчного протока). Частота осложнений составляет от 0,8 до 36,0%, летальность - 0,15-1,0%.
В ряде случаев после ЭРХПГ наблюдают повышение лабораторных маркеров холестаза и цитолиза гепатоцитов. Для достижения хороших результатов важно исключение больных с высоким риском осложнений и соответствующая предоперационная подготовка пациента.
ЭРХПГ имеет большое значение при диагностике аутоиммунного ХП, позволяя у всех больных выявить сегментарные или диффузные иррегулярные сужения главного панкреатического протока (типичный признак этой формы ХП).
5. МРТ и магнитно-резонансная холангиопанкреатография
(МРХПГ) в связи с более высокой чувствительностью и специфичностью, МРТ рассматривают в качестве альтернативной КТ методики при проведении дифференциальной диагностики ХП с раком ПЖ, при диагностике кист и псевдокист, врожденных аномалий развития ПЖ, включая pancreas divisum (расщепленная ПЖ).
Чувствительность МРТ - 92,2%, а специфичность - 97,1%.
В качестве первичного метода диагностики МРХПГ во многих диагностических ситуациях (особенно при непереносимости пациентами йодсодержащих препаратов и при декомпенсированном состоянии больных) может заменять ЭРХПГ, имеющую более высокий риск осложнений.
Информативность МРХПГ значительно превышает информативность других неинвазивных методик (УЗИ, КТ, МРТ). При МРХПГ выполняют и стандартную МРТ брюшной полости, при которой можно определить состояние паренхимы ПЖ и соседних органов.
При типичной картине холедохолитиаза как причины тяжелой атаки ХП (желтуха, расширение холедоха по данным УЗИ, хoлангит) показания к МРХПГ практически отсутствуют. Более целесообразно в данном случае проведение ЭРХПГ, обладающей также и лечебными возможностями (ЭПСТ, литоэкстракция и пр.).
МРХПГ может выступать как процедура выбора для диагностического скрининга, когда диагностические признаки холедохолитиаза сомнительны (диаметр общего желчного протока менее 10 мм, быстрая редукция маркеров холестаза, отсутствие признаков холангита и анамнестических указаний на желчнокаменную болезнь).
6. Дуоденоскопия
позволяет диагностировать патологию большого дуоденального сосочка, выявить заболевания желудка и ДПК, являющиеся возможной причиной развития ХП, выполнять селективный забор панкреатического сока для ферментного и морфологического исследования.
7. Метод манометрии сфинктера Одди
имеет ограниченное применение ввиду высокой частоты осложнений в 9-33% случаев (преимущественно атака ХП или ОП), высокой стоимости, а также в связи стем, что может быть выполнен только в специализированных медицинских центрах.
8. Рентгеновский метод. Обнаружение кальцификации ПЖ при обзорной рентгенографии органов брюшной полости считают наиболее достоверным рентгенологическим симптомом ХП, патогномоничным для этого заболевания.
При проведении рентгеноскопии органов грудной клетки иногда выявляют патогномоничные признаки осложнений тяжелой атаки ХП: левосторонний (реже двусторонний) экссудативный плеврит или дисковидный ателектаз нижней доли левого легкого, ограничение подвижности диафрагмы.
Критерии диагностики и диагностические алгоритмы
Для интерпретации данных, полученных при инструментальном и лабораторном обследовании, различными группами экспертов в разных странах предложены различные критерии диагностики.
Цюрихские диагностические критерии
Определенный алкогольный ХП.
В дополнение к общему и алкогольному анамнезу (>80 г/сут.), диагностическими считают один или более следующих критериев:
- кальцификация ПЖ;
- умеренные и выраженные изменения протоков ПЖ (кембриджские критерии);
- наличие экзокринной недостаточности, определяемое как присутствие стеатореи (>7 г жира в кале в сутки), прекращающейся, либо заметно уменьшающейся при приеме полиферментных препаратов;
- типичная гистологическая картина в ПЖ (при исследовании послеоперационного материала).
Вероятный алкогольный ХП.
В дополнение к общему и алкогольному анамнезу (>80 г/сут), диагноз ХП вероятен при наличии одного или более диагностических критериев:
- умеренные протоковые изменения (кембриджские критерии);
- рекуррентные или постоянные псевдокисты;
- патологический секретиновый тест;
- эндокринная недостаточность (в рамках нарушения толерантности к углеводам).
Диагностические критерии ХП Japan Pancreas Society
Определенный ХП.
При клиническом подозрении на ХП (хронические рецидивирующие абдоминальные боли и признаки экзокринной и эндокринной недостаточности) диагноз может быть установлен при обнаружении одного или более следующих признаков:
1. По данным УЗИ и КТ: интрапанкреатический калькулез.
2. По данным ЭРХПГ: участки расширения мелких панкреатических протоков по всей паренхиме ПЖ или неравномерное расширение главного панкреатического протока и проксимальных протоков с полным или неполным нарушением оттока (конкременты, белковые пробки).
3. По данным секретинового теста: патологически низкая концентрация бикарбонатов в сочетании со снижением продукции ферментов или уменьшением объема секреции.
4. Гистологическая картина: нерегулярный фиброз с разрушением и потерей экзокринной паренхимы в участках ткани.
5. Дополнительные критерии: белковые пробки, панкреатические камни, расширение протоков, гиперплазия и метаплазия протокового эпителия и формирование кист.
Вероятный ХП:
1. По данным УЗИ: усиленный рисунок, грубое несимметричное расширение панкреатических протоков или деформация ПЖ с нечетким контуром.
2. По данным КТ: деформация ПЖ с нечетким контуром.
3. По данным ЭРХПГ: единичные неправильной формы участки дилатации главного панкреатического протока; внутрипротоковые неконтрастирующиеся дефекты, похожие на неотвердевшие панкреатические камни или белковые пробки.
4. По данным секретинового теста: патологическое снижение концентрации бикарбонатов или уменьшение продукции ферментов в сочетании с уменьшенным объемом секреции.
5. По данным беззондовых тестов: одновременные изменения РАВТ-теста и теста на фекальный химотрипсин, наблюдаемые в течение нескольких месяцев.
6. Гистологическая картина: интралобулярный фиброз в сочетании с одним из следующих признаков: потеря экзокринной паренхимы; изолированные островки Лангерганса; псевдокисты.
Предварительный диагноз ХП можно поставить на этапе опроса больного.
В клинической практике диагноз основан на комбинации тестов.
УЗИ рекомендуют как первую ступень диагностики ввиду широкой распространенности и доступности.
При эластазном тесте в дополнение к УЗИ можно выявить нарушения экзокринной панкреатической функции. Во многих случаях прямая оценка панкреатической функции не может осуществляться длительное время, в связи с этим прямые тесты имеют в основном научное значение.
После получения клинических ультразвуковых признаков ХП у больного с четкой клинической картиной заболевания, дальнейшее исследование можно не проводить.
ЭРХПГ, КТ, МРТ занимают вторую ступень диагностического алгоритма. Применяются при возникновении сомнений или при необходимости получить детализированное представление:
ЭРХПГ дает возможность получить детальную информацию о протоковой системе;
- КТ: информация о жидкостных образованиях (кисты, внепанкреатические аномалии);
- МРТ чувствительна для выявления ранних фибротических изменений, предшествующих кальцификатам и грубым морфологическим изменениям.
Все технические исследования необходимы для осуществления дифференциальной диагностики ХП и рака ПЖ. Эндо-УЗИ и ЭРХПГ, КТ и МРТ дополняют друг друга. Комбинация эндо-УЗИ, КТ и ЭРХПГ повышает чувствительность диагностики до 95-97%, специфичность - до 100%.
При подозрении на рак ПЖ, гидатидный эхинококкоз, аутоиммунный панкреатит, туберкулез необходимо как можно более раннее проведение прицельной биопсии с последующим гистологическим или цитологическим исследованием.
Из-за высокого риска осложнений при ЭРХПГ и высокой стоимости исследования, предлагают проводить ЭУС, позволяющую также выполнить биопсию ПЖ.
Лабораторная диагностика
Лабораторная диагностика хронического панкреатита основана на определении активности ферментов ПЖ в крови и моче, диагностике экзо- и эндокринной недостаточности. Дополнительно проводят комплексное биохимическое и общеклиническое исследование крови.
Исследование содержания панкреатических ферментов в крови и моче.
1. Определение уровня амилазы в крови и моче
является наиболее распространенным диагностическим тестом. Имеет невысокую чувствительность в связи с кратковременностью гиперамилаземии и гиперамилазурии при панкреатитах.
Уровень амилазы крови начинает повышаться через 2-12 часов от начала обострения заболевания, через 20-30 часов достигает максимума и спустя 2-4 суток нормализуется (при благоприятном течении заболевания).
Содержание амилазы в моче начинает повышаться через 4-6 часов от начала обострения и через 8-10 часов (по некоторым данным - через 3 суток) может нормализоваться.
При тяжелом течении обострения ХП у больных с длительным анамнезом во многих случаях регистрируют нормальные или субнормальные величины амилазы.
Определение содержания амилазы в моче более информативно, чем в крови, так как гиперамилазурия более стойка, чем гиперамилаземия. В ряде случаев прямая связь между тяжестью панкреатита и активностью амилазы в крови и моче отсутствует.
Для повышения специфичности исследования амилазы в крови (особенно у больных с нормальным содержанием общей амилазы), следует определять не суммарное содержание фермента, а панкреатическую изоамилазу.
Специфичность определения панкреатической амилазы при ХП не превышает 88,6% при чувствительности 40,0-96,9%.
2. Определение сывороточной липазы
недостаточно чувствительно и информативно. По сывороточному уровню липазы невозможно определить тяжесть текущего обострения панкреатита и ближайший прогноз. Данные о сроках сохранения гиперферментемии варьируют, но они определенно больше, чем для амилазы.
3. Определение активности эластазы 1 в крови
считается наиболее "поздним" чувствительным тестом диагностики обострений ХП. Повышенный уровень фермента сохраняется в течение 8-10 дней после атаки. В этот период активность эластазы 1 в крови повышена у 100% больных, уровень липазы - у 85%, панкреатической изоамилазы - у 43%, общей а-амилазы - у 23% больных.
Выраженность гиперэластаземии не соответствует степени деструкции ткани ПЖ и не обладает большим диагностическим значением при функциональной недостаточности у больных с многолетним ХП.
Дифференциальный диагноз
Состояния, при которых необходима дифференциальная диагностика хронического панкреатита
(Nair R.J., Lawler L., Miller M.R., 2007)
Наиболее часто:
- острый холецистит;
- острый панкреатит;
- интестинальная ишемия или некроз;
- обструкция общего желчного протока;
- опухоли поджелудочной железы;
- язвенная болезнь;
- почечная недостаточность.
Редко:
- острый аппендицит;
- острый сальпингит;
- болезнь Крона;
- внематочная беременность;
- гастропарез;
- интестинальная обструкция;
- синдром раздраженного кишечника;
- различные заболевания, приводящие к развитию мальабсорбции;
- кисты яичника;
- папиллярная цистаденокарцинома яичника;
- грудная радикулопатия.
Осложнения
Холестаз (желтушный и безжелтушный);
- кровотечения (эрозивный эзофагит, синдром Меллори-Вейса, гастродуоденальные язвы);
- инфекционные осложнения (воспалительные инфильтраты, гнойные холангиты, перитониты, септические состояния);
- подпеченочная портальная гипертензия;
- тромбоз портальной и селезеночной вен;
- гипогликемические кризы;
- выпотной плеврит;
- обструкция ДПК;
- рак поджелудочной железы;
- панкреатический асцит;
- абдоминальный ишемический синдром.
Лечение за рубежом